Разработка и валидация методологии оценки потребления антимикробных препаратов у детей в условиях стационара
Разработать и валидировать методологию оценки потребления системных антимикробных препаратов (АМП) у пациентов детского возраста в условиях стационара.
Разработка методологии осуществлялась на основе стандартной ATC/DDD системы путем создания скорректированных детских DDD (сDDD) для пациентов в возрасте от 1 месяца до 12 лет. Валидация новой методологии проводилась в сравнении со стан дартной ATC/DDD системой, а также с объективными показателям потребления АМП в отделениях детской оториноларингологии и хирургии Смоленской областной клинической больницы за 2010 г.
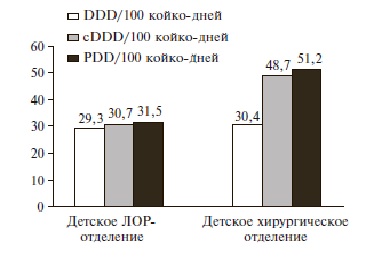
Общий уровень потребления системных АМП в отделении детской оториноларингологии и детской хирургии при использовании стандартной методологии составил 29,3 и 30,4 DDD/100 койко-дней, соответственно, скорректированной детской методологии – 30,7 и 48,7 сDDD/100 койко-дней, тогда как уровень потребления, рассчитанный путем анализа историй болезни в указанных отделениях, достигал 31,5 и 51,2 PDD/100 койко-дней.
Оценка потребления системных АМП у пациентов детского возраста с использованием разработанной методологии оказалась значительно более точной по сравнению со стандартной ATC/DDD системой, использование которой сопровождалось отчетливой тенденцией к занижению значений показателя.
Антимикробные препараты (АМП) – уникальный класс лекарственных средств, важность которых для клинической практики невозможно переоценить. Поскольку широкое и нерациональное использование АМП приводит к росту заболеваемости и смертности, сопровождается повышением частоты развития нежелательных лекарственных реакций, способствует селекции антибактериальной резистентности и повышению затрат на лечение [1], контроль за назначением указанных препаратов является неотъемлемым компонентом грамотной политики их применения.
Важную роль в процессе контроля и оптимизации использования АМП играют фармакоэпидемиологические исследования, в рамках которых производится анализ потребления лекарственных средств. Основным инструментом анализа является ATC/DDD методология, предложенная Всемирной организацией здравоохранения в качестве международного стандарта [2]. В основу методологии положена Анатомо-терапевтическо-химическая классификация (АТС, Anatomical Therapeutic Chemical Classification System), использующаяся для унификации группировки и подразделения лекарственных средств, а также установленная суточная доза лекарственного препарата (DDD, Defined Daily Dose). DDD представляет собой условную среднююподдерживающую суточную дозу лекарственного средства при его применении по основному показанию у взрослого человека массой 70 кг [2]. Необходимо отметить, что DDD является технической единицей измерения потребления лекарственных препаратов и может отличаться от рекомендуемой и применяющейся суточной дозы (PDD, Prescribed Daily Dose).
Несмотря на статус международного стандарта, ATC/DDD методология имеет ряд ограничений, одним из которых является невозможность корректной оценки потребления лекарственных средств в педиатрической популяции, так как дозировки препаратов у детей разного возраста значимо варьируются. Следовательно, применяющиеся в клинической практике средние суточные дозы могут существенно отличаться от DDD для конкретного препарата. В то же время, точность расчетов при использовании ATC/DDD методологии тем выше, чем ближе значение реально назначавшихся суточных доз к показателю DDD. Попытки оптимизировать оценку потребления АМП у детей, включая модификации стандартной ATC/DDD методологии и разработку кардинально новых подходов к решению данной задачи, предпринимаются в течение последних 20 лет, однако проблема все еще далека от решения.
Цель наcтоящего исследования – разработать и валидировать методологию оценки потребления системных АМП у пациентов детского возраста в условиях стационара.
Материал и методы
Разработка методологии оценки потребления у пациентов детского возраста проводилась для АМП следующих АТС групп: J01 – антибактериальные препараты для системного применения, J02 – антимикотики для системного применения и J05 – противовирусные препараты для системного применения, на основе стандартной ATC/DDD методологии путем создания скорректированных детских DDD (сDDD – средняя суточная доза АМП у ребенка с нормальной функцией печени и почек, рассчитанная исходя из массы тела в соответствии со стандартными подходами к дозированию препарата) для пациентов в возрасте от 1 месяца до 12 лет. Коррекция доз для пациентов старшего возраста была сочтена нецелесообразной, поскольку режимы дозирования АМП у них в большинстве случаев соответствуют таковым во взрослой популяции [3].
Исследование состояло из двух этапов:
1 этап – разработка значений сDDD системных АМП для каждой из приведенных возрастных групп: 1–11 мес,1 год, 2 года, 3 года, 4 года, 5 лет, 6 лет, 7 лет, 8 лет, 9 лет, 10 лет, 11 лет и 12 лет. При расчете сDDD использовали стандартные подходы к дозированию АМП, исходя из массы тела ребенка. Средняя масса тела детей в каждой возрастной группе была взята для пациентов обоего пола с распределением в популяции в соотношении 1:1 из центильных таблиц оценки физического развития ребенка (по S.M. Garn и С.G. Rohmann) в пределах 50% коридора значений [4].
2 этап – валидация и сравнительная оценка разработанной детской методологии со стандартной ATC/DDD методологией, а также с реальными данными потребления АМП на примере отделений детской оториноларингологии и детской хирургии ОГБУЗ "Смоленская областная клиническая больница".
С учетом вариаций в возрастном составе пациентов в отделениях расчет потребления в рамках детской методологии выполнялся с использованием средневзвешенного значения cDDD, складывавшегося из значений cDDD в каждой возрастной группе, помноженного на долю детей данной возрастной группы в популяции пациентов в отделении (табл. 1).
| Возрастная группа 1 | Возрастная группа 2 | Возрастная группа 3 | |
|---|---|---|---|
| Средневзвешенная сDDD = (сDDD-1×0,3) + (сDDD-2×0,5) + (сDDD-3×0,2) | |||
| сDDD | сDDD-1 | сDDD-2 | сDDD-3 |
| Доля детей данной возрастной группы в общей структуре за определенный период времени | 0,3 | 0,5 | 0,2 |
Данные о потреблении выражали в виде количества DDD и сDDD на 100 койко-дней, соответственно, и сравнивали с реальным потреблением АМП, полученным путем анализа историй болезни детей, госпитализированных в указанные отделения в 2010 г. (количество PDD на 100 койко-дней).
Результаты
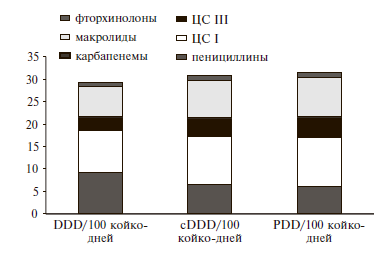
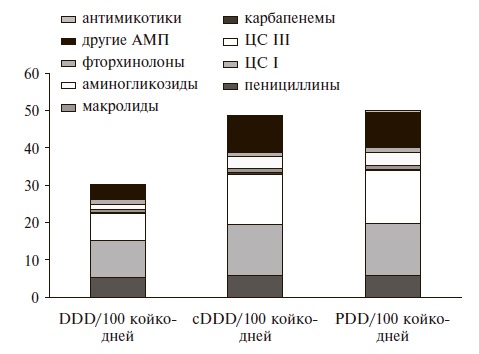
По результатам первого этапа исследования был разработан перечень сDDD, значения которых для наиболее широко применяющихся АМП представлены в табл. 2. Полученные cDDD были использованы для оценки структуры и уровня потребления АМП в отделениях детской оториноларингологии и детской хирургии ОГБУЗ "Смоленская областная клиническая больница" (рис. 1-3).
| АМП | Путь введения | DDD, г | Возраст | ||||||||||||
| 1-11 мес | 1 год | 2 года | 3 года | 4 года | 5 лет | 6 лет | 7 лет | 8 лет | 9 лет | 10 лет | 11 лет | 12 лет | |||
| Примечание: *О – перорально, Р - парентерально | |||||||||||||||
| Средняя масса тела | - | - | 7,30 | 11,89 | 13,23 | 14,78 | 16,6 | 17,75 | 18,75 | 20,98 | 25,3 | 28,15 | 31,0 | 34,6 | 38,7 |
| Бензилпенициллин | P | 3,6 | 0,44 | 0,71 | 0,79 | 0,89 | 1 | 1,07 | 1,13 | 1,26 | 1,52 | 1,69 | 1,86 | 2,08 | 2,32 |
| Ампициллин | P | 2 | 1,10 | 1,78 | 1,98 | 2,22 | 2,49 | 2,66 | 2,81 | 3,15 | 3,80 | 4,22 | 4,65 | 5,19 | 5,81 |
| Амоксициллин | O | 1 | 0,44 | 0,71 | 0,79 | 0,89 | 1 | 1,07 | 1,13 | 1,26 | 1,52 | 1,69 | 1,86 | 2,08 | 2,32 |
| Амоксициллин/клавуланат | O | 1 | 0,29 | 0,48 | 0,53 | 0,59 | 0,66 | 0,71 | 0,75 | 0,84 | 1,01 | 1,13 | 1,24 | 1,38 | 1,55 |
| Амоксициллин/клавуланат | P | 3 | 0,44 | 0,71 | 0,79 | 0,89 | 1 | 1,07 | 1,13 | 1,26 | 1,52 | 1,69 | 1,86 | 2,08 | 2,32 |
| Цефазолин | Р | 3 | 0,73 | 1,19 | 1,32 | 1,48 | 1,66 | 1,78 | 1,88 | 2,10 | 2,53 | 2,82 | 3,10 | 3,46 | 3,87 |
| Цефалексин | O | 2 | 0,33 | 0,54 | 0,60 | 0,66 | 0,75 | 0,80 | 0,84 | 0,94 | 1,14 | 1,27 | 1,40 | 1,56 | 1,74 |
| Цефотаксим | P | 4 | 0,73 | 1,19 | 1,32 | 1,48 | 1,66 | 1,78 | 1,88 | 2,10 | 2,53 | 2,82 | 3,10 | 3,46 | 3,87 |
| Цефтриаксон | P | 2 | 0,55 | 0,89 | 0,99 | 1,11 | 1,25 | 1,33 | 1,41 | 1,57 | 1,90 | 2,11 | 2,33 | 2,60 | 2,90 |
| Цефтазидим | P | 4 | 0,73 | 1,19 | 1,32 | 1,48 | 1,66 | 1,78 | 1,88 | 2,10 | 2,53 | 2,82 | 3,10 | 3,46 | 3,87 |
| Цефоперазон | P | 4 | 0,73 | 1,19 | 1,32 | 1,48 | 1,66 | 1,78 | 1,88 | 2,10 | 2,53 | 2,82 | 3,10 | 3,46 | 3,87 |
| Цефоперазон/сульбактам | P | 4 | 0,58 | 0,95 | 1,06 | 1,18 | 1,33 | 1,42 | 1,50 | 1,68 | 2,02 | 2,25 | 2,48 | 2,77 | 3,10 |
| Цефиксим | O | 0,4 | 0,06 | 0,10 | 0,11 | 0,12 | 0,13 | 0,14 | 0,15 | 0,17 | 0,20 | 0,23 | 0,25 | 0,28 | 0,31 |
| Цефепим | P | 2 | 0,37 | 0,59 | 1,98 | 2,22 | 2,49 | 2,66 | 2,81 | 3,15 | 3,80 | 4,22 | 4,65 | 5,19 | 5,81 |
| Имипенем | P | 2 | 0,73 | 1,19 | 1,32 | 1,48 | 1,66 | 1,78 | 1,88 | 2,10 | 2,53 | 2,82 | 3,10 | 3,46 | 3,87 |
| Меропенем | P | 2 | 0,73 | 1,19 | 1,32 | 1,48 | 1,66 | 1,78 | 1,88 | 2,10 | 2,53 | 2,82 | 3,10 | 3,46 | 3,87 |
| Эртапенем | P | 1 | 0,22 | 0,36 | 0,4 | 0,44 | 0,50 | 0,53 | 0,56 | 0,63 | 0,76 | 0,84 | 0,93 | 1,04 | 1,16 |
| Доксициклин | O | 0,1 | - | - | - | - | - | - | - | - | - | 0,11 | 0,12 | 0,14 | 0,15 |
| Доксициклин | P | 0,1 | - | - | - | - | - | - | - | - | - | 0,11 | 0,12 | 0,14 | 0,15 |
| Эритромицин | O | 1 | 0,37 | 0,59 | 0,66 | 0,74 | 0,83 | 0,89 | 0,94 | 1,05 | 1,27 | 1,41 | 1,55 | 1,73 | 1,94 |
| Эритромицин | P | 1 | 0,37 | 0,59 | 0,66 | 0,74 | 0,83 | 0,89 | 0,94 | 1,05 | 1,27 | 1,41 | 1,55 | 1,73 | 1,94 |
| Джозамицин | O | 2 | 0,37 | 0,59 | 0,66 | 0,74 | 0,83 | 0,89 | 0,94 | 1,05 | 1,27 | 1,41 | 1,55 | 1,73 | 1,94 |
| Кларитромицин | O | 0,5 | 0,11 | 0,18 | 0,2 | 0,22 | 0,25 | 0,27 | 0,28 | 0,31 | 0,38 | 0,42 | 0,47 | 0,52 | 0,58 |
| Азитромицин | P | 0,5 | 0,07 | 0,12 | 0,13 | 0,15 | 0,17 | 0,18 | 0,19 | 0,21 | 0,25 | 0,28 | 0,31 | 0,35 | 0,39 |
| Азитромицин | O | 0,3 | 0,07 | 0,12 | 0,13 | 0,15 | 0,17 | 0,18 | 0,19 | 0,21 | 0,25 | 0,28 | 0,31 | 0,35 | 0,39 |
| Гентамицин | P | 0,24 | 0,04 | 0,06 | 0,07 | 0,07 | 0,08 | 0,09 | 0,09 | 0,10 | 0,13 | 0,14 | 0,16 | 0,17 | 0,19 |
| Амикацин | P | 1 | 0,15 | 0,24 | 0,26 | 0,30 | 0,33 | 0,36 | 0,38 | 0,42 | 0,51 | 0,56 | 0,62 | 0,69 | 0,77 |
| Ванкомицин | P | 2 | 0,44 | 0,71 | 0,79 | 0,89 | 1 | 1,07 | 1,13 | 1,26 | 1,52 | 1,69 | 1,86 | 2,08 | 2,32 |
| Линезолид | O | 1,2 | 0,15 | 0,24 | 0,26 | 0,30 | 0,33 | 0,36 | 0,38 | 0,42 | 0,51 | 0,56 | 0,62 | 0,69 | 0,77 |
| Линезолид | P | 1,2 | 0,15 | 0,24 | 0,26 | 0,30 | 0,33 | 0,36 | 0,38 | 0,42 | 0,51 | 0,56 | 0,62 | 0,69 | 0,77 |
| Метронидазол | P | 1,5 | 0,16 | 0,27 | 0,3 | 0,33 | 0,37 | 0,40 | 0,42 | 0,47 | 0,57 | 0,63 | 0,70 | 0,78 | 0,87 |
| Нитрофурантоин | O | 0,2 | 0,05 | 0,08 | 0,09 | 0,10 | 0,12 | 0,12 | 0,13 | 0,15 | 0,18 | 0,20 | 0,22 | 0,24 | 0,27 |
| Фосфомицин | O | 3 | - | - | - | - | - | - | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| Фосфомицин | P | 8 | 0,58 | 0,95 | 1,06 | 1,18 | 1,33 | 1,42 | 1,50 | 1,68 | 2,02 | 2,25 | 2,48 | 2,77 | 3,10 |
| Флуконазол | O | 0,2 | 0,09 | 0,14 | 0,16 | 0,18 | 0,20 | 0,21 | 0,23 | 0,25 | 0,30 | 0,34 | 0,37 | 0,42 | 0,46 |
| Флуконазол | P | 0,2 | 0,09 | 0,14 | 0,16 | 0,18 | 0,20 | 0,21 | 0,23 | 0,25 | 0,30 | 0,34 | 0,37 | 0,42 | 0,46 |
| Амфотерицин В | P | 0,035 | 0,01 | 0,02 | 0,02 | 0,02 | 0,02 | 0,03 | 0,03 | 0,03 | 0,04 | 0,04 | 0,05 | 0,05 | 0,06 |
Общий уровень потребления системных АМП в отделении детской оториноларингологии и отделении детской хирургии при использовании стандартной методологии составил 29,3 и 30,4 DDD/100 койко-дней, скорректированной детской методологии – 30,7 и 48,7 сDDD/100 койко-дней, тогда как уровень потребления, рассчитанный путем анализа историй болезни в указанных отделениях, достигал 31,5 и 51,2 PDD/100 койкодней.
Отклонение уровня потребления АМП от действительного в отделении детской хирургии при использовании стандартной методологии составило 40,6% в меньшую сторону по сравнению с 4,9% для скорректированной детской методологии, в отделении детской оториноларингологии – 7,0% по сравнению с 2,5% соответственно (табл. 3). Таким образом, оценка общего уровня потребления АМП с использованием детской методологии оказалась значительно точнее стандартной ATC/DDD методологии, использование которой сопровождалось отчетливой тенденцией к занижению значения показателей потребления.
| Класс АМП | Стандартная ATC/ DDD методология | Детская ATC/DDD методология | ||
| Детское ЛОР отделение | Отделение детской хирургии | Детское ЛОР отделение | Отделение детской хирургии | |
| Примечание: *отрицательное значение означает тенденцию к занижению результатов по отношению к реальной ситуации, положительное – к завышению | ||||
| Пенициллины | 50,8 | -6,9 | 6,6 | 1,7 |
| Цефалоспорины | -20,0 | -39,0 | -3,2 | -3,2 |
| Карбапенемы | -20,0 | -50,0 | -20,0 | -40 |
| Аминогликозиды | - | -57,1 | - | -5,7 |
| Макролиды | -24,1 | -36,4 | -5,7 | -9,1 |
| Фторхинолоны | -10,9 | 0 | -10,0 | 0 |
| АМП разных групп | - | -57,6 | - | -1,0 |
| Системные антимикотики | - | -25,0 | - | -25,0 |
| Всего | -7,0 | -40,6 | -2,5 | 4,9 |
Анализ структуры потребления по классам АМП продемонстрировал схожие результаты. При этом более высокая точность измерения с помощью детской методологии в тех случаях, когда стандартная демонстрировала значимые отклонения от реального потребления, была характерна для аминогликозидов, пенициллинов, цефалоспоринов, макролидов, а также АМП разных групп (АТС J01Х), включая гликопептиды и нитроимидазолы (табл. 3).
Обсуждение
Потребление АМП в условиях стационара варьируется в широких пределах, что обусловлено не только объективными различиями в характеристиках стационаров и контингенте пациентов, локальными стандартами и сложившейся практикой применения препаратов, но и подходами к оценке показателя. Погрешности, вносимые некорректной методологией оценки, могут быть существенными и оказывать значимое влияние на интерпретацию результатов. В то же время, достоверная информация о качественных и количественных аспектах потребления АМП важна для разработки и внедрения адресных стратегий снижения их избыточного и нерационального использования.
Исходя из потребности в надежной и универсальной методологии, в 1981 г. Всемирной организацией здра воохранения в качестве международного стандарта оценки потребления лекарственных средств была предложена ATC/DDD система [2]. Популярность данной методологии отражает удобство ее применения и возможность сравнения потребления препаратов различных групп, а также в различных лечебных учреждениях, в том числе в разных странах. Существенным преимуществом методологии является проведение расчетов на основе агрегированных данных о закупках лекарственных средств без необходимости в сборе информации о назначениях на уровне индивидуальных пациентов, что, при отсутствии электронных записей, является крайне трудоемким процессом, требующим больших затрат времени [5].
Однако у ATC/DDD системы есть ряд недостатков, связанных как с используемой для категоризации препаратов АТС классификацией, так и с единицей измерения потребления – DDD. Установленная суточная доза – DDD – была разработана и внедрена норвежскими учеными совместно с Советом северных стран по лекарственным препаратам (Уппсала, Швеция) в 1976 г. [2] в качестве универсальной единицы количественной оценки потребления лекарственных средств независимо от конкретного препарата, его стоимости, форм и единиц дозирования [6]. В то же время, поскольку DDD является технической единицей и не соответствует рекомендованным или реально назначаемым дозам препаратов, ее использование может приводить к существенным погрешностям в оценке потребления лекарственных средств. Так, в исследовании, выполненном A. Muller и соавт. [7], на популяции взрослых пациентов, получавших лечение в 2001 г. на базе университетской больницы скорой и неотложной помощи, преимущественно в отделениях общего и хирургического профиля, было показано завышение расчетного уровня потребления АМП на 40% вследствие отклонения DDD от реальных дозировок, применявшихся в стационаре. Аналогичная тенденция была продемонстрирована и в ряде других исследований [8-10].
Особую актуальность эта проблема приобретает при анализе потребления лекарств у больных с нестандартными подходами к дозированию лекарственных средств, в первую очередь детей, вследствие значительного отклонения реальных доз, назначаемых детям, от утвержденных DDD, а также вариаций педиатрических доз в различных возрастных группах. Причиной тому является стандартный для детской популяции подход к дозированию лекарственных препаратов из расчета на килограмм массы тела.
Таким образом, можно выделить несколько огра ничений использования стандартной ATC/DDD методологии для оценки потребления лекарственных средств в педиатрической популяции: отсутствие адаптации DDD к дозам, применяющимся у детей в клинической практике, а также неоднородность популяции в различных учреждениях и в одном учреждении в различные периоды времени [11,12]. Немаловажным является также тот факт, что основные показания, по которым препарат применяется в педиатрической практике, могут отличаться от таковых у взрослых пациентов, обусловливая исходные различия в подходах к дозированию.
В течение последних двух десятилетий неоднократно предпринимались и продолжают предприниматься попытки повысить точность оценки потребления лекарственных препаратов в педиатрической популяции. К основным препятствиям к разработке универсальных методов оценки следует отнести широкий диапазон дозировок, применяющихся в различных возрастных группах, определяющий необходимость индивидуального подхода к каждой и не позволяющий внедрить единую систему DDD, а также непредсказуемость распределения пациентов по возрасту, требующую адаптации расчетов к ситуации, сложившейся в конкретном стационаре в заданный период времени.
В то же время, для получения корректных результатов, расчет педиатрических доз, в том числе в рамках оценки потребления, должен проводиться с учетом показателей массы тела конкретных пациентов или среднего показателя массы тела в популяции, для которой проводится этот расчет. Поскольку доступ к информации о демографических характеристиках пациентов и индивидуальных назначениях лекарственных препаратов в реальной практике часто ограничен, приходится прибегать к косвенным показателям оценки массы тела пациентов в популяции, например, возрасту.
Так, Z.C. Zhang [16] при оценке адекватности дозирования АМП в педиатрической популяции стратифицировал пациентов по возрасту. Пациенты были разделены на пять групп, каждой из которых были присвоены свои значения DDD: 1–6 месяцев – DDD0=1/7DDD; 6–12 месяцев – DDD1=1/5DDD; 1–4 года – DDD2=1/3DDD; 4–8 лет – DDD3=1/2DDD; 8–15 лет – DDD4=2/3DDD. Необходимо отметить, что разработанные DDD не были специфичными для конкретных препаратов, базировались на возрасте без привязки к массе тела и не рассматривались авторами как инструмент оценки потребления лекарственных средств.
Разработка специфичных для препаратов детских DDD (cDDD) была выполнена Lu Han и соавт. [17] в 2009 г. Под cDDD исследователи понимали расчетную среднюю поддерживающую дозу препарата в сутки на единицу массы тела при его использовании по основному показанию у ребенка по аналогии со стандартными DDD. При этом сDDD для ряда препаратов были представлены в виде интервалов в зависимости от особенностей применения.
Т.В. Liem и соавт. [11] в 2010 г. предложили специальные DDD для 10 АМП, наиболее часто применяющихся у новорожденных в условиях ОРИТ. Расчет данных DDD проводился, исходя из предположительной массы тела ребенка 2 кг, на основе стандартов дозирования препаратов и мнения экспертов. В 2011 г. на базе исследований, выполненных Z.C. Zhang и и соавт. [18] был предложен подход к созданию системы детских DDD для оценки оптимальности дозирования препаратов в педиатрической практике.
Необходимо подчеркнуть, что все вышеописанные разработки выполнялись исключительно с целью оценки адекватности дозирования в педиатрической популяции. Валидация доз, как правило, не проводилась, и возможность их использования для оценки потребления лекарственных средств не исследовалась.
В 2012 г. А. Porta и соавт. [19] в ходе международного пилотного исследования на базе четырех стационаров Европы (Великобритания, Греция, Италия) был предложен алгоритм сравнительной оценки потребления АМП у пациентов детского возраста. Для наиболее широко применявшихся препаратов исследователи стратифицировали дозы для трех весовых групп (масса тела <10, 10–25 и ≥25 кг). Анализ уровней потребления проводился изолированно в каждой группе на основе стандартной ATC/DDD методологии с учетом реально назначавшихся доз (PDD).
R. Raastad и соавт. [20] в 2014 г. для сравнения потребления АМП в педиатрической популяции в динамике использовали рекомендованные суточные дозы в отношении к килограммо-дням, показавшие, по мнению авторов работы, более высокую точность, особенно в популяции новорожденных. Расчет доз выполнялся на основе национальных рекомендаций с использованием среднестатистических показателей массы тела для пациентов соответствующего возраста и пола.
Несмотря на вышеописанные исследования, эффективной и доступной к использованию в реальной клинической практике методики оценки потребления лекарственных средств у детей до настоящего времени не создано, в силу чего проблема остается далекой от решения. В ходе выполненной нами работы была предпринята первая попытка разработать универсальную методологию оценки потребления АМП в детской популяции, применимую не только для отслеживания тенденций в пределах одного лечебного учреждения, но и для сравнения показателя между различными учреждениями.
За основу нами была взята ATC/DDD система, как стандарт оценки потребления лекарственных средств. Поскольку основные погрешности использования данной методологии у пациентов детского возраста связаны с расхождением взрослых DDD с дозами, назначающимися детям в реальной клинической практике, было принято решение пойти по пути коррекции доз с целью максимального их приближения к реальным. При этом было решено сконцентрироваться на популяции пациентов в возрасте до 12 лет включительно, поскольку у детей старшей возрастной группы дозы АМП, как правило, соответствуют таковым во взрослой популяции.
Стандартным подходом к дозированию лекарственных средств в педиатрической практике является расчет, исходя из массы тела пациента. Однако стратификация по массе тела и расчет дозировок для различных весовых групп, как в описанных выше работах зарубежных исследователей, были признаны нецелесообразными, поскольку дальнейшее использование методологии потребовало бы сбора информации о распределении пациентов в стационаре по массе тела. В связи с этим было принято решение использовать в качестве признака стратификации пациентов коррелирующий с массой тела показатель, который входит в типовой отчет лечебно-профилактического учреждения – возраст.
Таким образом, пациенты были стратифицированы нами по возрасту с шагом 1 год, за исключением группы детей первого года жизни, из которой с учетом особенностей дозирования были исключены новорожденные. Для каждой группы на основании данных официальной статистики демографических показателей РФ, представленной в виде центильных таблиц, была определена среднестатистическая масса тела, на основе которой производился расчет рекомендованной суточной дозировки, исходя из инструкций препаратов и национальных стандартов их назначения в терапии инфекционных заболеваний.
Для каждой возрастной группы была разработана система универсальных сDDD, на основе которых в дальнейшем выполнялся расчет средневзвешенного значения DDD в реальной популяции пациентов с учетом доли пациентов каждой возрастной группы, вошедшей в популяцию. Использование средневзвешенного показателя позволило учесть возрастную структуру популяции и максимально приблизить cDDD к реально назначенным дозам, благодаря чему предложенная методология может применяться не только для оценки потребления лекарственных средств, но и для проведения сравнений как в одном ЛПУ в различные периоды времени, так и между несколькими ЛПУ с различным возрастным контингентом пациентов.
Основным преимуществом представленной методологии является более высокая точность по сравнению со стандартной ATC/DDD системой. Так, согласно проведенной нами оценке, расчеты с использованием скорректированной детской методологии были значительно ближе к объективным показателям потребления АМП. В пользу методологии свидетельствует относительная простота расчетов и доступность информации для их проведения. Фактически, для оценки потребления достаточно агрегированных данных о закупках лекарственных средств и информации о возрастной структуре пациентов за заданный период времени. Таким образом, она может быть использована в стационарах, не оснащенных медицинскими инфор мационными системами и не ведущих в рутинном порядке учет демографических характеристик и индивидуальных назначений на уровне каждого пациента.
Необходимо, однако, отметить, ряд ограничений данной методологии. К их числу следует отнести преимущественно расчетный характер представленных cDDD. В то же время, даже в таком несовершенном виде данная методология продемонстрировала значимо более высокую точность оценки потребления по сравнению со стандартной как для АМП в целом, так и для отдельных классов препаратов. Приближение разработанных cDDD к реально применяющимся в клинической практике дозам является предметом дальнейшей работы.
Актуальным остается вопрос о соответствии использованных при проведении расчетов показателей массы тела, приведенных в центильных таблицах, реальным показателям массы тела у пациентов детского возраста в стационарах. Погрешности возможны как в связи с динамикой показателя в популяции с течением времени, так и в связи с вариациями массы тела в пределах одной возрастной группы в различных регионах нашей страны.
В дополнительном изучении нуждается полезность применения новой методологии для оценки потребления АМП в отделениях различного профиля детских стационаров, исходя из возрастной структуры пациентов, а также вопрос о целесообразности ее использования во взрослых многопрофильных стационарах с педиатрическими отделениями.
Нельзя не упомянуть, что актульность детской методологии для анализа потребления различных классов АМП была неодинаковой. Очевидно, что расчеты на основе стандартной ATC/DDD методологии сопровождаются тем более выраженными погрешностями при оценке потребления АМП, чем больше дозы в реальной клинической практике отклоняются от DDD. Необходимы дальнейшие исследования для определения классов препаратов, а также возрастных групп пациентов, анализ потребления у которых наиболее целесообразно проводить с использованием скорректированной детской методологии.
Заключение
Нами предложена новая универсальная методология оценки потребления АМП в педиатрической популяции, разработанная на основе стандартной ATC/DDD системы. Использование описанного подхода позволяет получить значительно более точное представление об истинном потреблении системных АМП у пациентов в возрасте от 1 месяца до 12 лет в условиях стационара по сравнению со стандартной ATC/DDD методологией.
Необходимо проведение дальнейших исследований для оптимизации разработанных детских DDD и изучения полезности использования новой методологии для оценки потребления различных групп АМП в отделениях различного профиля детских и взрослых многопрофильных стационаров.
Используемые источники
- Shorr AF. Epidemiology and economic impact of meticillin-resistant Staphylococcusaureus: review and analysis of the literature. Pharmacoeconomics 2007;25:751–68.
- Доступно на сайте www.whocc.no/atc_ddd_methodology/ purpose_of_the_atc_ ddd_system/.
- Практическое руководство по антиинфекционной химиотерапии. Под ред. Страчунского Л.С., Белоусова Ю.Б., Козлова С.Н. Смоленск: МАКМАХ, 2007.
- Воронцов И.М., Мазурин А.В. Пропедевтика детских болезней. 3-е изд. СПб: ООО “Издательство Фолиант”; 2009.
- Monnet D. Measuring antimicrobial use: theway forward. Clin Infect Dis 2007;44:671–3.
- WHO Collaborating Centre for Drug Statistics Methodology. Guidelines for ATC classification and DDD assignment. 2010. Oslo, Norway, 2009.
- Muller A, Monnet DL, Talon D, et al. Discrepancies between prescribed daily doses and WHO defined daily doses of antibacterials at a university hospital.Br J Clin Pharmacol 2006;61(5):585-91.
- de With K, Maier L, Steib-Bauert M, et al. Trends in antibiotic use at a universi- ty hospital: defined or prescribed daily doses? Patient days or admissions as denominator? Infection 2006;34:91–4.
- Ruef C. What’s the best way to measure antibiotic use in hospitals? Infection 2006;34:53–4.
- Shetka M, Pastor J, Phelps P. Evaluation of the defined daily dose method for estimating anti-infective use in a university hospital. Am J Health Syst Pharm 2005;62:2288–92.
- Liem TB, Heerdink ER, Egberts ACG, Rademaker CMA. Quantifying antibiotic use in paediatrics: a proposal for neonatal DDDs. Eur J Clin Microbiol Infect Dis 2010;29:1301–3.
- Amadeo B, Zarb P, Muller A. European Surveillance of Antibiotic Consumption (ESAC) point prevalence survey 2008: paediatric antimicrobial prescribing in 32 hospitals of 21 European countries. J Antimicrob Chemother 2010;65:2247–52.
- Polk RE, Fox C, Mahoney A, et al. Measurement of adult antibacterial drug use in 130 US hospitals: comparison of defined daily dose and days of therapy. Clin Infect Dis 2007;44:664–70.
- de With K, Bestehorn H, Steib-Bauert M, Kern WV. Comparison of defined ver- sus recommended versus prescribed daily doses for measuring hospital antibiotic consumption. Infection 2009;37:349–52.
- Pakyz AL, Gurgle HE, Ibrahim OM, et al. Trends in antibacterial use in hospital- ized pediatric patients in United States academic health centers. Infect Control Hosp Epidemiol 2009;30:600–3.
- Zhang ZC. The analysis of rationality of antibiotics in pediatric department. Anhui Med Pharm J 2005;9(12):934–6.
- Han L, Zeng LN, Guo YC, et al. Utilization analysis of drug efficacy of the 392 cases of Wenchuan earthquake women and children patients. Chin J Evid-Based Med 2009;9(3):265–72.
- Zhang L, Li Y, Zeng L, Wang Z. Applying "children defined daily dose" to assess appropriate dose in pediatrics. J Evid Based Med 2012;5(1):2-5.
- Porta A, Hsia Y, Doerholt K, et al. Comparing neonatal and paediatric antibiotic prescribing between hospitals: a new algorithm to help international benchmark- ing. J Antimicrob Chemother 2012;67:1278–86.
- Raastad R, Tvete IF, Abrahamsen TG, et al. A worrying trend in weight-adjusted paediatric antibiotic use in a Norwegian tertiary care hospital. Acta Paediatr 2015;104(7):687-92.
