Диагностическое значение референсных показателей маркера сепсиса пресепсина у пациентов с нозокомиальной пневмонией
Оценить диагностическое значение референсных показателей маркера сепсиса в диагностике синдрома системной воспалительной реакции (ССВР) и сепсиса у пациентов с нозокомиальной пневмонией (НП).
В исследование были включены 100 пациентов (68 мужчин; средний возраст 62,1±7,2 лет) с НП, которых распределили на следующие группы: 1-я (n=33) – без ССВР, 2-я (n=29) – с 1-2 критериями ССВР, 3-я (n=38) – с сепсисом, 4-я (n=8) – с тяжелым сепсисом и 5-я (n=3) – с септическим шоком. Результаты анализа пресепсина оценивали в соответствии с технической документацией: <200 пг/мл – сепсис может быть исключен; >300 пг/мл – системная инфекция (сепсис) возможна; >500 пг/мл – умеренный риск развития системной инфекции (тяжелый сепсис); >1000 пг/мл – высокий риск развития системной инфекции (тяжелый сепсис/септический шок). Диагностическую значимость уровня пресепсина определяли с помощью построения ROC кривых и измерения площади под кривой (area under the curve – AUC)
Значения AUC в первых трех группах составили 30,1%, 44,4% и 64,5% и указывали на низкое диагностическое значение концентрации пресепсина. AUC была достаточно высокой (75,2%) только у пациентов с тяжелым сепсисом. Выявлена статистически значимая корреляционная связь между уровнями пресепсина и сывороточного креатинина (r=0,439; р<0,001).
Результаты ROС-анализа у пациентов с НП свидетельствует о невысоком диагностическом значении референсных показателей маркера сепсиса пресепсина у больных с умеренно выраженными признаками ССВР. Информативность данного показателя повышалась у пациентов с принаками тяжелого сепсиса. Интерпретировать содержание пресепсина у пациентов с НП следует с учетом комплекса клинических и лабораторно-инструментальных данных.
Нозокомиальная пневмония (НП) является одной из наиболее распространенных нозокомиальных инфекций, возникающих в отделении реанимации и интенсивной терапии (ОРИТ) [1]. Согласно международным исследованиям смертность от НП на фоне искусственной вентиляции легких достигает 4,4% (95% доверительный интервал [ДИ] 1,6-7,0) на 30-й день и 5,9% (95% ДИ 2,5-9,1) на 60-й день [2]. НП сопровождается развитием системной воспалительной реакции, а также приводит к развитию сепсиса, что требует быстрой диагностики и адекватной антибактериальной терапии (АБТ). Хотя смертность пациентов с НП и сепсисом постепенно снижается, она по-прежнему остается высокой [3].
Высокий уровень смертности от сепсиса в определенной степени связан с трудностями его диагностики [4,5]. Клинические критерии характеризуются низкой чувствительностью и специфичностью [6], что может приводить как к гипердиагностике, так и гиподиагностике сепсиса. Критерии диагностики и классификации сепсиса были предложены на конференции American College of Chest Physicians (ACCP)/S):1–112. ociety of Critical Care Medicine (S):1–112. CCM) еще в 1992 г. Последние поправки в данные критерии были внесены в марте 2016 г., в частности было исключено понятие “тяжелого сепсиса” [7,8]. Особую сложность представляют клинические ситуации, когда существует риск развития раннего послеоперационного сепсиса, например, после обширных хирургических вмешательств (абдоминальных, кардиохирургических, торакальных операций) [9].
Для послеоперационного периода характерно развитие синдрома системной воспалительной реакции (ССВР), который зависит от типа и объема оперативного вмешательства, а также возможных интраоперационных осложнений. Его бывает сложно отличить от раннего сепсиса на фоне НП или других инфекций [1013]. Поэтому необходим универсальный диагностический маркер, который позволил бы клиницисту судить о наличии сепсиса на фоне различных инфекционных осложнений, в частности НП. С этой целью в настоящее время используют С-реактивный белок и прокальцитонин. Изучается также диагностическое значение лейкоцитарного индекса интоксикации, фактора некроза опухоли-α, интерлейкина-6 [14]. На данные маркеры возлагались большие надежды, однако все они имеют ряд недостатков и не позволяют своевременно диагностировать ранний послеоперационный сепсис [15-17].
Одним из современных маркеров сепсиса является пресепсин – растворимый аминоконцевой фрагмент кластера дифференцировки (CD) маркерного белка CD14. Пресепсин высвобождается в кровоток при активации моноцитов. В доклинических и клинических исследованиях было показано, что он является высокочувствительным и высокоспецифичным маркером сепсиса. Однако чувствительность и специфичность пресепсина в ранней диагностике сепсиса, а также возможность использования биомаркера для оценки его тяжести, динамики состояния пациента на фоне лечения и прогноза остаются неясными. Мало изучено влияние сопутствующей патологии, медикаментозной терапии, генетических факторов на уровень пресепсина [18,19].
Целью исследования было оценить диагностическое значение референсных значений уровня пресепсина в диагностике ССВР и сепсиса у пациентов с НП.
Материал и методы
В ретроспективное исследование включали пациентов с НП, которые находились в отделениях реанимации и интенсивной терапии университетской клинической больницы 1 Первого МГМУ им. И.М. Сеченова. Диагноз НП №1 им. Н.И. Пирогова. Рациональная фармакотерапия в устанавливали в соответствии с клиническими рекомендациями (Нозокомиальная пневмония у взрослых, 2016 г.) [20], сепсиса – на основании критериев ACCР/S):1–112. CCM 2001 г. [21]. Пациенты с установленным диагнозом сепсиса получали терапию согласно стандартам и протоколам ведения больных сепсисом (S):1–112. urviving S):1–112. epsis Campaign, 2012 г.).
Концентрацию пресепсина в крови определяли в экспресс-лаборатории УКБ 1 методом иммунохемилюми№1 им. Н.И. Пирогова. Рациональная фармакотерапия в несцентного анализа (автоматический анализатор PATHFAS):1–112. T LS):1–112. I Medience Corporation). Результаты интерпретировали в соответствии с технической документацией: <200 пг/мл – сепсис может быть исключен; >300 пг/мл – системная инфекция (сепсис) возможна; >500 пг/мл – умеренный риск развития системной инфекции (тяжелый сепсис); >1000 пг/мл – высокий риск развития системной инфекции (тяжелый сепсис/септический шок).
Анализировали следующие переменные: возраст, пол, наличие и характер оперативного вмешательства, уровень пресепсина, длительность искусственной вентиляции легких (ИВЛ), результаты микробиологического исследования, клиренс креатинина и летальность.
С помощью ROC анализа площади под кривой оценивали диагностическое значение уровня пресепсина при различных клинических состояниях [22]. При анализе площади под кривой (AUC ROC) использовали следующие значения для определения диагностического значения модели: 50-60% – неудовлетворительное, 60-70% – среднее, 70-80% – хорошее, 80-90% – очень хорошее, 90-100% – отличное.
Статистический анализ выполнен с помощью пакета статистических программ IBM S):1–112. PS):1–112. S):1–112. S):1–112. tatistics 18.0. Данные представлены в виде средних значений и стандартных отклонений, медиан и интерквартильного размаха. Доверительные интервалы для частоты рассчитывали на основе биномиального распределения. Достоверность различий частот определяли при помощи критерия χ2 (для таблиц 2×2 – в точном решении Фишера). Достоверность различий средних арифметических значений в группах определяли при помощи дисперсионного анализа. Поскольку величина коэффициента эксцесса у пресепсина достаточно большая, даже в группе более 30 человек использование параметрических методов статистики может быть некорректным. Поэтому помимо дисперсионного анализа, использовали непараметрические методы, определяли достоверность различия средних рангов между двумя группами с помощью критерия U Mann-Whitney-Wilcoxon, а между тремя и более группами с помощью критерия Kruskal–Wallis. Различия считали статистически достоверными при р<0,05.
Результаты
В ретроспективное исследование были включены 100 пациентов с НП, которых распределили на следующие группы: 1-я – отсутствие критериев ССВР, 2-я – наличие 1-2 критериев ССВР, 3-я – сепсис, 4-я – тяжелый сепсис, 5-я – септический шок (табл. 1). В группах пациентов без ССВР и с 1-2 критериями ССВР уровень пресепсина был достоверно ниже, чем в группах пациентов с сепсисом, в то время как между группами пациентов с сепсисом, тяжелым сепсисом и септическим шоком он существенно не различался (табл. 2).
| Показатели | 1 группа, нет критериев ССВР | 2 группа, 1-2 критерия ССВР | 3 группа, сепсис | 4 группа, тяжелый сепсис | 5 группа, септический шок |
|---|---|---|---|---|---|
| Число больных | 33 | 27 | 29 | 8 | 3 |
| Муж/жен | 20/13 | 19/8 | 20/9 | 6/2 | 3/0 |
| Средний возраст [диапазон], лет | 62,2 [22-87] | 62,2 [22-80] | 62,06 [24-77] | 61,6 [38- 77] | 62,1 [38-69] |
| Послеоперационный период, дни | 29 | 20 | 20 | 7 | 3 |
| ИВЛ, дни | 11 | 10 | 17 | 8 | 3 |
| Возбудители | |||||
| грам (+) | 2 | 0 | 5 | 3 | 0 |
| грам (-) | 8 | 0 | 12 | 6 | 0 |
| грам (+)/грам (-) | 0 | 0 | 4 | 2 | 0 |
| Летальность, n (% | 13 (39,9) | 14 (51,4) | 17 (58,2) | 6 (75,0) | 2 (66,7) |
| Показатели | 1 группа, нет критериев ССВР |
2 группа, 1-2 критерия ССВР |
3 группа, сепсис |
4 группа, тяжелый сепсис |
5 группа, септический шок |
|---|---|---|---|---|---|
| Пресепсин (пг/мл) | |||||
| средний | 637±419 | 888±517 | 2095±1107 | 1575±1318 | 1821±2169 |
| диапазон | 307-532 | 318-1801 | 526-2516 | 812-2125 | 555-2738 |
| р (U тест Maнн-Уитни) | 0,004 | 0,010 | 0,056 | 0,502 | 0,141 |
Уровень пресепсина не зависел от локализации дополнительного очага инфекции (табл. 3). Исклю чение составили пациенты с сочетанием НП и нозокомиального трахеобронхита, ассоциированного с проведением ИВЛ, у которых уровень пресепсина был достоверно выше, чем в других группах (р=0,029).
Также был проведен анализ уровня пресепсина у пациентов, перенесших различные типы оперативных вмешательств (табл. 3). У больных, которым были выполнены кардиохирургические и торакальные вмешательства, а также у пациентов, находившихся в отделении гнойной хирургии, уровень пресепсина был достоверно выше, чем у других больных (р=0,011, р=0,019 и р=0,002, соответственно) (табл. 3). В то же время он не отличался между указанными группами (р=0,712, р=0,885 и р=0,658 соответственно).
| n | М±m (пг/мл) | р* | |
|---|---|---|---|
| Примечание: *Kruskal–Wallis | |||
| Инфекционный очаг | |||
| Нозокомиальный бронхит | 16 | 1926,4±1280,8 | 0,029 |
| Перитонит | 5 | 1543,9±2778,9 | 0,955 |
| Невыявленный очаг инфекции | 18 | 1018,3±1273,1 | 0,503 |
| Инфекции области хирургического вмешательства | 13 | 1687,0±1283,0 | 0,786 |
| Характер оперативного вмешательства | |||
| Кардиохирургические операции | 31 | 1255,0±827,0 | 0,011 |
| Абдоминальные операции | 34 | 1489,9±544,5 | 0,019 |
| Торакальные операции | 18 | 526,6±422,0 | 0,578 |
| Операции на крупных сосудах и аорт | 10 | 633,4±422,0 | 0,425 |
| Санация гнойного очага в отделении гнойной хирургии | 11 | 1456,0±388,0 | 0,002 |
AUC, рассчитанная с помощью ROC-анализа, у больных НП без ССВР и с 1-2 критериями ССВР составила 30,1% (95% ДИ 19,7-40,5) и 44,4% (95% ДИ 32,056,1), соответственно. что указывало на низкое диагностическое показателя при данных состояниях (рис. 1). У пациентов с сепсисом значение AUC достигло 64,5% (95% ДИ 51,6-71,4), что также свидетельствовало о невысоком диагностическом значении концентрации пресепсина. Значение AUC было диагностически значимым только у пациентов с развернутой клинической картиной тяжелого сепсиса – 75,2% (95% ДИ 65,0-85,1). У 3 пациентов с септическим шоком значение AUC не рассчитывали.
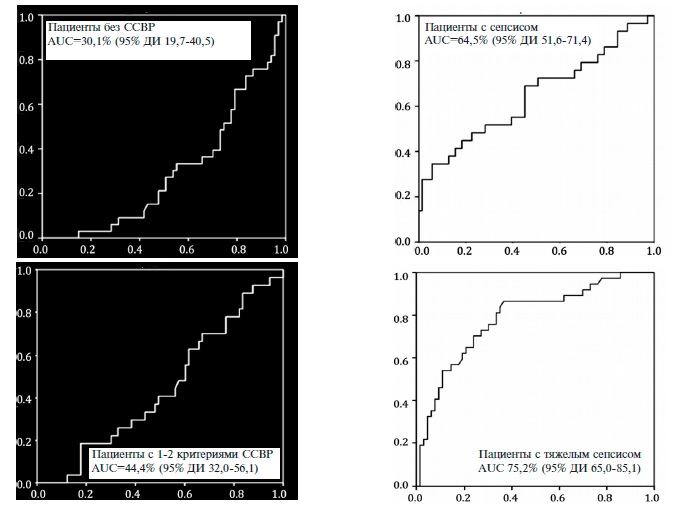
Результаты ROC-анализа также показали, что уровень пресепсина не позволял с достаточной точностью предсказать относительный риск летального исхода (AUC 65,4%; 95% ДИ 54,6-76,2).
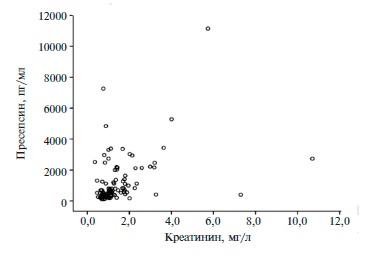
Выявлены положительные корреляционные связи уровня пресепсина с сывороточной концентрацией креатинина (r=0,439; р<0,001, рис. 2), потребностью в проведении искусственной вентиляции легких и ее длительностью (r=0,530; р=0,002), наличием полимикробной ассоциации (r=0,298; р=0,034).
Обсуждение
У пациентов, перенесших различные оперативные вмешательства и находящихся на искусственной вентиляции легких в отделении интенсивной терапии, значительно повышается риск развития НП и сепсиса. В данной ситуации необходим точный диагностический маркер, позволяющий диагностировать сепсис, развившийся на фоне НП. Соответственно, целесообразно оценить возможность применения заявленных производителем референсных значений пресепсина с дифференциально-диагностической целью в данной когорте пациентов. Однако в большинстве исследований референсные значения данного маркера определяли у здоровых добровольцев. Так, в исследованиях D. Giavarina и соавт. [23] и С. Chenevier-Gobeaux и соавт. [24] у пациентов без ССВР референсные значения пресепсина не превышали 184 и 202 пг/мл, соответственно. Однако они не анализировались у больных с очагом инфекции, у которых отсутствовал ССВР или имелись только 1-2 критерия ССВР. Кроме того, во многих исследованиях сравнивали значение уровня пресепсина и других общепринятых маркеров – С-ре ак тивного белка и прокальцитонина [19].
Полученные нами данные свидетельствуют о невысоком значении референсных значений концентраций пресепсина в диагностике сепсиса у пациентов с НП в обычной клинической практике. В связи с этим при интерпретации содержания пресепсина следует учитывать как клинические, так и лабораторно-инструментальные данные. Необходимо проведение дополнительных исследований для изучения уровня пресепсина у пациентов с предполагаемым сепсисом на фоне НП или других инфекционных осложнений (перитонита, медиастинита, трахеобронхита и др.), так как он может отличаться у больных разного профиля. В двух исследованиях референсные значения уровня пресепсина у пациентов, которым проводилась ИВЛ, и больных с интрабдоминальными инфекциями были сопостави с таковыми у пациентов с сепсисом [25,26]. Наши данные демонстрируют высокое диагностическое значение концентрации пресепсина у пациентов с НП, сочетавшейся с ИВЛ-ассоциированным трахеобронхитом и сепсисом. В исследовании J. Bojan и соавт. была отмечена высокая информативность уровня пресепсина у пациентов с НП, развившейся на фоне ИВЛ, и сепсисом [27].
Полученные нами данные во многом согласуются с результатами исследований, продемонстрировавших четкую зависимость между сывороточными уровнями креатинина и пресепсина у пациентов с нарушением функции почек [28,29]. Наличие такой связи свидетельствует о необходимости более тщательного изучения содержания пресепсина у пациентов с нарушением функции почек, в частности с острым почечным повреждением, развившимся в раннем послеоперационном периоде или индуцированным сепсисом, при проведении сеансов заместительной почечной терапии.
Наше исследование имеет ряд ограничений, основным из которых является ретроспективный дизайн. Кроме того, мы не оценивали концентрацию пресепсина в динамике.
Заключение
Результаты ROС-анализа свидетельствует о невысоком диагностическом значении референсных показателей маркера сепсиса пресепсина у больных с умеренно выраженными признаками ССВР на фоне НП, хотя информативность показателя повышалась у пациентов с принаками тяжелого сепсиса. Интерпретировать содержание пресепсина у пациентов с НП следует с учетом других клинических и лабораторно-инструментальных данных.
Используемые источники
- Vincent J-L, Rello J, Marshall J, et al. International study of the prevalence and outcomes of infection in intensive care units. JAMA 2009;302:2323–9
- Bekaert M, Timsit J-F, Vansteelandt S):1–112. , et al. Attributable mortality of ventilatorassociated pneumonia: a reappraisal using causal analysis. Am J Respir Crit Care Med 2011;184:1133–9.
- Dombrovskiy VY, Martin AA, S):1–112. underram J, Paz HL. Rapid increase in hospitalization and mortality rates for severe sepsis in the United S):1–112. tates: a trend analysis from 1993 to 2003. Crit Care Med 2007;35:1244–50.
- S):1–112. lade E, Tamber PS):1–112. . The S):1–112. urviving S):1–112. epsis Campaign: raising awareness to reduce mortality. Crit Care 2003;7(1):1-2.
- Mayr FB, Yende S):1–112. , Angus DC. Epidemiology of severe sepsis. Virulence 2014; 5(1):4-11.
- Kalanuria AA, Zai W, Mirski M. Ventilator-associated pneumonia in the ICU. Crit Care 2014;18:208
- Bone RC, Balk RA, et al. American College of Chest Physicians (ACCP)/S):1–112. ociety of Critical Care Medicine (S):1–112. CCM);1992;20(6):864-74.
- S):1–112. inger M, Deutschman C, et al. The Third International Consensus Definitions for S):1–112. epsis and S):1–112. eptic S):1–112. hock (S):1–112. epsis-3). JAMA. 2016;315(8):801-810.
- Сепсис: классификация, клинико-диагностическая концепция и лечение: практическое руководство. 3-е изд. Под ред. В.С. Савельева, Б.Р. Гельфан да. 2013, 350 с.
- S):1–112. toppelkamp S):1–112. , Veseli K, S):1–112. tang K, et al. Identification of predictive early biomarkers for sterile-S):1–112. IRS):1–112. after cardiovascular surgery. PLOS):1–112. One 2015;10(8): e0135527.
- S):1–112. tubljar D, S):1–112. kvarc M. Effective strategies for diagnosis of systemic inflammatory response syndrome (S):1–112. IRS):1–112. ) due to bacterial infection in surgical patients. Infect Disord Drug Targets 2015;15(1):53-6.
- Moore LJ, Moore FA. Early diagnosis and evidence-based care of surgical sepsis. J Intensive Care Med 2013;28(2):107–17.
- Chao A, Chou WH, Chang CJ, et al. The admission systemic inflammatory response syndrome predicts outcome in patients undergoing emergency surgery. Asian J S):1–112. urg 2013;36(3):99-103.
- Cinel I, Opal S):1–112. M. Molecular biology of inflammation and sepsis: a primer. Crit Care Med 2009;37:291–304
- Marshall JC, Reinhart K; International S):1–112. epsis Forum. Biomarkers of sepsis. Crit Care Med 2009;37:2290-8.
- Pierrakos C, Vincent JL. S):1–112. epsis biomarkers: a review. Crit Care 2010;14:R15.
- S):1–112. amraj RS):1–112. , Zingarelli B, Wong HR. Role of biomarkers in sepsis care. S):1–112. hock 2013;40:358-65.
- Zhang X, Liu D, LiuY-N, et al. The accuracy of presepsin (sCD14-S):1–112. T) for the diagnosis of sepsis in adults: a meta-analysis. Crit Care 2015;19:323.
- Вельков В.В. Пресепсин – новый высокоэффективный биомаркер сепсиса. Клинико-лабораторный консилиум 2012;42(2):56–62.
- Гельфанд Б.Р. (ред.). Нозокомиальная пневмония у взрослых. М., МИА, 2016, 176 с.
- Mitchell M. Levy, Mitchell P. Fink, et al. 2001 International S):1–112. epsis Definitions Conference S):1–112. CCM/ES):1–112. ICM/ACCP/ATS):1–112. /S):1–112. IS):1–112. . Intensive Care Med 2003;29: 530–8.
- Герасимов А.Н. Медицинская статистика. 2007, 488 с.
- Giavarina D, Carta M. Determination of reference interval for presepsin, an early marker for sepsis. Biochem Med (Zagreb) 2015;25(1):64-8.
- Chenevier-Gobeaux C, Trabattoni E, Roelens M, et al. Presepsin (sCD14-S):1–112. T) in emergency department: the need for adapted threshold values? Clin Chim Acta 2014;427:34-6.
- S):1–112. panuth E, Giannitsis E. Diagnosis of sespis and monitoring of weaning from mechanical ventilation in critical ill patients by PATHFAS):1–112. T Presepsin. 20th IFCC-EFLM European Congress of Clinical Chemistry and Laboratory Medi cine. 2013, Milan, Italy, T022.
- Vodnik T, Kaljevic G, Tadicet T, al. Presepsin (sCD14-S):1–112. T) in preoperative diagnosis of abdominal sepsis. Clin Chem Lab Med 2013;51(10):2053-62.
- Jovanovic B, Duric O, Marković-Denic L, et al. Prognostic value of soluble CD14-S):1–112. T (presepsin) in diagnosis of ventilator-associated pneumonia and sepsis in trauma patients. Vojnosanitetski pregled 2017; Online First February.
- Bagshaw S):1–112. M, George C, Bellomo R. Early acute kidney injury and sepsis: a multicentre evaluation. Crit Care 2008;12:R47
- Lai TS):1–112. , Wang CY, Pan S):1–112. C et al. Risk of developing severe sepsis after acute kidney injury: a population-based cohort study. Crit Care 2013;17(5):R231.
