Исследование ORAL Strategy – стратегия лечения ревматоидного артрита
Целью рандомизированного клинического исследования ORAL Strategy было сравнение различных стратегий лечения больных средне-тяжелым или тяжелым ревматоидным артритом, не ответивших на терапию метотрексатом: присоединение тофацитиниба или ингибитора фактора некроза опухоли-α или переход на монотерапию тофацитинибом. Две схемы комбинированной терапии не отличались по эффективности и безопасности. Частота ответа на монотерапию была достаточно высокой, но ниже таковой у пациентов, получавших тофацитиниб или адалимумаб в сочетании с метотрексатом. Результаты исследования свидетельствуют о том, что при отсутствии ответа на стандартные базисные противовоспалительные препараты больным активным ревматоидным артритом следует назначать комбинированную терапию тофацитинибом и метотрексатом. Монотерапия тофацитинибом возможна у пациентов, которые не переносят метотрексат или другие базисные противовоспалительные препараты или имеют противопоказания к их применению
Всоответствии с последними рекомендациями Европейский антиревматической лиги (EULAR) и Американской коллегии ревматологов (ACR) пациентам с ревматоидным артритом (РА), не ответившим на монотерапию или комбинированную терапию стандартными базисными противовоспалительными препаратами (БПВП), необходимо назначить генноинженерный биологический препарат (ГИБП), такой как ингибитор фактора некроза опухоли-α (ФНО), или таргетный БПВП [1,2]. К последней группе относятся ингибиторы янус-киназ – низкомолекулярные синтетические препараты, предназначенные для приема внутрь и оказывающие селективное действие на внутриклеточную сигнальную систему JAK/STAT, которая опосредует действие многих цитокинов, участвующих в патогенезе РА [3-6]. В России единственным зарегистрированным препаратом этой группы является тофацитиниб (Яквинус). Эффективность и безопасность тофацитиниба в дозе 5 мг и 10 мг два раза в день в виде монотерапии или в комбинации со стандартными БПВП, прежде всего метотрексатом, у больных активным РА установлены в нескольких плацебоконтролируемых исследованиях 3 фазы и длительных наблюдательных исследования (до 105 мес) [7]. В двух исследованиях была сопоставлена эффективность тофацитиниба и ингибитора ФНО-α адалимумаба у больных РА, однако оба этих исследования имели определенные ограничения, что не позволило сделать окончательные выводы [8,9]. Недавно были опубликованы результаты рандомизированного контролируемого исследования 3b/4 фазы (Oral Rheumatoid Arthritis triaL [ORAL] Strategy), которое предполагало прямое сравнение трех стратегий лечения у больных РА, не ответивших на метотрексат, – монотерапии тофацитинибом или комбинированной терапии тофацитинибом с метотрексатом или адалимумабом с метотрексатом [10].
Дизайн исследования
ORAL Strategy было 12-месячным, двойным слепым, прямым сравнительным исследованием, которое проводилось в 194 центрах в 25 странах, включая Россию. Целью исследования было доказать, что монотерапия тофацитинибом в дозе 5 мг два раза в день или комбинированная терапия тофацитинибом внутрь в дозе 5 мг два раза в сутки и метотрексатом по эффективности не уступает (non-inferiority) комбинированной терапии адалимумабом в дозе 40 мг подкожно каждые 2 недели и метотрексатом у больных активным ревматоидным артритом (счет болезненных или опухших суставов по крайней мере 4 и концентрация высокочувствительного С-реактивного белка >3 мг/л). Критерием включения было также отсутствие ответа на лечение метотрексатом в дозе 15-25 мг/нед в течение по крайней 4 мес (в стабильной дозе в течение по крайней мере 6 последних недель). Пациентов рандомизировали на три равные группы и назначали монотерапию тофацитинибом или добавляли тофацитиниб или адалимумаб к метотрексату в прежней дозе. Чтобы обеспечить слепую маскировку, использовали тройное плацебо.
Первичной конечной точкой исследования была частота ответа по критериям Американской коллегии ревматологов (АКР) 50 через 6 мес у всех рандомизированных пациентов. Кроме того, оценивали частоту ответа по критериям АКР20 и АКР70, частоту достижения низкой активности и ремиссии РА, динамику качества жизни (короткая форма [SF] 36, EuroQol) и усталости, а также ряд других вторичных конечных точек через 6 мес и в другие сроки исследования. Критериями ремиссии служили значения SDAI ≤3,3, CDAI ≤2,8, DAS28-4[СОЭ] <2,6, DAS28-4[CРБ] <2,6 и критерии ACR–EULAR Boolean.
Результаты
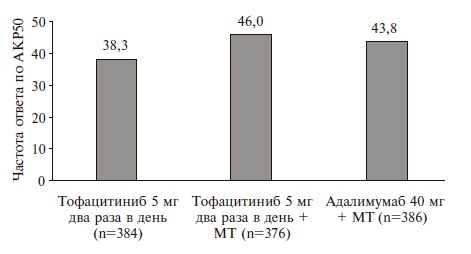
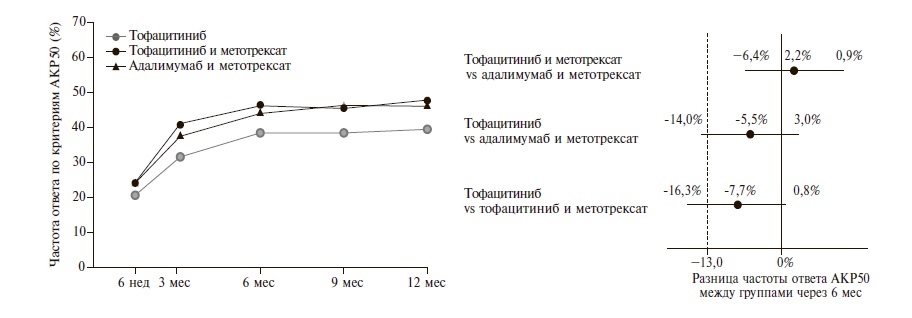
Характеристика больных. В исследование были включены 1146 больных; 384 из них получали монотерапию тофацитинибом, 376 – тофацитиниб в сочетании с метотрексатом и 386 – адалимумаб в сочетании с метотрексатом. По демографическим и исходным клиническим показателям, в том числе активности и тяжести РА, три группы были сопоставимыми (табл. 1). Эффективность. Во всей выборке через 6 мес ответ по критериям АКР50 был достигнут у 38% больных, получавших монотерапию тофацитибином, 46% пациентов, получавших тофацитиниб и метотрексат, и 44% больных, получавших адалимумаб и метотрексат (рис. 1,2). Комбинированная терапия тофацитинибом и метотрексатом по эффективности не уступала комбинации ингибитора ФНО-α и метотрексата: разница частоты ответа по критериям АКР50 между группами составила 2% (98,34% доверительный интервал [ДИ] от -6 до 11), а нижняя граница указанного ДИ находилась выше точки, предусмотренной протоколом (-13%). В то же время сопоставимая эффективность монотерапии тофацитинибом по сравнению с комбинацией тофацитиниба и метотрексата (разница между группами -8%; 98,34% ДИ от -16 до 1) или адалимумаба и метотрексата (разница -6%; 98,34% ДИ от -14 до 3) на основании приведенного выше критерия не была подтверждена. Сходные результаты были получены в выборке пациентов, выполнивших протокол. В этой выборке частота ответа по критерия АКР50 у больных, получавших только тофацитиниб или комбинированную терапию тофацитинибом и метотрексатом или адалимумабом и метотрексатом, составила 41%, 51% и 47%, соответственно.
| Тофацитиниб (n=384) | Тофацитиниб + метотрексат (n=376) | Адалимумаб + метотрексат (n=386) | |
|---|---|---|---|
| Примечание: АЦПП - антитела к цитруллинированному пептиду, вчСРБ - высокочувствительный С-реактивный белок | |||
| Женщины | 319 (83%) | 311 (83%) | 320 (83%) |
| Возраст, лет | 49,7±12,2 | 50,0±13,4 | 50,7±13,4 |
| Длительность РА, лет | 6,1 (0,2–41,6 | 5,4 (0,0–43,5) | 6,0 (0,3–42,8 |
| Предыдущая терапия | |||
| Стандартный БПВП (помимо метотрексата) | 122 (32%) | 115 (31%) | 142 (37%) |
| ГИБП (исключая ингибиторы ФНО) | 17 (4%) | 14 (4%) | 20 (5%) |
| Ингибитор ФНО | 28 (7%) | 16 (4%) | 19 (5%) |
| Доза метотрексата, мг/нд | 0 | 16,7±3,7 | 16,4±3,7 |
| Глюкокортикостероиды исходно | 223 (58%) | 214 (57%) | 218 (57%) |
| Суточная доза глюкокортикостероидов, мг | 7,3±13,3 | 6,5±2,5 | 6,5±2,6 |
| Счет болезненных суставов (28) | 15,4±6,5 | 15,6±6,5 | 15,2±6,7 |
| Счет опухших суставов (28) | 11,2±5,6 | 11,8±5,7 | 11,0±5,4 |
| Общая оценка активности пациентом | 60,1±21,4 | 61,7±22,0 | 60,2±23,5 |
| Общая оценки активности врачом | 59,7±17,7 | 60,7±18,0 | 60,3±19,6 |
| Боль по визуальной аналоговой шкале | 61,2±21,7 | 60,7±22,4 | 60,6±22,6 |
| DAS28-4(СОЭ) | 6,5±0,9 | 6,6±0,9 | 6,5±1,0 |
| DAS28-4(CРБ) | 5,7±0,9 | 5,8±0,9 | 5,7±1,0 |
| SDAI | 40,2±13,0 | 41,6±13,2 | 39,8±13,3 |
| CDAI | 38,6±12,6 | 39,7±12,7 | 38,2±12,9 |
| HAQ-DI | 1,6±0,6 | 1,6±0,6 | 1,6±0,6 |
| вчСРБ, мг/дл | 16,6±19,3 | 18,7±21,9 | 16,7±21,3 |
| АЦПП | 291 (76%) | 282 (75%) | 299 (78%) |
Через 12 мес частота ответа по критериям АКР50 в выборке intention-to-treat существенно не изменилась и составила 39% в группе тофацитиниба, 48% в группе тофацитиниба и метотрексата и 46% в группе адалимумаба и метотрексата. В конце исследования частота ответа по критериям АКР20, АКР50 и АКР70 в группах больных, получавших комбинированную терапию, была сопоставимой и превышала таковую у пациентов, которым проводили монотерапию тофацитинибом (табл. 2).
| Тофацитиниб (n=384) | Тофацитиниб + МТ (n=376) | Адалимумаб + МТ (n=386) | |
|---|---|---|---|
| Примечание: МТ - метотрексат | |||
| АКР20 | |||
| 6 мес | 249 (65%) | 275 (73%) | 274 (71%) |
| 12 мес | 237 (62%) | 264 (70%) | 261 (68%) |
| АКР50 | |||
| 6 мес | 147 (38%) | 173 (46%) | 169 (44%) |
| 12 мес | 151 (39%) | 179 (48%) | 177 (46%) |
| АКР70 | |||
| 6 мес | 70 (18%) | 94 (25%) | 80 (21%) |
| 12 мес | 81 (21%) | 109 (29%) | 100 (26%) |
| Низкая активность РА | |||
| SDAI (≤11) | |||
| 6 мес | 167 (43%) | 187 (50%) | 182 (47%) |
| 12 мес | 169 (44%) | 187 (50%) | 204 (53%) |
| CDAI (≤10) | |||
| 6 мес | 163 (42%) | 183 (49%) | 179 (46%) |
| 12 мес | 173 (45%) | 188 (50%) | 202 (52%) |
| DAS28-4(СОЭ) (<3,2) | |||
| 6 мес | 79 (21%) | 100 (27%) | 106 (27%) |
| 12 мес | 87 (23%) | 102 (27%) | 128 (33%) |
| DAS28-4(CРБ) (<3,2) | |||
| 6 мес | 159 (41%) | 174 (46%) | 181 (47%) |
| 12 мес | 157 (41%) | 175 (47%) | 201 (52%) |
| Ремиссия РА | |||
| SDAI (≤3,3) | |||
| 6 мес | 38 (10%) | 50 (13%) | 50 (13%) |
| 12 мес | 53 (14%) | 61 (16%) | 62 (16%) |
| CDAI (≤2,8) | |||
| 6 мес | 39 (10%) | 52 (14%) | 51 (13%) |
| 12 мес | 54 (14%) | 70 (19% | 65 (17%) |
| DAS28-4(СОЭ) (<2,6) | |||
| 6 мес | 40 (10%) | 45 (12%) | 48 (12%) |
| 12 мес | 43 (11%) | 55 (15% | 66 (17%) |
| DAS28-4(СРБ) (<2,6) | |||
| 6 мес | 81 (21%) | 115 (31%) | 108 (28%) |
| 12 мес | 92 (24%) | 114 (30%) | 136 (35%) |
| ACR–EULAR | |||
| 6 мес | 27 (7%) | 31 (8%) | 34 (9%) |
| 12 мес | 37 (10% | 49 (13%) | 47 (12%) |
Результаты анализа различных вторичных конечных точек эффективности были сходными с таковыми первичного анализа. Например, доля пациентов достигших низкой активности, которую оценивали на основании SDAI (≤11), через 6 мес не отличалась среди больных, получавших комбинированную терапию тофацитинибом и метотрексатом (50%) или адалимумабом и мето трексатом (47%), и превышала таковую в группе тофацитиниба (43%). Похожие результаты были получены при анализе частоты достижения низкой активности РА, которую оценивали на основании CDAI, DAS28-4 (СОЭ) и DAS28-4(СРБ).
Частота достижения ремиссии РА через 6 мес (SDAI≤3,3) была одинаковой при комбинированной терапии тофацитинибом или адалимумабом с метотрексатом (13% и 13%, соответственно) и несколько ниже при монотерапии тофацитинибом (10%). При использовании других критериев ремиссии РА были получены такие же сходные результаты как через 6 мес, так и 12 мес. Динамика средних значений SDAI, CDAI, DAS284(СОЭ) и DAS28-4(СРБ) через 6 и 12 мес также была более выраженной в обеих группах больных, которым проводилась комбинированная терапия.
Безопасность. Хотя частота серьезных нежелательных явлений (НЯ) была несколько выше в обеих группах пациентов, получавших тофацитиниб, тем не менее, частота прекращения лечения из-за НЯ оказалась выше в группе адалимумаба и метотрексата (табл. 3). Какихлибо новых или неожидаемых НЯ ни в одной группе не зарегистрировали. Большинство НЯ были легкими или средне-тяжелыми, а наиболее распространенные НЯ во всех трех группах включали в себя инфекции верхних дыхательных путей (7-10%), повышение активности АЛТ (2-7%), назофарингит (4-6%), инфекции мочевых путей (3-4%) и тошноту (3-4%). Опоясывающий герпес в целом развился у 18 (2%) больных, в том числе у 4, 8 и 6 пациентов, получавших только тофацитиниб, тофацитиниб и метотрексат или адалимумаб и мето трексат, соответственно. Среди 216 пациентов, иммунизированных вакциной против герпеса, развитие этой инфекции наблюдали в 3 (1%) случаях, а среди 930 невакцинированных больных – в 15 (2%) случаях.
Небольшое увеличение средних уровней общего холестерина, липопротеинов низкой и высокой плотности, сывороточного креатинина, гемоглобина, активности аминотрансфераз и содержания билирубина и снижение абсолютного числа нейтрофилов было выявлено во всех трех группах пациентов.
Обсуждение
Исследование ORAL Strategy было призвано ответить на вопрос, какую стратегию терапии следует выбрать, если пациент с активным РА не отвечает на лечение метотрексатом или другими стандартными БПВП: добавить к метотрексату тофацитиниб или ингибитор ФНО-α, такой как адалимумаб, или перевести больного на монотерапию тофацитинибом. Соответственно, пациенты, включенные в исследование, были распределены на три равные группы и получали только тофацитиниб или комбинированную терапию тофацитинибом или адалимумабом с метотрексатом. Примерно 60% пациентов исходно принимали глюкокортикостероиды в низкой дозе. Одна первичная конечная точка исследования была достигнута – через 6 мес частота ответа по критериям АКР50 была сопоставимой в двух группах больных, которым проводилась комбинированная терапия. Это свидетельствовало о том, что при присоединении к метотрексату тофацитиниба или ингибитора ФНО-α адалимумаба можно ожидать сходных результатов лечения.
В определенной степени эти результаты были ожидаемыми. В ранее опубликованном рандомизированном контролируемом исследовании ORAL Standard, в котором сравнивали эффективность и безопасность тофацитиниба и плацебо у больных РА, не ответивших на метотрексат в стабильной дозе, была выделена группа пациентов, получавших адалимумаб [11]. Пациенты всех трех групп продолжали прием метотрексата в прежней дозе. По частоте ответа по критериям АКР20 через 6 мес (первичная конечная точка) схемы комбинированной терапии тофацитинибом или адалимумабом с метотрексатом достоверно не отличались (52% и 47%, соответственно). Частота ответа по критериям АКР50 при лечении тофацитинибом с метотрексатом была выше (37%), чем при комбинированной терапии адалимумабом и метотрексатом (28%), однако разница не достигла статистической значимости. Необходи мость в дополнительном сравнительном анализе комбинированной терапии тофацитинибом или ингибитором ФНО-α была связана с тем, что дизайн исследования ORAL Standard не предполагал подтверждение сходной эффективности тофацитиниба и адалимумаба.
Второй целью исследования ORAL Strategy было показать сопоставимую эффективность (non-inferiority) монотерапии тофацитинибом и комбинированной терапии препаратами сравнения и метотрексатом. Эта конечная точка не была достигнута. Как по первичному, так и различным вторичным показателям эффективности, которые оценивали через 6 и 12 мес, монотерапия ингибитором янус-киназ уступала комбинированной терапии как тофацитинибом и метотрексатом, так и адалимумабом и метотрексатом. Тем не менее, полученные данные не указывают на неэффективность монотерапии тофацитинибом. Дизайн исследования не предполагал подтверждение более высокой эффективности той или иной схемы лечения, поэтому полученные данные не позволяют сделать вывод о том, что комбинированная терапия превосходила монотерапию.
Результаты применения ингибитора янус-киназ в исследовании ORAL Strategy были сходными с результатами плацебо-контролируемого исследования ORAL Solo, в котором изучалась эффективность монотерапии тофацитинибом у 611 пациентов с РА, прекративших лечение по крайней мере одним БПВП и ГИБП из-за недостаточного ответа или плохой переносимости [12]. Большинство пациентов до включения в это исследование получали метотрексат (более 80%) или другие БПВП, в то время как опыт применения ГИБП имелся примерно у одной пятой больных. Пациенты двух основных групп на протяжении всего исследования получали тофацитиниб в дозах 5 или 10 мг два раза в день, в то время как у пациентов двух групп сравнения в течение первых 3 месяцев применяли плацебо, после чего их переводили на тофацитиниб в дозах 5 или 10 мг два раза в сутки. Соответственно, первичные показатели эффективности оценивали через 3 месяца после начала лечения. Монотерапия тофацитинибом в обеих дозах по эффективности достоверно превосходила плацебо, а после перевода пациентов контрольной группы на лечение ингибитором янус-киназ наблюдалось быстрое увеличение частоты ответа на терапию. В группе пациентов, получавших тофацитиниб в дозе 5 мг два раза в день, через 3 мес частота ответа по критериям АКР20, АКР50 и АКР70 составила 59,8%, 31,1% и 15,4%. Эти показатели более чем в два раза превышали таковые в группе плацебо (p<0,001 во всех случаях) и соответствовали результатам монотерапии тофацитинибом в исследовании ORAL Strategy (рис. 3).
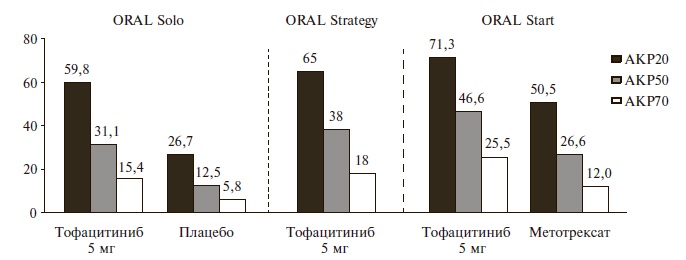
Еще одним исследованием, в котором пациенты с РА получали монотерапию тофацитинибом, было ORAL Start [13]. В отличие от предыдущих исследований, в нем изучали эффективность терапии первой линии, а тофацитиниб сравнивали с метотрексатом у 958 больных РА, не получавших ранее метотрексат или не принимавших его в терапевтических дозах. В этом исследовании частота ответа на лечение тофацитинибом через 6 мес была несколько выше, чем в исследованиях ORAL Strategy и ORAL Solo, что отражало особенности выборки – пациенты с ранним РА, не получавшие ранее БПВП или принимавшие их в низких дозах. Основным результатом исследования ORAL Start было достоверное превосходство тофацитиниба над метотрексатом по эффективности. Например, через 6 мес частота ответа по критериям АКР70 при лечении тофацитинибом в дозе 5 мг два раза в день (25,5%) была в два раза выше, чем в группе метотрексата (12,0%; p<0,001), а достигнутое преимущество сохранялось в течение 2 лет. Сходные различия были выявлены и при анализе частоты достижения ремиссии и низкой активности РА, которые оценивали с помощью счета DAS28. Оба препарата задерживали прогрессирование деструктивных изменений суставов, в пользу чего свидетельствовали небольшие изменения модифицированного счета Шарпа, который через 2 года в группах тофацитиниба увеличился в меньшей степени, чем в группе метотрексата. При этом доля больных, у которых отсутствовало прогрессирование структурных изменений (увеличение общего счета Шарпа ≤0,5), при лечении тофацитинибом была достоверно выше, чем при применении метотрексата. Нельзя исключить, что эффективность метотрексата в исследовании ORAL Start была несколько заниженной, так как дозу его увеличивали максимум до 20 мг/нед, в то время как сегодня допускается увеличение дозы этого препарата до 25-30 мг/нед. Следует также подчеркнуть, что применение тофацитиниба для терапии первой линии у больных РА не зарегистрировано, поэтому результаты исследования ORAL Start приведены только для иллюстрации возможной эффективности монотерапии тофацитинибом.
По переносимости и безопасности, в том числе частоте серьезных НЯ и прекращения лечения из-за НЯ, в исследовании ORAL Strategy сравниваемые схемы существенно не отличались. В предыдущих исследованиях было показано, что лечение тофацитинибом может сопровождаться увеличением риска развития опоясывающего герпеса [14]. В исследовании ORAL Strategy частота герпеса была низкой и сходной при монотерапии тофацитинибом (4/384) и комбинированной терапии адалимумабом и метотрексатом (6/386) и недостоверно выше в группе тофацитиниба и метотрек сата (8/376). Таким образом, применение последнего может способствовать развитию герпетической инфекции у пациентов, получающих тофацитиниб. Частота опоясывающего герпеса у пациентов, иммунизированных и не иммунизированных живой вакциной против герпеса, оказалась практически одинаковой (1% и 2%, соответственно). Необходимо однако учитывать, что протокол исследования не предполагал изучение эффективности вакцины, а решение о вакцинации принимали сами исследователи по своему усмотрению.
Заключение
В исследовании ORAL Strategy у больных активным РА, не ответивших на метотрексат, комбинированная терапия тофацитинибом в дозе 5 мг два раза в день и метотрексатом по эффективности и безопасности не отличалась от терапии адалимумабом и метотрексатом. Монотерапия тофацитинибом по эффективности уступала обеим схемам комбинированной терапии, хотя результаты применения одного ингибитора янус-киназ были сопоставимыми с таковыми в рандомизированных клинических исследованиях, подтвердивших более высокую эффективность монотерапии тофацитинибом по сравнению с плацебо или метотрексатом. Полученные данные свидетельствуют о том, что тофацитиниб может применяться у больных тяжелым и среднетяжелым РА, не отвечающих на метотрексат или другие стандартные БПВП, наравне с ингибиторами ФНО-α. Тофацитиниб следует назначать в комбинации с метотрексатом, однако монотерапия тофацитинибом возможна, если пациент не переносит метотрексат и другие стандартные БПВП или имеет противопоказания к их применению.
Используемые источники
- Singh JA, Saag KG, Bridges SL Jr, et al. 2015 American College of Rheumatology guideline for the treatment of rheumatoid arthritis. Arthritis Care Res (Hoboken) 2016;68:1–25.
- Smolen JS, Landew éR, Bijlsma J, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2016 update. Ann Rheum Dis 2017;76:960–77.
- Banerjee S, Biehl A, Gadina M, et al. JAK-STAT signaling as a target for inflammatory and autoimmune diseases: current and future prospects. Drugs 2017;77(5):521-46.
- Каратеев Д.Е. Новое направление в патогенетической терапии ревматоидного артрита: первый ингибитор Янус-киназ тофацитиниб. Современная ревматология 2014;1:39-44.
- Насонов Е.Л. Новые подходы к фармакотерапии ревматоидного артрита: тофацитиниб. Научно-практическая ревматология 2014;52(2):209–21.
- Новиков П.И., Моисеев С.В. Тофацитиниб – первый пероральный ингибитор янус-киназ в лечении ревматоидного артрита. Клин фармакол тер 2015;24 (5):
- Новиков П.И., Моисеев С.В. Ингибиторы янус-киназ в лечении рев матоид ного артрита. Клин фармакол тер 2017;26(4).
- van Vollenhoven RF, Fleischmann R, Cohen S, et al. Tofacitinib or adalimumab versus placebo in rheumatoid arthritis. N Engl J Med 2012;367:508–19.
- Fleischmann R, Cutolo M, Genovese MC, et al. Phase IIb dose-ranging study of the oral JAK inhibitor tofacitinib (CP-690,550) or adalimumab monotherapy versus placebo in patients with active rheumatoid arthritis with an inadequate response to disease-modifying antirheumatic drugs. Arthritis Rheum 2012; 64:617–29.
- Fleischmann R, Mysler E, Hall S, et al. Efficacy and safety of tofacitinib monotherapy, tofacitinib with methotrexate, and adalimumab with methotrexate in patients with rheumatoid arthritis (ORAL Strategy): a phase 3b/4, doubleblind, head-to-head, randomised controlled trial. Lancet 2017;390(10093):457-68.
- van Vollenhoven RF, Fleischmann R, Cohen S, Lee EB, Garc ía Meijide JA, Wagner S, et al; ORAL Standard Investigators. Tofacitinib or adalimumab versus placebo in rheumatoid arthritis. N Engl J Med 2012;367(6):508-19.
- Fleischmann R, Kremer J, Cush J, Schulze-Koops H, Connell CA, Bradley JD, et al; ORAL Solo Investigators. Placebo-controlled trial of tofacitinib monotherapy in rheumatoid arthritis. N Engl J Med 2012;367(6):495-507.
- Lee EB, Fleischmann R, Hall S, Wilkinson B, et al; ORAL Start Investigators. Tofacitinib versus methotrexate in rheumatoid arthritis. N Engl J Med 2014;370(25):2377-86.
- Curtis JR, Xie F, Yun H, et al. Real-world comparative risks of herpes virus infections in tofacitinib and biologic-treated patients with rheumatoid arthritis. Ann Rheum Dis 2016;75:1843–47.
