Эффективность и безопасность терапии инфликсимабом у больных ревматоидным артритом в реальной клинической практике
Оценка результатов лечения инфликсимабом (ИНФ) у больных ревматоидным артритом (РА) в реальной клинической практике.
Обобщен опыт применения ИНФ у 23 пациентов с достоверным диагнозом РА. Основным показанием к лечению ИНФ в комбинации с метотрексатом в дозе 15 мг/нед было отсутствие ответа на предшествующую базисную терапию. Эффективность ИНФ оценивали на основании динамики индекса DAS28, числа болезненных суставов (ЧБС), числа припухших суставов (ЧПС), СОЭ, уровней С-реактивного белка (СРБ) и ревматоидного фактора (РФ).
Лечение ИФН привело к достоверному снижению среднего индекса DAS28, ЧБС и ЧПС, а также лабораторных показателей активности РА. Через 48 недель сроку ремиссия РА (DAS28<2,6) была достигнута у 2 (9,1%) из 22 больных, продолжавших лечение, а низкая степень активности – у 6 (27,3%). У большинства пациентов после второй инфузии препараты были купированы системные внесуставные проявления РА, в том числе экссудативный плеврит, ревматоидный васкулит и полинейропатия. У пациентов с ранним и поздним РА динамика индекса DAS28 была в целом сопоставимой, однако более выраженное снижение показателя было отмечено при раннем РА. У одной пациентки после первой инфузии ИФН развился венозный тромбоз голени, в связи с чем препарат был отменен. У остальных пациентов переносимость ИФН была хорошей.
Полученные данные свидетельствует об эффективности ИНФ в комбинации с метотрексатом в дозе 15 мг/нед у больных со средне-тяжелым и тяжелым течение РА в реальной клинической практике.
Ревматоидный артрит (РА) – хроническое системное аутоиммунное воспалительное заболевание с преимущественным поражением суставов в виде эрозивного артрита. Распространенность и заболеваемость РА в России в 2012-2013 гг. имели тенденцию к росту, особенно в Приволжском федеральном округе [1,2]. Однако в Пензенской области в 2013-2014 гг. было отмечено снижение распространенности РА со 194,1 до 148,9 на 100000 населения. Современная концепция лечения РА (Treat to Target – “лечение до достижения цели”) предполагает раннее назначение базисных противовоспалительных препаратов, достижение ремиссии или низкой активности РА и постоянную базисную терапию. Лечение РА представляет сложную задачу. У части пациентов наблюдаются тяжелое течение заболевания и неуклонное его прогрессирование, поэтому они нуждаются в комбинированной терапии стандартными базисными противовоспалительными препаратами и генно-инженерными биологическими препаратами (ГИБП) [3,4], которые оказывают селективное ингибирующее действие на отдельные противовоспалительные цитокины [5,6]. В многочисленных рандомизированных контролируемых исследованиях доказано, что применение ГИБП позволяет снизить активность иммунопатологического процесса и добиться клинического эффекта и длительной ремиссии [710]. Анализ применения ГИБП в России, выполненный в НИИ ревматологии имени В.А. Насоновой, показал, что в реальной клинической практике ГИБП получали лишь 2,8% больных РА. Среди них чаще всего использовали инфликсимаб (ИНФ) и ритуксимаб, что отражает возможность назначения этих препаратов по программе льготного обеспечения инвалидов из федерального бюджета [1,11]. В течение последних 2 лет в Пензенской областной клинической больнице им. Н.Н. Бурденко пациенты получают ГИБП в специализированном кабинете в рамках оказания высокотехнологичных видов медицинской помощи [12].
Изучение ИНФ в России началось в 2001 г. Он был первым ГИБП, зарегистрированным в нашей стране для лечения больных РА. Эффективность ИНФ, который представляет собой моноклональное химерное антитело к фактору некроза опухоли-α (ФНО-α), при РА и других ревматических заболеваниях в настоящее хорошо изучена [13,14]. ФНО-α – это один наиболее важных цитокинов, играющих роль в патогенезе РА и других воспалительных заболеваний опорно-двигательного аппарата. Показано, что помимо непосредственной блокады ФНО-α, ИНФ способен снижать содержание интерлейкина-6 у больных РА [15]. В современных рекомендациях указано, что ГИБП при РА назначают при неадекватном ответе на базисную противоспалительную терапию по крайней мере двумя препаратами (одним из которых должен быть метотрексат) в течение 6 месяцев. Недостаточным ответом считают отсутствие улучшения по критериями Амери канской коллегии ревматологов (АКР) по крайней мере на 50% или сохранение умеренной активности РА, оцениваемой по DAS28 (3,2-5,1), появление более двух новых эрозий в течение 12 месяцев даже при снижении активности заболевания до низкой, нарастание титров ревматоидного фактора (РФ) и антител к цитрулли нированным пептидам [16,17]. В многочисленных рандомизированных контролируемых исследованиях показана высокая эффективность ИНФ у больных с длительным течением РА [18-23].
Целью исследования была оценка результатов лечения ИНФ больных с РА, получавших препарат в реальной клинической практике.
Материал и методы
Нами обобщен опыт применения ИНФ у 23 пациентов с достоверным диагнозом РА. Среди больных преобладали женщины среднего возраста с большой продолжительностью болезни и высокой активностью воспалительного процесса (табл. 1). РФ определялся у 16 больных, а АЦПП – у 12. Средний титр последнего составил 56,7 ед. Ранний РА (от 6 мес до 6 лет) диагностировали у 8 пациентов, развернутый – у 5, поздний (более 5 лет) – у 10. У 15 и 8 пациентов выявили II и III рентгенологическую стадию заболевания, соответственно. У 11 пациентов с РА имелись системные проявления, в том числе плеврит (3), ревматоидный васкулит (5), полинейропатия (3).
| Показатели | Значения |
|---|---|
| Женщины, n (%) | 17 (73,9) |
| Средний возраст, лет | 45,8±5,7 |
| РФ, n (%) | 17 (73,9) |
| АЦЦП, n (%) | 12 (52,2) |
| ЧПС (18) | 8,8±1,4 |
| ЧБС (28 | 18,5±3,7 |
| СОЭ мм/ч | 44,2±8,5 |
| DAS28, ед | 6,1±1,4 |
| Давность РА, лет | 5,2±4,2 |
| Лечение, n (%) | |
| НПВП | 23 (100) |
| Глюкокортикостероиды | 16 (69,6) |
| Метотрексат | 16 (69,6) |
| Лефлюномид | 3 (13,0) |
| Сульфасалазин | 2 (8,7) |
| Аминохинолиновые | 2 (8,7) |
Основным показанием для назначения ГИБП была недостаточная эффективность предшествующей базисной терапии. До начала терапии ИНФ пациенты получали традиционные базисные препараты, прежде всего метотрексат, а также нестероидные противовоспалительные препараты (НПВП) и глюкокортикостероиды (табл. 1). Всем пациентам ИНФ вводили по классической схеме в дозе 3 мг/кг в сочетании с метотрексатом 15 мг/нед в течение 96 недель. Перед началом лечения проводили общий анализ крови, рентгенографию органов грудной клетки, кистей и стоп, пробу Манту, определяли маркеры вирусов гепатита В и С, РФ, АЦЦП и С-реактивный белок (СРБ) в сыворотке крови. Для оценки эффективности терапии определяли динамику индекса DAS28, числа болезненных суставов (ЧБС) и припухших суставов (ЧПС), СОЭ, СРБ и РФ через 12, 24 и 48 недель.
При обработке результатов исследования использовали программу Statistica 6,0 (StatSolf Inc., США). Результаты представлены в виде M±SD при нормальном распределении. Для анализа применяли параметрический критерий t Cтьюдента. За статистическую достоверность различий принимали значение p<0,05. При ненормальном распределении значения представляли в виде медианы – Me (Q25%; Q75%), а для проверки нулевой гипотезы использовали непараметрический ранговый критерий Вилкоксона.
Результаты
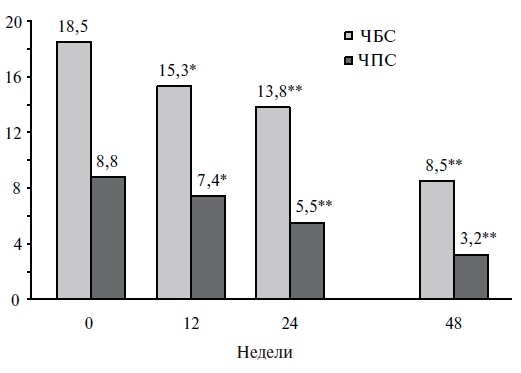
У одной пациентки ИНФ был отменен после первой инфузии, поэтому результаты лечения анализировали у 22 пациентов. Достоверное снижение среднего индекса DAS28 было отмечено, начиная с 12-й недели лечения (p<0,05) (рис. 1), а через 48 недель он снизился в среднем с 6,1 до 4,6 (p<0,01). К этому сроку ремиссия РА (DAS28<2,6) была достигнута у 2 (9,1%) из 22 больных, продолжавших лечение, низкая степень активности (средние значения DAS28 – 3,0, ЧБС – 2, ЧПС – 0, СОЭ – 12 мм/ч, ВАШ по оценке пациента – 40 мм) – у 6 (27,3,0%), средняя степень активности (средние значения DAS28 – 4,4, ЧБС – 4, ЧПС – 1, СОЭ – 27 мм/ч, ВАШ по оценке пациента – 50 мм) – у 14 (63,6%). У 2 (9,1%) больных сохранялась высокая активность РА (DAS28 – 5,1, ЧБС – 6, ЧПС – 2, СОЭ – 35 мм/ч, ВАШ по оценке пациента – 60 мм). Лечение ИНФ привело к достоверному уменьшению ЧБС и ЧПС (p<0,05; рис. 2), а также утренней скованности. Интенсивность боли при ходьбе, которую оценивали сами пациенты и врачи по визуальной аналоговой шкале, через 24 недели снизилась с 63 до 43 мм и с 55 до 32 мм, соответственно. У большинства пациентов после второй инфузии препараты были купированы системные внесуставные проявления РА, в том числе экссудативный плеврит (у всех 3), ревматоидный васкулит (у 4 из 5) и полинейропатия (у 2 из 3). Макси мальный клинический эффект был достигнут после шестой инфузии.

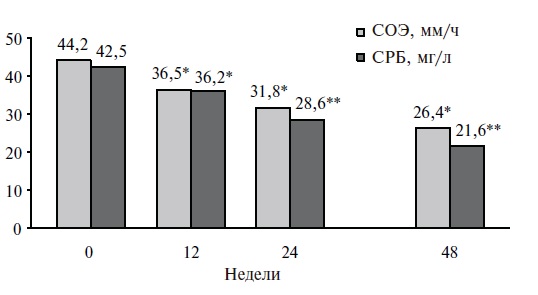
Динамика лабораторных показателей на фоне терапии ИНФ приведена на рис. 3. В результате 48-недельного лечения СОЭ уменьшилась с 44,2 до 26,4 мм/ч (p< 0,05), уровень СРБ – с 42,5 до 21,6 мг/л (p<0,05), РФ – со 120 до 103 ед/л (p<0,05).
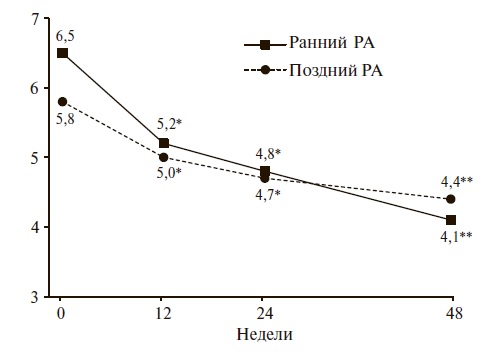
Мы сопоставили эффективность ИНФ у 8 пациентов с ранним РА (длительность болезни от 6 мес до 2 лет) и 10 больных поздним РА (от 5 до 8 лет). У подавляющего большинства больных имелась высокая активность заболевания, причем у пациентов с ранним РА средний индекс DAS28 был недостоверно выше, чем у больных поздним РА (рис. 4). Динамика индекса DAS28 была сопоставимой в двух группах. В среднем он достоверно снизился через 12 недель и продолжал прогрессивно снижаться на фоне терапии. Через 48 недель у пациентов с ранним РА индекс DAS28 снизился в большей степени, чем у больных поздним РА (на 36,9% и 24,1%, соответственно).
У одной пациентки после первой инфузии ИФН развился венозный тромбоз голени, в связи с чем препарат был отменен. У остальных пациентов переносимость ИНФ была хорошей. Только у 2 больных отмечалась умеренная тахикардия. Инфекционных осложнений и случаев туберкулеза не зарегистрировали.
Обсуждение
Терапия стандартными базисными противовоспалительными препаратами, в частности метотрексатом в дозе 15-20 мг/нед и выше, не позволяет достичь низкой активности или ремиссии почти у 50% больных РА [20,21]. В нашем исследовании, проводившемся в обычной клинической практике, 48-недельная терапия ИНФ в стандартной дозе 3 мг/кг в комбинации с метотрексатом в дозе 15 мг/нед у больных РА, не ответивших на стандартную терапию, привела к достоверному снижению среднего индекса DAS28 на 24,6%. Ремиссия или низкая активность РА были достигнуты примерно у трети больных, в то время как более чем у половины больных сохранялась средняя степень активности РА, а в отдельных случаях – и высокая активность заболе вания. Недостаточная эффективность ИФН ассоции ровалась с большей длительностью заболевания, серонегативностью, более высокой рентгенологической стадией и лечением глюкокортикостероидами, в то время как достижение низкой степени активности РА при лечении ИНФ ассоциировалось с серопозитивностью, более молодым возрастом, меньшей длительностью заболевания, лечением метотрексатом, наличием системных проявлений.
ЧБС и ЧПС медленно снижались при лечении ИФН. Значительного снижения обоих показателей (более чем в 2,5 раза) удалось достичь через 48 недель терапии. Снижение лабораторных показателей активности РА также было отмечено уже через 12 недель, однако в последующем они уменьшались очень медленно, особенно СОЭ.
Заключение
Таким образом, опыт применения ИНФ в комбинации с метотрексатом в дозе 15 мг/нед свидетельствует о высокой эффективности комбинированной терапии у больных со средне-тяжелым и тяжелым течением РА, не ответивших на стандартные базисные противовоспалительные препараты. У пациентов с ранним РА лечение ИНФ приводило к несколько более выраженному снижению активности заболевания, чем у больных с поздним РА. Переносимость препарата была хорошей.
Используемые источники
- Насонов Е.Л. Лечение ревматоидного артрита: современное состояние про- блемы. РМЖ 2006;8(14):573-7.
- Балабанова Р.М., Эрдес Ш.Ф. Распространенность ревматических заболева- ний в России в 2012-2013 гг. Научно-практическая ревматология 2015;53(2): 120-4.
- Насонов Е.Л. фармакотерапия ревматоидного артрита в эру генно-инже- нерных биологических препаратов. Терапевтический архив 2007;79(5):1-9.
- Насонов Е.Л., Денисов Л.Н., Станислав М.Л, Ильина А.Е. Перспективы фармакотерапии ревматоидного артрита: моноклональные антитела. Научно-практическая ревматология 2012;3:75-82.
- Сигидин Я.А, Лукина Г.В. Биологическая терапия в ревматологии. Москва: Практическая медицина; 2007, 303.
- Haque UJ, Bathom JM. The role of biological in early rheumatoid arthritis. Best Pract Res Clin Rheumatol 2005;19(1):179-89.
- Насонов Е.Л. Применение ритуксимаба при ревматоидном артрите с пози- ций медицины, основанной на доказательствах. Терапевтический архив 2007;79(12):76-83.
- Чичасова Н.В. Инфликсимаб (Ремикейд): возможности в лечении ревмато- идного артрита. Современная ревматология 2011;1:67-75.
- Jones G, Sebba A, Gu J et al. Comprasion of tocilizumab monotherapy versus methotrexate in patients with moderate to severe rheumatoid arthritis: The Ambition study. Ann Rheum Dis 2010;69(1):86-8.
- Taylor PC, Feldman M. Anti-TNF biologic agents: still the therapy of choice for rheumatoid arthritis. Nat Rev Rheumatol 2009;5(10):578-82.
- Марусенко И.М. Терапия ревматоидного артрита с применением генно- инженерных биологических препаратов в Республике Карелия. Современная ревматология 2013;4:97-100.
- Приказ МЗ СР РФ N315n от 4 мая 2019г. “Об утверждении Порядка оказа- ния медицинской помощи больным с ревматическими заболеваниями” (Приложение 8).
- Brandt J, Haibei H, Cornely D, et al. Suecessful treatment of active ankylosing spondilytis with the tumor necrosis factor alpha monoclonal antibody Infliximab. Arthr Rheum 2000;43:1346-52.
- Provenzano G, Termini A, le Moli C, et al. Efficacy of infliximab in psoriatic arthritis resistant to treatment with disease modifying antirheumatic drugs: an open pilot study. Ann Rheum Dis 2003;62:680-1.
- Charles P, Elliott MJ, Davis D, et al. Regulation of cytokines in rheumatoid arthritis following anti-TNF-{alpha} therapy inhibitiors, and acute-phase proteins. J Immunol 1999;163:1521-8.
- Agrawal S, Misra R, Aggarwal A. Autoantibodies in rheumatoid arthritis: associa- tion with severity of disease in established RA. Clin Rheumatol 2007;26:201-4.
- Ates A, Kinikli G, Turgay M, et.al. Effects of rheumatoid factor isotypes on dis- ease activity and severity in patients with rheumatoid arthritis: a comparative study. Clin Rheumatol 2007;26:538-45.
- Амирджанова В.Н., Кайгородцева Е.Ю., Горячев Д.В. и др. Российский регистр инфликсимаба. Влияние терапии на функциональное состояние больных ревматоидным артритом. Научно-практическая ревматология 2010;6:23-30.
- Лукина Г.В., Сигидин Я.А., Позднякова Е.С. и др. Инфликсимаб в россий- ской клинической практике. Современная ревматология 2013;3:37-43.
- Eliott M, Maini R, Feldman M, et al. Randomized double-blind comparision of chimeric monoclonal antibody to tumor necrosis factor (cA2) in patients with rheumatoid arthritis. Lancet 1994;341:1105-10.
- Kavanaugh A, Cush J, St.Clair E, et al. Anti-TNF monoclonal antibody treatment of rheumatoid arthritis with active disease on methotrexate: results of open label, related dose administration following a single dose, double-blind, placebo-con- trolled trial. Arhtr Rheum 1996;39 (suppl.):S244.
- Балабанова Р.М. Инфликсимаб: на все ли вопросы получены ответы за 10 лет? Современная ревматология 2010;1:61-5.
- Насонов Е.Л. Эффективность и безопасность ингибиторов фактора некроза опухоли-альфа при ревматоидном артрите. РМЖ 2008; 24(334):1602-10
