Cовременные подходы к медикаментозной терапии остеоартрита
Признаки центральной сенситизации определяются у трети пациентов с остеоартритом (ОА), что обосновывает назначение не только нестероидных противовоспалительных средств (НПВП), но и препаратов центрального действия.
Оценка эффективности антиконвульсанта прегабалина в комбинации с ацеклофенаком в лечении хронического болевого синдрома у больных ОА коленных суставов.
В исследование были включены 60 женщин с ОА коленных суставов с признаками нейропатической боли, которую оценивали с помощью опросников DN4 и Pain DETECT. Пациентки были рандомизированы на две группы по 30 человек и в течение 42 дней получали комбинированную терапию ацекло- фенаком в дозе 100 мг два раза в сутки и пре- габалином в дозе 75 мг два раза в сутки в течение 14 дней и 150 мг два раза в сутки в течение следующих 28 дней или монотерапию ацеклофенаком в дозе 100 мг два раза в сутки. Для оценки эффективности лечения применяли индекс WOMAC, визуальную аналоговую шкалу (ВАШ), опросники HADS (эмоциональ- но-аффективная сфера) и EQ-5D (качество жизни)
Комбинированная терапия нестероидным противовоспалительным препаратом и прегабалином вызывала более выраженное уменьшение интенсивности боли по ВАШ, функциональных нарушений по WOMAC и нейропатических дескрипторов, чем монотерапия НПВП.
У пациентов с ОА коленных суставов необходимо оценивать наличие выраженной центральной сенситизации, которая служит основанием для лечения хронического болевого синдрома с использованием НПВП в комбинации с прегабалином.
Повышение качества жизни пациента, страдающего хроническим заболеванием, является одной из основных задач, стоящих перед врачом. Всемирная организация здравоохранения провела ис сле дование, целью которого была оценка состояния здоровья населения земного шара. В исследовании, продолжавшемся 23 года, приняли участие 188 стран и были проанализированы 301 заболевание и 3227 их осложнений. Согласно полученным данным в России лидирующими причинами снижения качества жизни являются боль в нижней части спины, боль в шейном отделе позвоночника и остеоартрит (ОА) [1].
ОА – неоднородная группа заболеваний различной этиологии со сходными биологическими, морфологическими, клиническими проявлениями и исходами, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондральной кости, синовиальной оболочки, связок, капсулы, околосуставных мышц [2]. Основное проявление остеоартрита – хроническая боль, которая вызывает снижение качества жизни и функциональной активности пациентов.
Препаратами выбора для лечения ОА являются нестероидные противовоспалительные препараты (НПВП), однако 27-61% пациентов, несмотря на лечение, продолжают испытывать хроническую боль [3]. НПВП оказывают периферическое противовоспалительное действие, направленное на источник боли, и вызывают уменьшение афферентного болевого потока, однако в ряде случаев этого оказывается недостаточным для ее купирования. В связи этим пациентам, у которых хроническая боль сопровождается нейропатическими дескрипторами, такими как онемение, жжение, покалывание, ползание мурашек, аллодиния и т.д., рекомендуют назначение препаратов центрального действия из группы антиконвульсантов [4].
Целью исследования была оценка эффективности антиконвульсанта прегабалина в комбинации с ацеклофенаком в лечении хронического болевого синдрома у больных ОА коленных суставов.
Материалы и методы
Рандомизированное открытое клиническое исследование проводилось в соответствии с принципами Хельсинкской декларации. Протокол его был одобрен на заседании этического комитета института ФГБНУ НИИР им В.А. Насоно вой. Все пациенты дали информированное согласие на участие в исследовании.
Критерии включения: женщины в возрасте от 45 до 65 лет с первичным ОА коленных суставов, установленным согласно критериям Американской ревматологической ассоциации 1991 г. [17], наличие нейропатической боли, которую оценивали с помощью опросника DN4 (>4). Критерии исключения: сопутствующие заболевания, сопровождающиеся хроническим болевым синдромом, не связанным с ОА (корешковый синдром, диабетическая или алкогольная полинейропатия и др.; психические заболевания, затрудняющие адекватную оценку болевого синдрома, эмоционального состояния и заполнение опросников; противопоказания к назначению прегабалина; хондропротективная терапия в течение по крайней мере 3 мес до начала исследования.
После скрининга и подписания информированного согласия пациенток рандомизировали на две группы и в течение 42 дней проводили комбинированную терапию ацеклофенаком в дозе 100 мг два раза в сутки в сочетании с прегабалином (Прегабалин-Рихтер®, Гедеон Рихтер) в дозе 75 мг два раза в сутки в течение 14 дней и 150 мг два раза в сутки в течение следующих 28 дней или монотерапию ацеклофенаком (Аэртал®, Гедеон Рихтер) в дозе 100 мг два раза в сутки. Рандомизация производилась на основании порядкового номера: пациентки с нечетными порядковыми номерами (1, 3 ...) составили 1-ю группу, а с четными (2, 4 ...) – 2-ю группу.
Исследование состояло из трех визитов. Во время первого визита (исходного) проводили клинико-неврологическое обследование, определяли функциональный индекс WOMAC, оценивали интенсивность боли в покое и при движении по визуальной аналоговой шкале (ВАШ), наличие нейропатической боли (опросники DN4 и Pain DETECT), эмоционально-аффективную сферу (опросник HADS) и качество жизни (опросник EQ-5D). Во время второго визита на 14-й день определяли функциональный индекс WOMAC и интенсивность боли при движении. Во время третьего визита на 42-й день повторяли все исследования, предусмотренные для первого визита.
Статистическая обработка материала проводилась с помощью компьютерной программы Statistiса-10.0. Для описания количественных переменных использованы методы описательной статистики с вычислением средних величин. При нормальном распределении данные представлены в виде среднего значения (М) и стандартного отклонения (SD), данные, не имеющие нормального распределения, – в виде медианы. Для проверки статистических гипотез применялись параметрические и непараметрические критерии Фишера, x2, t-тест Стьюдента, Манна-Уитни.
Результаты
Характеристика пациенток.В исследование были включены 60 женщин в возрасте в среднем 59,8±4,5 года с ОА коленных суставов, которых рандомизировали на две группы по 30 человек. При неврологическом обследовании пациенток не было выявлено признаков органического поражения как периферической соматосенсорной нервной системы, так и центральных ее отделов, которое могло бы быть причиной нейропатической боли. Однако при неврологическом осмотре у пациенток выявили чувствительные нарушения (аллодинию, гипестезию и гиперестезию) не только в области пораженных коленных суставов, но и в области голеней, а в ряде случаев и бедер. Аллодиния и гипестезия в области коленных суставов, бедер и голеней отмечались у 16 (26,7%), 2 (3,4%) и 7 (11,7%) из 60 пациенток, соответственно, гиперестезия – у 8 (13,4%), 1 (1,7%) и 13 (21,7%). Чувствительные нарушения отсутствовали только у 8 (13,4%) пациенток, включенных в исследование; различий между группами не было. Перечисленные чувствительные нарушения были анатомически нелогичными (топически не соответствовали какому-либо поражению нервной системы), а также локализовались вне пораженного сустав, что является характерным клиническим признаком центральной сенситизации.
У всех пациенток наблюдалась умеренная или выраженная боль в коленных суставах при движениях и в покое, интенсивность которой была сопоставимой в двух группах. Индексы WOMAC и показатели нейропатической боли (DN4, Pain DETECT) были достоверно выше у больных 1-й группы, получавших комбинированную терапию (табл. 1). Выявленные различия могли объясняться большей длительностью заболевания, которая является предиктором возникновения нейропатического компонента боли и худшей функциональной активности пациенток.
| Показатель | 1-я группа | 2-я группа | р |
|---|---|---|---|
| Возраст, лет | 60,2±4,3 | 59,4±4,7 | 0,48 |
| Рост, см | 161,1±5,6 | 160,7±5,9 | 0,69 |
| Масса тела, кг | 89,2±13,7 | 83,7±13,6 | 0,25 |
| Индекс массы тела, кг/м2 | 38,9±18,0 | 36,9±18,5 | 0,27 |
| Длительность ОА, лет | 12,9±4,9 | 9,7±6,7 | 0,02 |
| R-стадия по КеллгренуЛоуренсу | |||
| II | 19 | 23 | 0,13 |
| III | 11 | 7 | 0,06 |
| WOMAC | 1385,30±365,83 | 1206,04±358,72 | 0,06 |
| боль | 277,50±86,02 | 236,35±79,78 | 0,11 |
| скованность | 107,57±36,99 | 92,34±41,97 | 0,15 |
| функциональная недостаточность | 1000,27±263,86 | 874,90±261,56 | 0,05 |
| Боль по ВАШ, мм | |||
| при движениях | 61,60±14,91 | 56,07±22,58 | 0,43 |
| в покое | 58,70±15,50 | 62,80±19,80 | 0,11 |
| DN4 | 5,97±1,24 | 5,35±0,93 | 0,04 |
| Pain DETECT | 17,93±3,87 | 15,03±5,26 | 0,02 |
| HADS-T | 9,93±4,21 | 10,0±2,71 | 0,89 |
| HADS-D | 7,80±3,88 | 8,17±2,30 | 0,66 |
| EQ-5D | 0,29±0,31 | 0,26±0,30 | 0,71 |
| ВАШ EQ-5D, мм | 45,50±14,34 | 43,82±15,06 | 0,81 |
Клиническая эффективность.В обеих группах через 14 дней было выявлено достоверное улучшение функциональной активности, которую оценивали с помощью индекса WOMAC (табл. 2). При продолжении комбинированной терапии ацеклофенаком и прегабалином наблюдалось дальнейшее снижение этого индекса (p=0,01 по сравнению со вторым визитом), в то время как при монотерапии ацеклофенаком он существенно не изменился (р=0,49). Через 42 дня значение индекса WOMAC у больных двух групп снизилось на 35% и 19% по сравнению с исходным, соответственно.
| 1-я группа | 2-я группа | |||||
|---|---|---|---|---|---|---|
| 0 | 14 дней | 42 дня | 0 | 14 дней | 42 дня | |
| Примечание: *p<0,05 между 1 и 2 визитом, **p<0,05 между 2 и 3 визитом | ||||||
| Индекс боли при движениях по ВАШ, мм | 61,6±14,9 | 45,3±16,1* | 36,2±18,1** | 56,1±22,6 | 44,9±18,7* | 42,0±24,0 |
| Индекс функциональной активности WOMAC | 1385,3±365,8 | 1034,7±402,3* | 886,6±456,3** | 1206,0±358,7 | 1016,5±428,5* | 976,6±408,0 |
Интенсивность боли при движениях в 1-й группе достоверно снизилась через 14 дней и еще в большей степени через 42 дня (различия были достоверными как между первым и вторым, так и вторым и третьим визитами; p=0,04) (табл. 2). Во 2-й группе интенсивность боли при ВАШ при движении также снизилась через 14 дней (p=0,031), однако в последующем не изменилась. Наличие статистически значимых изменений индекса WOMAC и выраженности боли при движении на протяжении всей терапии свидетельствует о большей эффективности ацеклофенака в комбинации с прегабалином по сравнению с монотерапией ацеклофенаком.
Качественные характеристики боли в двух группах до и после лечения оценивали с помощью опросника DN4. В 1-й группе после лечения было выявлено статистически достоверное (p<0,005) уменьшение частоты жжения (с 86,7% до 33,4%), прострелов как ударом тока (с 90,0% до 40,0%), ползания мурашек (с 86,7% до 50,0%), покалывания (с 83,4% до 43,4%), онемения (с 90,0% до 56,7%), пониженной чувствительности к покалыванию (с 60,0% до 23,4%), пониженной чувствительности к прикосновению (с 16,7% до 10,0%), аллодинии (с 16,7% до 6,7% ), в то время как во 2-й достоверно уменьшилась только частота зуда (с 16,7% до 3,4%) и болезненного ощущения холода (с 56,7% до 23,4%).
Через 42 дня у пациентов обеих групп было выявлено достоверное снижение баллов по опросникам DN4 и Pain DETECT (рис. 1). Более выраженная положительная динамика нейропатической боли отмечалась у пациентов 1-й группы, которые получали комбинированную терапию ацеклофенаком и прегабалином.
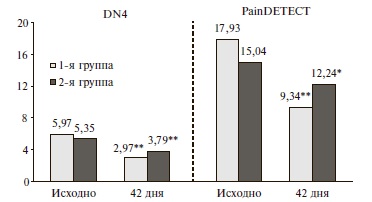
При оценке эмоционально-аффективной сферы с помощью опросника HADS перед началом терапии у пациентов обеих групп выявили умеренное тревожное расстройство (9,93±4,21 и 10,0±2,71, p<0,89). Комби ниро ван ная терапия ацеклофенаком и прегабалином привела к достоверному уменьшению показателя тревоги (до 7,27±3,91; p<0,007), в то время как при монотерапии ацеклофенаком он достоверно не изменился (9,49±3,42; р<0,4), что указывало на сохранение субклинической тревоги.
Переносимость и безопасность.У 6 (20%) из 30 пациенток 1-й группы в первые 3-5 суток от начала приема прегабалина наблюдались головокружение или ощущение “пьяной головы”, которые прошли самостоятельно. Дискомфорт и боли в эпигастральной области отмечались у 6 (20%) и 7 (24%) пациенток двух групп, соответственно Присоединение омепразола к основной терапии позволило купировать эти нежелательные явления. У 1 (3%) пациентки 2-й группы во время лечения был заподозрен инфаркт миокарда, в связи с чем она была исключена из исследования после второго визита (при дополнительном обследовании диагноз инфаркта миокарда подтвержден не был).
Обсуждение
Целью рандомизированного клинического исследования было сравнение эффективности комбинированной терапии ацеклофенаком (Аэртал®) и прегабалином (Прегабалин-Рихтер®), действующей на два механизма хронической боли (воспаление и центральная сенситизация), и монотерапии ацеклофенаком у пациенток с ОА. У всех пациенток с помощью опросника DN4 были выявлены признаки нейропатической боли, которую расценивали как отражение центральной сенситизации в связи с отсутствием органического повреждения нервной системы. Комбинированная терапия по анальгетической эффективности и влиянию на функциональную активность больных превосходила монотерапию НПВП. Кроме того, применение прегабалина оказывало анксиолитическое действие, что было ранее показано при лечении генерализованного тревожного расстройства [6,7]. Анксиолитический эффект препарата также может способствовать уменьшению интенсивности боли [8].
Согласно современным представлениям о патогенезе болевого синдрома выделяют три типа боли: ноцицептивную (воспалительную), нейропатическую, обусловленную поражением соматосенсорной нервной системы, и дисфункциональную (боль при центральной сенситизации). В клинической практике болевой синдром нередко носит смешанный характер, когда отмечаются признаки сразу нескольких типов боли. Универсальным механизмом, поддерживающим сохранение любой боли, является центральная сенситизация, которая представляет собой повышенную реактивность центральных ноцицептивных нейронов, вызывающую усиление боли. Центральная сенситизация формируется чаще всего в результате постоянной афферентной ноцицептивной импульсации – “мощного залпа” болевых импульсов, направленных в задние рога спинного мозга, в результате чего возникают гипервозбудимость центральных ноцицепторов и их неадекватная реакция на обычные стимулы. Клинические признаки центральной сенситизации включают в себя аллодинию (болевую реакцию на неболевые стимулы), вторичную гипералгезию (расширение первичной зоны боли), снижение порогов боли в неболевой зоне, феномен взвинчивания (усиление боли при каждом последовательном болевом раздражении).
Центральная регуляция боли при ОА остается недостаточно изученной. В проведенных исследованиях было показано наличие качественных нейропатических характеристик боли у пациентов с ОА коленных суставов в виде онемения, жжения, аллодинии, прострелов как ударом тока и др. [13,15,16]. Установлено отсутствие корреляции между степенью структурных изменений в пораженном суставе и интенсивностью боли. При этом у 40% пациентов с изменениями в суставах и окружающих тканях боль вовсе отсутствовала [17]. После адекватно выполненного эндопротезирования коленного сустава боль сохранялась у 30-44% больных [18], что указывало на роль не только периферических (воспаление), но и других механизмов в генезе хронической боли. С помощью функциональной МРТ было показано, что множество областей в головном мозге при ОА находятся в активном состоянии (ствол мозга, передняя поясная зона, правая дорзолатеральная префронтальная кора, левая средняя фронтальная извилина, левая латеральная затылочная область, таламус) по сравнению с контролем несмотря на лечение НПВП [19,20]. В единичных исследованиях лечение препаратами центрального действия (антиконвульсантом прегабалином и антидепрессантом дулоксетином) вызывало умень шение не только болевого синдрома, но и тревожнодепрессивных нарушений [21]. В плацебо-контролируемом исследовании терапия дулоксетином была эффективной у 30% пациентов с ОА коленных суставов [22].
Рассматривая ОА как модель хронической боли, можно предположить, что именно центральная сенситизация, наряду с хроническим воспалением, обеспечивает длительное сохранение боли. Воздействие на основные механизмы хронической боли является залогом успешного ее лечения. Ноцицептивный механизм, обусловленный воспалительными и дегенеративными изменениями пораженного сустава, имеет очевидное значение в патогенезе боли при ОА коленных суставов. В связи с этим все такие пациенты нуждаются в традиционной терапии НПВП, в частности в нашем исследовании они получали ацеклофенак (Аэртал®). В недавно проведенном исследовании Е.Ф. Туровская обнаружила нейропатические черты при отсутствии каких-либо признаков поражения нервной системы у 37% пациентов с ОА [23]. Эти данные подтверждаются также рядом зарубежных исследований. При проведении количественного сенсорного тестирования с помощью функциональной МРТ во время серий импульсов была выявлена повышенная активация нейронов ствола мозга околоводопроводного серого вещества [24]. A. Aşkin и соавт. с помощью опросников DN4 и Pain DETECT обнаружили нейропатические дескрипторы у 46,7% и 66,7% пациентов с ОС, соответственно. Признаки нейропатии прямо коррелировали с интенсивностью боли по ВАШ и нарушением функциональной активности по WOMAC [25].
Заключение
Центральная сенситизация, наряду с воспалением, принимает участие в патогенезе хронической боли при ОА коленных суставов. У ряда пациентов она является выраженной и может быть причиной недостаточной эффективности НПВП. Перед началом лечения у пациентов с ОА коленных суставов необходимо оценивать наличие выраженной центральной сенситизации с помощью опросников, предназначенных для выявления нейропатической боли (DN4). При наличии >4 баллов по опроснику DN4 для более эффективного контроля боли целесообразно назначение комбинированной терапии НПВП и прегабалином в дозе 150-300 мг/сут. Противотревожное действие прегабалина также способствует уменьшению интенсивности хронического болевого синдрома при ОА коленных суставов.
Используемые источники
- Давыдов ОС. Распространенность болевых синдромов и их влияние на качество жизни в мире и в России, по данным исследования глобального б ремени болезней за период с 1990 по 2013 г. Российский журнал боли 2015;40(3–4):11–8. [Davydov OS. The prevalence of pain syndromes and their impact on quality of life in the world and Russia according to the data of the Global Burden of Disease Study in the period 1990 to 2013. Rossiyskiy Zhurnal B oli 2015;40(3–4):11–8 (In Russ.)].
- Российские клинические рекомендации. Ревматология. Под редакцией академика РАН Насонова Е.Л. М.:ГЭОТАР-Медиа. 2017:240-52. [Rossiiskie rekomendacii. Revmotologia. Pod redakciei akademika Nasonova E.L. M.:GEOTAR-Media. 2017: 240-52 (In Russ.)].
- Breivik H, Collett B, Ventafridda V, et al. Survey of chronic pain in Europe: prevalence, impact on daily life, and treatment. Europ J Pain 2006;10:287–333.
- Attal N, Cruccu G, Haanpaa M, et al. EFNS guidelines on pharmacological treatment of neuropathic pain. Europ J Neurol 2006, 13:1153–69.
- Altman RG, Alarcon D, Appelouth D, et al. The American College of Rheu - m atology criteria for the classification and reporting of osteoarthritis of the hip. Arhritis Rheum 1991;34:505-14.
- Baldwin DS, Ajel K, Masdrakis VG, et al. Pregabalin for the treatment of gener- alized anxiety disorder: an update. Neuropsychiatr Dis Treat 2013;9:883-92.
- Buoli M, Caldiroli A, Serati M. Pharmacokinetic evaluation of pregabalin for the treatment of generalized anxiety disorder. Expert Opin Drug Metab Toxicol 2 017;13(3):351-9.
- Ohmichi Y, Ohmichi M, Murai N, et al. Therapeutic effects of diclofenac, prega- balin, and duloxetine on disuse-induced chronic musculoskeletal pain in rats. Sci Rep 2018;8(1):3311.
- Baron R, Binder A. How neuropathic is sciatica? The mixed pain concept. Orthopade 2004;33(5):568-75.
- Hansson P, Fields H, Hill R, Marchettini P. Neuropathic pain: pathophysiology and treatment. Progress in Pain Research and Management. Seattle, WA: IASP Press; 2001;21:151-67.
- Hochman JR, Gagliese L, Davis AM, Hawker GA. Neuropathic pain symptoms in a community knee OA cohort. Osteoarthr Cartilage 2011;19:647-54. 1 2. Hochman JR, Davis AM, Elkayam J, et al. Neuropathic pain symptoms on the modified pain DETECT correlate with signs of central sensitization in knee osteoarthritis. Osteoarthritis Cartilage 2013;21:1236-42.
- Im HJ, Kim JS, Li X, et al. Alteration of sensory neurons and spinal response to an experimental osteoarthritis pain model. Arthritis Rheum 2010;62(10):29953005.
- Туровская Е.Ф., Алексеева Л.И., Филатова Е.Г. Механизмы хронической боли при остеоартрозе коленного сустава. Научно-практическая ревмато - логия 2014;52(5):526-29 [Turovskaya EF, Alekseeva LI, Filatova EG. Mechanisms of chronic pain at osteoarthrosis of the knee. Nauchno-praktich- eskaya revmatologiya = Rheumatology Science and Practice 2014;52(5):526-29. (In Russ.)].
- Hochman JR, French MR, Bermingham SL. The nerve of osteoarthritis pain. Arthr Care Res 2010;62(7):1019-23.
- Moreton BJ, Tew V, Nair R, et al. Pain phenotype in people with knee osteoarthritis; classification and measurement properties of painDETECT and SLANSS in a cross-sectional study. Arthritis Care Res (Hoboken) 2015;67(4):51928.
- Sofat N, Ejindu V, Kiely P. What makes osteoarthritis painful? The evidence for local and central pain processing. Rheumatology 2011;50(12):2157-65.
- Wylde V, Hewlett S, Learmonth ID et all. Persistent pain after joint replacement: Prevalence, sensory qualities, and postoperative determinants. Pain 2011;152: 566–72.
- Gwilym SE, Keltner JR, Warnaby CE. Psychophysical and functional imaging evidence supporting the presence of central sensitization in a cohort of osteo - arthritis patients. Arthr Rheum 2009;61(9):1226-34.
- Sofat N, Smee C, Hermansson M, et al. Functional MRI demonstrates pain per- ception in hand osteoarthritis has features of central pain processing. J Biomed Graph Comp 2013;3(4):10.5430/jbgc.v3n4p20.
- Sofat N, Harrison A, Russell MD, et al. The effect of pregabalin or duloxetine on arthritis pain: a clinical and mechanistic study in people with hand osteoarthritis. J Pain Res 2017:10:2437-49.
- Chappell AS, Ossanna MJ, Liu-Seifert H. Duloxetine, a centrally acting analgesic, in the treatment of patients with osteoarthritis knee pain: a 13-week, randomized, placebo-controlled trial. Pain 2009;146(3):253-60.
- Туровская Е.Ф. Неврогенные механизмы в патогенезе хронического болево- го синдрома у пациентов с остеоартрозом. Дис. ... канд. мед. наук. Москва, 2012. http://www.mma.ru/upload/444413.pdf.
- Gwilym SE, Keltner JR, Warnaby CE, et al. Psychophysical and functional imag- ing evidence supporting the presence of central sensitization in a cohort of o steoarthritis patients. Arthritis Rheum 2009;61:1226-34.
- Aşkin A, Özkan A, Tosun A, et al. Quality of life and functional capacity are a dve rsely affected in osteoarthritis patients with neuropathic pain. Kaohsiung J Med Sci 2017;33(3):152-8.
