Ориентация на центральное АД – перспективный подход к ведению пациентов с неконтролируемой артериальной гипертоний, сахарным диабетом 2 типа и хронической болезнью почек
Сравнение эффективности коррекции комбинированной антигипертензивной терапии (АГТ) у пациентов с неконтролируемой артериальной гипертонией, сахарным диабетом 2 типа и хронической болезнью почек 3 стадии по уровню АД в плечевой артерии или центрального АД.
В открытое рандомизированное одноцентровое исследование включено 60 пациентов, у которых измеряли клиническое периферическое и центральное АД и проводили суточное мониторирование АД (СМАД). Пациенты были рандомизированы на две группы в соотношении 1:1. У пациентов основной группы дозы антигипертензивных препаратов титровали на основании центрального АД, контрольной группы – на основании периферического АД. Всем больным назначали фиксированные комбинации индапамид/ периндоприл или амлодипин/индапамид/ периндоприл в разных дозах в зависимости от уровня АД. Целевым уровнем периферического АД считали <140/85 мм рт. ст., целевой уровень центрального АД определяли в зависимости от возраста и пола. Продолжитель ность исследования составила 6 месяцев.
Через 1 мес увеличение доз антигипертензивных препаратов потребовалось у 93% пациентов обеих групп, через 3 мес – у 13% и 37% пациентов основной и контрольной групп, соответственно (p=0,07). Медиана снижения периферического систолического АД через 6 мес в двух группах составила 25 и 27 мм рт. ст., центрального – 28 и 26 мм рт. ст., соответственно. Целевое АД было достигнуто в 97% и 93% случаев.
При сопоставимом влиянии на клиническое периферическое и центральное АД, в основной группе отмечена тенденция к более быстрому достижению целевого АД и снижению частоты использованию максимальных доз трехкомпонентной АГТ.
Артериальная гипертония (АГ) – один из наиболее важных факторов риска развития сердечно-сосудистых заболеваний [1]. Закономерные последствия АГ включают в себя хроническую сердечную недостаточность, ишемическую болезнь сердца (ИБС), инсульт и снижение функции почек [2-4]. Лечение АГ имеет особое значение у пациентов с сахарным диабетом (СД) как для профилактики сердечно-сосудистых заболеваний, так и снижения риска прогрессирования хронической болезни почек (ХБП). Ингибиторы ангиотензинпревращающего фермента (АПФ) и блокаторы рецепторов ангиотензина II (БРА) замедляют прогрессирование нефропатии и предотвращают появление альбуминурии более эффективно, чем другие антигипертензивные средства. В связи с этим они являются препаратами первой линии при лечении АГ у пациентов с СД и ХБП, у которых терапию необходимо начинать с фиксированной комбинации, включающей помимо ингибитора АПФ/БРА блокатор кальциевых каналов или диуретик [5-8].
Сочетание СД и ХБП повышает риск развития неблагоприятных исходов у больных с АГ [8-11] и затрудняет подбор эффективной антигипертензивной терапии (АГТ), обеспечивающей достижение целевого АД [12,13]. Высказано предположение, что центральное (аортальное) АД более тесно ассоциируется с поражением органов-мишеней [14], общей и сердечно-сосудистой смертностью, чем периферическое АД [15]. В исследовании BP GUIDE были показаны эффективность и безопасность подбора АГТ на основании значений центрального АД у пациентов с неосложненной АГ [16].
В многочисленных исследованиях изучалось влияние различных классов антигипертензивных препаратов на центральное систолическое АД (САД). Хотя эти исследования были небольшими, различались по продолжительности лечения и методам оценки центрального САД, в целом при применении ингибиторов АПФ обнаружена тенденция к снижению центрального САД, в то время как в отношении других классов препаратов данные оказались более противоречивыми [17-20]. Эффективность антигипертензивной стратегии, ориентированной на уровень центрального АД, у пациентов с СД 2 типа и ХБП ранее не изучалась.
Целью исследования было сравнение эффективности коррекции комбинированной АГТ у пациентов с неконтролируемой АГ, СД 2 типа и ХБП 3 стадии по уровню центрального АД или АД в плечевой артерии.
Материал и методы
В открытое рандомизированное одноцентровое исследование включали пациентов старше 18 лет с сочетанием СД 2 типа, ХБП (скорость клубочковой фильтрации, рассчитанная по формуле CKD-EPI 30-60 мл/мин/1,73 м2) и эссенциальной АГ, не леченной или не контролируемой на фоне стабильной моно- или комбинированной АГТ в течение предыдущих трех месяцев. Критериями невключения были возраст старше 80 лет, систолическое и диастолическое АД≥180 и/или 110 мм рт. ст., сердечно-сосудистые заболевания, связанные с атеросклерозом, фибрилляция предсердий, хроническая сердечная недостаточность III-IV функционального класса, альбуминурия >300 мг/г креатинина в разовой порции мочи, женщины репродуктивного возраста, индивидуальная непереносимость ингибиторов АПФ, тиазидных и тиазидоподобных диуретиков или блокаторов кальциевых каналов.
Все пациенты подписывали информированное согласие на участие в исследовании, протокол которого был одобрен Комитетом по Этике Медицинского института РУДН (протокол №10/17).
У всех пациентов измеряли клиническое периферическое и центральное АД и проводили суточное мониторирование АД (СМАД) и обычное лабораторное обследование (рис. 1). Продолжительность исследования составила 6 мес.
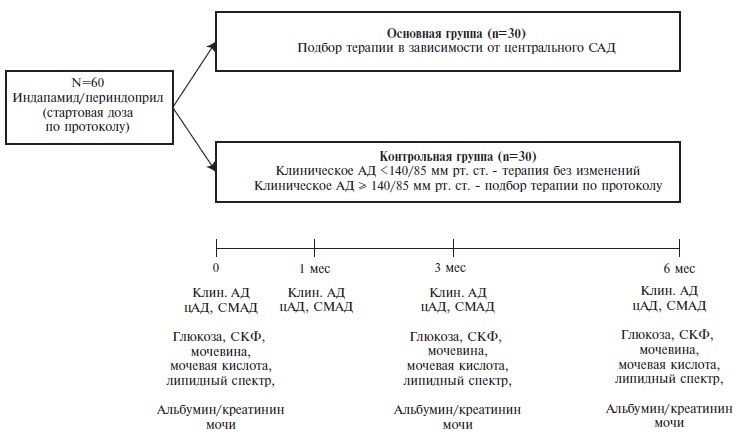
Измерение АД. Периферическое офисное АД измеряли с помощью валидированного автоматического сфигмоманометра в положении сидя после 10-минутного отдыха. Анализировали среднее значение трех измерений с интервалом 3-5 минут. На первом визите АД измеряли на обеих руках, в дальнейшем – на руке с более высокими значениями АД. Для измерения центрального систолического и диастолического АД (ДАД) и оценки суточного профиля АД применяли валидированный осциллометрический прибор BPLab Vasotens (ООО "Петр Телегин", Нижний Новгород).
| Сценарий | Доза, мг |
|---|---|
| Примечание: АГТ – антигипертензивная терапия, ДАД – диастолическое АД, САД – систолическое АД | |
| • САД 140-159 и/или ДАД 85-99 мм рт.ст. и/или | 0,625/2,5 |
| • Отсутствие АГТ ранее или монотерапия | |
| • САД 160-179 и/или ДАД 100-109 мм рт.ст. и/или | 1,25/5 |
| • Отсутствие АГТ или двухкомпонентная АГТ (свободная или фиксированная комбинация) в средних дозах | |
| • Двухкомпонентная АГТ в максимальных дозах и/или | 2,5/10 |
| • Трехкомпонентная терапия в минимальных или средних дозах | |
Принципы назначения и коррекции антигипертензивной терапии. Всем пациентам исходно назначали фиксированную комбинацию периндоприл/индапамид. Доза определялась исходным периферическим АД и количеством антигипертензивных препаратов, принимаемых до включения в исследование (табл. 1). Далее пациентов рандомизировали на две группы в соотношении 1:1 методом конвертов. В основной группе титрование дозы антигипертензивных препаратов проводили на основании значений центрального САД, в контрольной – на основании значений периферического АД. Целевым значением периферического АД считали <140/85 мм рт. ст. (исследование было начато до выхода рекомендаций по лечению АГ Европейского общества кардиологов/Европейского общества артериальной гипертонии 2018 г.). Целевое центральное систолическое АД определяли в зависимости от возраста и пола по нормативам А. Herbert и соавт. (табл. 2) [21].
| Пол | Возраст, лет | ||||||
|---|---|---|---|---|---|---|---|
| <20 | 20-29 | 30-39 | 40-49 | 50-59 | 60-69 | 70-79 | |
| Муж | 103-111 | 105-113 | 109-118 | 113-122 | 115-124 | 117-126 | 118-127 |
| Жен. | 98-107 | 101-110 | 105-116 | 109-120 | 115-126 | 118-128 | 119-128 |
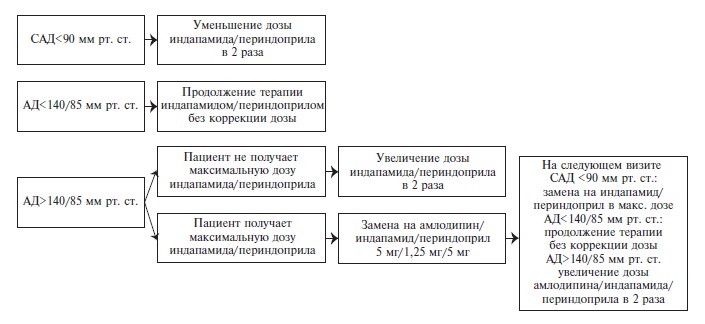
Коррекция дозы препарата осуществлялась через 1, 3 и 6 мес от начала терапии. Алгоритм изменения дозы препаратов в контрольной группе изображен на рис. 2. В основной группе изменение терапии осуществлялось в зависимости от значений центрального САД и среднего периферического АД за сутки аналогично сценариям, использовавшимся в исследовании BP GUIDE (табл. 3) [16]. Целевым уровнем суточного АД считали значения <130/80 мм рт. ст. [6].
| Сценарий | Доза | |
|---|---|---|
| • Клиническое периферическое АД в пределах целевых значений или выше | Увеличение дозы | |
| • СМАД в пределах целевых значений или выше | ||
| • Центральное САД выше целевых значений | ||
| • Клиническое периферическое АД в пределах целевых значений или выше | Без изменений | |
| • СМАД в пределах целевых значений или выше | ||
| • Центральное САД в пределах целевых значений или ниже | ||
| • Клиническое периферическое АД в пределах целевых значений или выше | Снижение | |
| • СМАД в пределах целевых значений | ||
| • Центральное САД ниже целевых значений |
Статистический анализ. Статистический анализ данных проводился с использованием программы Statistica (версия 8.0). Количественные переменные в случае нормального распределения представлены как M±SD, где M – среднее, SD – стандартное отклонение; при асимметричном распределении – как Ме (IQR), где Ме – медиана, а IQR – интерквартильный размах. Качественные данные представлены в виде абсолютных (n) и относительных (%) значений. Для сравнения двух групп в случае непрерывных переменных в зависимости от типа распределения использовали критерий Стьюдента или U-критерий Манна-Уитни. Динамику АД оценивали при помощи критерия Вилкоксона. Стати стически значимыми считали различия при двустороннем значении р<0,05.
Результаты
В открытое рандомизированное одноцентровое исследование были включены 60 пациентов, которых рандомизировали на две группы по 30 человек. В обеих группах преобладали женщины и часто встречались дислипидемия и ожирение (табл. 4). Две группы были сопоставимы по основным клинико-демографическим параметрам. В контрольной группе были выше сывороточные концентрации общего холестерина (ОХС) и холестерина липопротеидов низкой плотности (ХС ЛНП), достоверно чаще отмечалась ХБП 3а стадии и несколько реже – С3б стадии.
| Показатели | Контрольная группа (n=30) | Основная группа (n=30) | p |
|---|---|---|---|
| Примечание: АГ – артериальная гипертония, ИМТ – индекс массы тела, ОХС – общий холестерин, СД – сахарный диабет, СКФ – скорость клубочковой фильтрации, ССТ – сахароснижающая терапия, ХС-ЛНП – холестерин липопротеидов низкой плотности, HbA1c – гликированный гемоглобин | |||
| Возраст, годы | 58 (54;63) | 57 (48;63) | 0,57 |
| Женщины, n (%) | 24 (80) | 18 (60) | 0,08 |
| ИМТ, кг/м2 | 30 (27;33) | 31 (28;36) | 0,19 |
| ИМТ ≥30 кг/м2, n (%) | 13 (43) | 18 (60) | 0,20 |
| Длительность АГ, лет | 13 (10;17) | 12 (9;15) | 0,26 |
| Длительность СД, лет | 9 (6;10) | 10 (8;15) | 0,17 |
| Курение, n (%) | 8 (27) | 7 (23) | 0,99 |
| Дислипидемия, n (%) | 24 (80) | 21 (70) | 0,55 |
| ОХС, ммоль/л, | 5,7 (4,2;6,0) | 4,4 (3,8;5,8) | 0,03 |
| ХС ЛНП, ммоль/л | 3,0 (2,4;3,8) | 2,5 (2,1;3,0) | 0,01 |
| Триглицериды, ммоль/л | 2,0 (1,6;2,8) | 1,95 (1,5;2,7) | 0,83 |
| Статины, n (%) | 12 (40) | 12 (40) | 0,99 |
| HbA1c, % | 7,3 (7,0;8,5) | 8,0 (7,2;9,2) | 0,07 |
| Пероральная ССТ, n (%) | 15 (50) | 9 (30) | 0,19 |
| Креатинин, мкмоль/л | 110 (99;117) | 120 (110;132) | 0,02 |
| СКФ, мл/мин/1,73 м2 | 53 (49;56) | 52 (48;56 | 0,51 |
| С3а | 28 (93) | 26 (87) | 0,02 |
| С3б | 2 (7) | 4 (13) | 0,09 |
| Альбуминурии, n (%) | |||
| А1 | 15 (50) | 11 (37) | 0,43 |
| А2 | 15 (50) | 19 (63) | 0,43 |
| Калий, ммоль/л | 4,2 (4,0;4,5) | 4,2 (4,0;4,5) | 0,64 |
| Альбумин/креатинин мочи, мг/г | 36 (23;85) | 39 (12;88 | 0,80 |
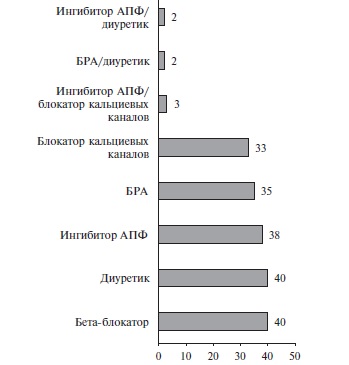
Характеристика антигипертензивной терапии. До начала исследования пациенты в основном получали терапию свободными комбинациями антигипертензинвых препаратов, чаще всего b-адреноблокаторов, ингибиторов АПФ, диуретиков, блокаторов кальциевых каналов и/или БРА. Фиксированные комбинации получали лишь 4 (7%) пациента (рис. 3). На моно-, двух- и трехкомпонентной АГТ находились 4 (13%), 13 (43%) и 13 (43%) пациентов контрольной группы, соответственно, и 4 (13%), 18 (60%), 8 (27%) пациентов основной группы. По исходной терапии две группы не различались (p>0,05 для сравнений всех классов препаратов).
Частота коррекции АГТ на визитах в исследуемых группах представлена на рис. 4. Через 1 мес большинству пациентов потребовалось изменить дозу препаратов, необходимость в замене двухкомпонентной АГТ на трехкомпонентную в средних дозах (амлодипин/индапамид/периндоприл 5/1,25/5 мг) возникла у 10 (33%) пациентов контрольной группы и 15 (50%) пациентов основной группы (p=0,19). Через 3 мес увеличение дозы потребовалось 11 (37%) пациентам контрольной группы и 4 (13%) пациентам основной группы (p=0,07). У части пациентов, получающих средние дозы трех антигипертензивных препаратов, пришлось увеличить дозы до максимальных: 7/10 (70%) и 4/15 (27%), соответственно, в двух группах (р=0,049). В целом трехкомпонентную терапию в средних и максимальных дозах получали 12 (40%) пациентов контрольной группы и 16 (53%) пациентов основной группы (p=0,3). Через 6 мес (завершающий визит) двум пациентам контрольной группы и одному пациенту основной группы произведена замена максимальных доз индапамида/периндоприла на амлодипин/индапамид/периндоприл 5/1,25/5 мг. Необходимость уменьшения дозы отмечена у одного пациента контрольной группы на первом визите и у 4 (13,3%) пациентов основной группы на третьем визите. При этом у них не было клинических проявлений гипотонии на момент осмотра и лабораторных признаков ухудшения функции почек.
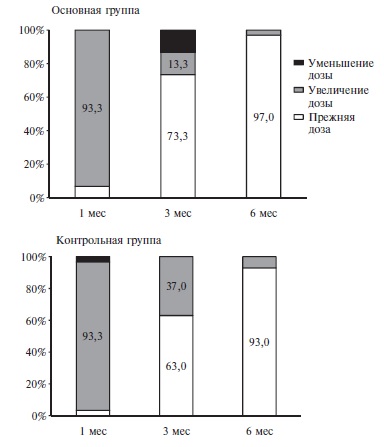
К моменту завершения исследования пациенты основной группы достоверно чаще получали тройную комбинацию в средних дозах, но различий в общем количестве пациентов на трехкомпонентной терапии не выявлено (p=0,61) (табл. 5).
| Препарат | Контрольная группа (n=30) | Основная группа (n=30) | p |
|---|---|---|---|
| Индапамид/периндоприл 0,625 мг/2,5 мг | 0 | 0 | - |
| Индапамид/периндоприл 1,25 мг/5 мг | 6 (20) | 6 (20) | 0,99 |
| Индапамид/периндоприл 2,5 мг/10 мг | 10 (33) | 7 (23) | 0,57 |
| Амлодипин/индапамид/периндоприл 5 мг/1,25 мг/5 мг | 7 (23) | 13 (43) | <0,001 |
| Амлодипин/индапамид/периндоприл 10 мг/2,5 мг/10 мг | 7 (23) | 4 (13) | 0,51 |
Динамика клинического АД в ходе исследования. В обеих группах клиническое периферическое и центральное АД достоверно снизилось по сравнению с исходным (р<0,001 на последнем визите для САД и для ДАД). В основной группе через 1 и 3 мес эти значения были значимо ниже, чем в контрольной группе. От визита к визиту в обеих группах отмечалось достоверное снижение АД по сравнению с предыдущим и по сравнению с исходным (р<0,001). К концу исследования достоверных различий периферического и центрального АД между группами не выявлено (рис. 5).
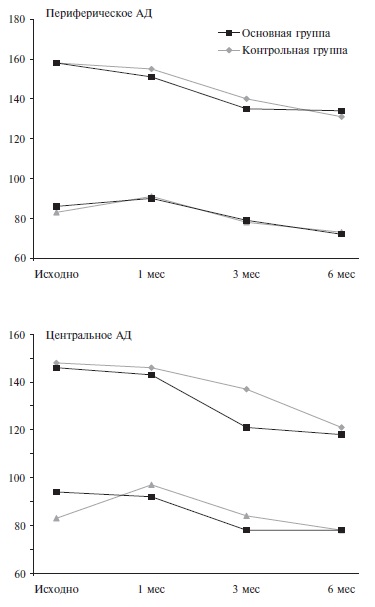
Через 3 мес в основной группе по сравнению с контрольной наблюдалось более выраженное снижение клинического периферического САД (медиана снижения: 22 и 16 мм рт. ст., р=0,007) и клинического центрального САД (медиана снижения: 28 и 19 мм рт. ст., р=0,005). Через 6 мес степень снижения клинического АД была сопоставимой в двух группах: медиана снижения периферического САД в основной и контрольной группах составила 25 (18;31) и 27 (17;32) мм рт. ст., соответственно, центрального САД – 28 (21;24) и 26 (21;34) мм рт. ст., периферического ДАД – 13 (6;19) и 8 (3;15) мм рт. ст., центрального ДАД – 12 (6;23) и 18 (5;21) мм рт. ст.
Большинство пациентов достигли целевых значений клинического периферического АД к моменту завершения исследования. Две стратегии АГТ были одинаково эффективны в этом отношении (табл. 6).
| Срок | Контрольная группа (n=30) | Основная группа (n=30) |
|---|---|---|
| Примечание: р>0,05 | ||
| Исходно | 0 (0) | 0 (0) |
| 1 мес | 1 (3) | 2 (7) |
| 3 мес | 18 (60) | 21 (70) |
| 6 мес | 28 (93) | 29 (97) |
Безопасность терапии. Значимой динамики показателей функции почек и содержания электролитов на фоне лечения не выявлено (табл. 7). Нежелательные явления не зарегистрировали. Терапия сопровождалась снижением уровня креатинина и повышением СКФ в обеих группах.
| Показатели | Контрольная группа (n=30) | Основная группа (n=30) | p | ||
|---|---|---|---|---|---|
| Исходно | 6 мес | Исходно | 6 мес | ||
| Примечание: *p<0,05 при сравнении значений группы стандартного подхода и группы вмешательства | |||||
| Креатинин, мкмоль/л | 110 (99;117) | 98 (90;100) | 120 (110;132)* | 103 (110;115) | <0,001 |
| СКФ, мл/мин/1,73 м2 | 53 (49;56) | 56 (53;58) | 52 (48;56) | 53 (50;57) | 0,07 |
| Альбумин/креатинин мочи, мг/г | 36 (23;85) | 30 (18;65) | 39 (12;88) | 39 (4;78) | 0,87 |
| Калий, ммоль/л | 4,2 (4;4,5) | 4,1 (3,9;4,2) | 4,2 (4;4,5) | 4 (3,9;4,1) | 0,18 |
| Натрий, ммоль/л | 134 (126;140) | 138 (128;140) | 130 (124;141) | 132 (123;143) | 0,21 |
| Хлор, ммоль/л | 103 (100;105) | 103 (99;105) | 102 (98;104) | 103 (100;104) | 0,67 |
| Глюкоза, ммоль/л | 7,9 (5,9;10,0) | 7,3 (5,4;8,2) | 8,9 (6,9;10,2) | 7,6 (5,9;8,9) | 0,12 |
Обсуждение
Центральное САД является доказанным прогностическим фактором развития неблагоприятных сердечнососудистых исходов и уже давно обсуждается как возможная мишень АГТ. Однако возможность использования этого показателя в качестве ориентира при подборе АГТ изучалась в единичных исследованиях, которые проводились в общей популяции пациентов с АГ [16,22]. СД и ХБП ассоциируются с высоким и очень высоким сердечно-сосудистым риском, что определяет необходимость контроля АД у пациентов с этими состояниями. При этом наличие СД и ХБП затрудняет достижение целевого АД и сопровождается высокой частотой скрытой неэффективности лечения и отсутствия снижения АД в ночное время [23-25].
Результаты нашего исследования показали, что две стратегии подбора АГТ на основании периферического или центрального САД оказались одинаково эффективными в отношении достижения целевого периферического АД и снижения центрального АД. При этом в основной группе через 3 мес были достоверно ниже значения периферического и центрального САД. Кроме того, в этой группе отмечалась тенденция к более быстрому подбору терапии и достижению целевого периферического и центрального АД и более редкому использованию максимальных доз трехкомпонентной АГТ. При этом статистическая значимость различий достигнута не была, возможно, в связи с относительно небольшой выборкой и не очень продолжительным периодом наблюдения.
В исследованиях, в которых эффективность АГТ изучали в общей популяции пациентов с АГ, целевое АД через 3 мес лечения было достигнуто в большинстве случаев (83-87%) [26,27], в то время как в нашем исследовании частота достижения целевого АД к указанному сроку в обеих группах была существенно ниже (70% в основной и 60% в контрольной). Лишь через 6 мес достичь целевого АД удалось более чем у 90% пациентов. Данный результат подтверждает относительную резистентность АГ к лечению у пациентов с СД и ХБП.
В целом, полученные нами данные сходны с результатами исследования BP GUIDE [16], в котором степень снижения клинического АД не зависела от метода подбора АГТ, однако при коррекции лечения на основании центрального САД пациентам требовались меньшие дозы антигипертензивных препаратов для адекватного контроля АД. В нашем исследовании выявлена аналогичная тенденция. Очевидно, для пациентов с СД и ХБП возможность приема меньших эффективных доз антигипертензивных препаратов имеет важное значение, учитывая повышение риска нежелательных явлений на фоне нарушения функции почек [28]. Следует отметить, что для адекватного сопоставления результатов двух исследований необходимо применение одинаковых методов оценки доз препаратов. В исследовании BP GUIDE использовалась DDD (defined daily dose) – суточная поддерживающая доза лекарственного средства, используемого по основному показанию у взрослых [29]. В нашем же исследовании такой подход не применялся, так как терапия была стандартизована. Наши данные сопоставимы с результатами исследования W. Kosmala и соавт., в котором оценивалось влияние двух стратегий на систолическую и диастолическую функцию левого желудочка в общей популяции больных АГ [22]. В этом исследовании также не было выявлено достоверной разницы степени снижения периферического и центрального АД.
Эффекты фиксированных комбинаций блокаторов ренин-ангиотензин-альдостероновой системы (РААС) и тиазидного/тиазидоподобного диуретика на центральное АД у пациентов с неконтролируемой АГ изучались и в других исследованиях. В открытом исследовании Ж.Д. Кобалавы и соавт. при применении фиксированной комбинации азилсартана медоксомил/хлорталидона в течение 12 недель 88% пациентов достигли целевого периферического АД [19]. В нашем исследовании выявлено более выраженное снижение центрального АД, что особенно важно ввиду того, что в исследование включали пациентов с сочетанием ХБП и СД, затрудняющих достижение целевых значений АД.
Основными ограничениями работы были небольшое число пациентов и относительно короткая продолжительность лечения.
Заключение
При сопоставимом влиянии на клиническое периферическое и центральное АД подбор АГТ по центральному САД ассоциировался с тенденцией к более быстрой стабилизации АД, более частому достижению целевого АД через 3 мес и несколько более редкому использованию максимальных доз трех антигипертензивных препаратов. Подтверждена безопасность использования данного подхода в отношении функции почек и электролитного баланса. Таким образом, данный метода подбора АГТ, вероятно, может использоваться при лечении пациентов с сочетанием АГ, СД и ХБП 3 стадии. Необходимы более крупные и длительные исследования с целью изучения влияния разных стратегий подбора АГТ на риск сердечно-сосудистых событий.
Используемые источники
- Kjeldsen SE. Hypertension and cardiovascular risk: General aspects. Pharmacol Res 2018;129:95-9.
- Lewington S, Clarke R, Qizilbash N, et al. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360:1903–13.
- Flint AC, Conell C, Ren X, et al. Effect of systolic and diastolic blood pressure on cardiovascular outcomes. N Engl J Med 2019;381(3):243-51.
- Hsu CY, McCulloch CE, Darbinian J, et al. Elevated blood pressure and risk of end-stage renal disease in subjects without baseline kidney disease. Arch Intern Med 2005;165(8):923-8.
- Tuttle KR, Bakris GL, Bilous RW, et al. Diabetic kidney disease: a report from an ADA Consensus Conference. Diabetes Care 2014;37:2864–83.
- Williams B, Mancia G, Spiering W, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology and the European Society of Hypertension. J Hypertens 2018;36(10):1953-2041.
- Артериальная гипертензия у взрослых. Клинические рекомендации 2020. Российский кардиологический журнал. 2020;25(3):3786 [Arterial hypertension in adults. Clinical guidelines 2020. Russ J Cardiol 2020;25(3):3786 (In Russ.)].
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood-pressure-lowering treatment on outcome incidence in hypertension: 10 – Should blood pressure management differ in hypertensive patients with and without diabetes mellitus? Overview and meta-analyses of randomized trials. J Hypertens 2017;35:922–44.
- Emdin CA, Rahimi K, Neal B, et al. Blood pressure lowering in type 2 diabetes: a systematic review and meta-analysis. JAMA 2015;313:603–15.
- Ettehad D, Emdin CA, Kiran A, et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet 2016;387:957–67.
- Brunstrom M, Carlberg B. Effect of antihypertensive treatment at different blood pressure levels in patients with diabetes mellitus: systematic review and metaanalyses. BMJ 2016;352:i717.
- Van Buren PN, Toto R. Hypertension in diabetic nephropathy: epidemiology, mechanisms, and management. Adv Chronic Kidney Dis 2011;18(1):28–41.
- Rossignol P, Massy ZA, Azizi M, et al. The double challenge of resistant hypertension and chronic kidney disease. Lancet 2015;386(10003):1588-98.
- Mitchell GF. Effects of central arterial aging on the structure and function of the peripheral vasculature: implications for end-organ damage. J Appl Physiol 2008;105(5):1652-60.
- Vlachopoulos C, Aznaouridis K, O’Rourke MF, et al. Prediction of cardiovascular events and all-cause mortality with central haemodynamics: a systematic review and meta-analysis. Eur Heart J 2010;31:1865–71.
- Sharman JE, Marwick TH, Gilroy D, et al. Randomized trial of guiding hypertension management using central aortic blood pressure compared with best-practice care: principal findings of the BP GUIDE study. Hypertension 2013;62(6): 1138-45.
- McEniery CM, Cockcroft JR, Roman MJ, et al. Central blood pressure: current evidence and clinical importance. Eur Heart J 2014;35(26):1719-25.
- Morgan T, Lauri J, Bertram D, Anderson A. Effect of different antihypertensive drug classes on central aortic pressure. Am J Hypertens 2004;17:118–23.
- Кобалава Ж.Д., Виллевальде С.В., Кулаков В.В. Антигипертензивные эффекты фиксированной комбинации азилсартана медоксомил/хлорталидон у пациентов с неконтролируемой артериальной гипертонией. Кардио ло гия 2017;57(11):12-8 [Kobalava ZD, Villevalde SV, Kulakov VV. Antihyperte nsive efficacy of fixed combination azilsartan medoxomil/chlorthalidone in patients with uncontrolled arterial hypertension. Kardiologiia 2017;57(11):12-8 (In Russ.)].
- Mackenzie IS, McEniery CM, Dhakam Z, et al. Comparison of the effects of antihypertensive agents on central blood pressure and arterial stiffness in isolated systolic hypertension. Hypertension 2009;54:409–13.
- Herbert A, Cruickshank JK, Laurent S, et al. Establishing reference values for central blood pressure and its amplification in a general healthy population and according to cardiovascular risk factors. Eur Heart J 2014;35(44):3122-33.
- Kosmala W, Marwick TH, Stanton T, et al. Guiding hypertension management using central blood pressure: effect of medication withdrawal on left ventricular function. Am J Hypertens 2016;29(3):319-25.
- Babu M, Drawz P. Masked hypertension in CKD: increased prevalence and risk for cardiovascular and renal events. Curr Cardiol Rep 2019;21(7):58.
- Sinha AD, Agarwal R. The complex relationship between CKD and ambulatory blood pressure patterns. Adv Chronic Kidney Dis 2015;22(2):102-7.
- Oh SW, Han SY, Han KH et al. Morning hypertension and night non-dipping in patients with diabetes and chronic kidney disease. Hypertens Res 2015;38(12): 889-94.
- Кобалава Ж.Д., Троицкая Е.А., Толкачева В.В. Комбинированная терапия артериальной гипертонии с использованием трехкомпонентной фиксированной комбинации амлодипина, индапамида и периндоприла аргинина в клинической практике: организация и основные результаты программы ДОКАЗАТЕЛЬСТВО. Кардиология 2018;58(9):21-30 [Kobalava ZD, Troit skaya EA, Tolkacheva VV. Combined therapy of arterial hypertension with a triple fixed-dose combination of amlodipine/indapamide/ perindopril arginine in real clinical practice: the organization and the main results of the DOKAZATEL’STVO (Proof) Study. Kardiologiia 2018;58(9):21-30 (In Russ.)].
- Кобалава Ж.Д., Котовская Ю.В., Лукьянова Е.А. Комбинированная терапия артериальной гипертонии с использованием фиксированной комбинации периндоприла аргинина/амлодипина в реальной клинической практике: организация и основные результаты программы КОНСТАНТА. Кардиология 2013;6:25-34 [Kobalava ZhD, Kotovskaya YuV, Lukyanova EA. Combined therapy of arterial hypertension with the fixed combination of perindopril arginine/amlodipine in real clinical practice: the organization and the main results of the program CONSTANTA. Kardiologiia 2013;53(6):25-34) (In Russ)].
- Whittaker CF, Miklich MA, Patel RS, Fink JC. Medication safety principles and practice in CKD. Clin J Am Soc Nephrol 2018;13(11):1738–46.
- WHO Collaborating Centre for Drug Statistics Methodology, Guidelines for ATC classification and DDD assignment, 2020. Oslo, 2019.
