Ингибиторы янус-киназ: фармакологические свойства и сравнительные клиническая эффективность и безопасность
Ингибиторы янус-киназ блокируют внутриклеточную сигнальную систему JAK/STAT, которая опосредует действие различных цитокинов, принимающих участие в развитии ревматоидного артрита (РА) и других иммуновоспалительных заболеваний. Целью обзора литературы было сравнение результатов клинических исследований трех ингибиторов янускиназ, отличающихся по селективности действия (тофацитиниба, барицитиниба и упадацитиниба), при РА. Хотя прямые сравнительные исследования этих препаратов не проводились, тем не менее, в контролируемых клинических исследованиях все они по эффективности достоверно превосходили плацебо, а частота ответа на лечение была сопоставимой. Спектр нежелательных эффектов ингибиторов янус-киназ также был сходным.
Ингибиторы янус-киназ относятся к группе пероральных таргетных синтетических базисных противовоспалительных препаратов (тсБПВП), которые оказывают действие на внутриклеточную систему JAK/STAT, опосредующую эффекты различных цитокинов и других молекул, в частности факторов роста гемопоэза и некоторых гормонов. В Российской Федерации для лечения ревматических заболеваний зарегистрированы три ингибитора янускиназ – тофацитиниб (ревматоидный артрит [РА], псориатический артрит), барицитиниб (ревматоидный артрит) и упадацитиниб (ревматоидный артрит). Система JAK/STAT включает в себя четыре янус-киназы (JAK1, JAK2, JAK3 и тирозинкиназу 2 – TYK2), которые при взаимодействии цитокинов с рецепторами I и II типов фосфорилируют белки STAT (signal transducer and activator of transcription), в том числе STAT1, STAT2, STAT3, STAT4, STAT5A, STAT5B и STAT6 (рис. 1). Последние индуцируют транскрипцию генов, опосредующих действие цитокинов. Рецепторы I типа связываются с различными интерлейкинами (ИЛ), колониестимулирующими факторами и гормонами, такими как эритропоэтин, пролактин и гормон роста, рецепторы II типа – с интерферонами и цитокинами семейства ИЛ-10 [1].
![СистемаJAK/STAT, включающая всебя4 янус-киназы- JAK1, JAK2, JAK3 иTYK1 [1]](/img/articles/2021.1/ingibitory-yanus-kinaz-farmakologicheskie-svojstva-i-sravnitelnye-klinicheskaya-ehffektivnost-i-bezopasnost_fig1.jpg)
В отличие от генно-инженерных биологических препаратов, полностью блокирующих функцию определенного провоспалительного цитокина, например, ИЛ-6, ингибиторы янус-киназ модулируют активность различных биологически активных молекул, полная блокада которых может привести к развитию тяжелого иммунодефицита и нарушению гомеостаза [2]. Соответственно, целью применения ингибиторов янус-киназ является обратимое снижение активности одного или нескольких изоферментов, а не полное “выключение" JAK/STAT системы в целом. Эффективность ингибиторов янускиназ связывают в первую очередь с подавлением активности JAK1, в связи с чем разрабатываются препараты, которые обладают более высокой селективностью в отношении этого фермента по сравнению с первыми тсБПВП – тофацитинибом и барицитинибом. К ним относятся филготиниб, упадацитиниб, итацитиниб, солцитиниб и др. Полагают, что применение селективных ингибиторов JAK1 может привести к улучшению результатов лечения РА и других аутоиммунных заболеваний, прежде всего за счет повышения его безопасности, так как некоторые побочные эффекты тсБПВП развиваются в результаты блокады других янус-киназ. Например, цитопении могут быть следствием подавления активности JAK2, которая опосредует действие факторов роста гемопоэза. С другой стороны, селективность ингибиторов янус-киназ гипотетически может привести к снижению эффективности лечения аутоиммунных заболеваний, которые характеризуются дисбалансом многочисленных цитокинов. В частности, ингибирование JAK2 может усилить про тивовоспалительный эффект ингибитора янус-киназ за счет блокады гранулоцитно-макрофагального колониестимулирующего фактора (ГМ-КСФ), обладающего провоспалительной активностью. JAK3 также опосредует действие провоспалительных цитокинов и рассматривается как самостоятельная мишень при разработке новых тсБПВП. Эффективность первых препаратов, избирательно действующих на этот фермент, таких как децернотиниб и пефицитиниб, была показана в плацебо-контролируемых клинических исследованиях II фазы у пациентов с РА [3].
Необходимо учитывать, что селективность действия ингибиторов янус-киназ является относительной и зависит от дозы препарата и его концентрации в крови, метода исследования (биохимический или клеточный), степени проникновения лекарственного вещества в ткани, генетических факторов и т.д. [2]. Например, увеличение концентрации препарата в крови, которая зависит не только от дозы, но и особенностей фармакокинетики у конкретного пациента, обычно сопровождается уменьшением селективности действия любых лекарственных средств. I. McInnes и соавт. в опытах in vitro показали, что тофацитиниб, барицитиниб и упадацитиниб подавляли активность JAK1, 2, и 3, хотя и в разной степени [4]. При этом упадацитиниб, который считается селективным ингибитором JAK1, оказывал действие на JAK2/2-зависимые цитокины ИЛ-3 и ГМСКФ. Сходные данные получили M. Dowty и соавт., которые выявили сопоставимое подавление активности различных цитокинов под действием терапевтических доз тофацитиниба, барицитиниба, упадацитиниба и филготиниба [5].
С клинической точки зрения большее значение имеет не селективность действия ингибиторов янускиназ как таковая, а ее потенциальное влияние на эффективность и безопасность препаратов этой группы. В связи с этим целью обзора литературы было сравнение результатов клинических исследований тофацитиниба, барицитиниба и упадацитиниба при ревматических заболеваниях. Тофацитиниб оказывает действие на JAK1, JAK2 и JAK3 и в меньшей степени на тирозинкиназу 2 (TYK2), в то время как барицитиниб обладает наибольшей активностью в отношении JAK1 и JAK2, а упадацитиниб – в отношении JAK1 [3]. Соответственно, тофацитиниб и барицитиниб считают неселективными ингибиторами янус-киназ, а упадацитиниб – селективным ингибитором JAK1.
Клиническая эффективность ингибиторов янус-киназ при РА
Среди зарегистрированных в Российской Федерации ингибиторов янус-киназ только тофацитиниб имеет дополнительные показания к применению помимо РА (псориатический артрит, псориаз и язвенный колит). В связи с этим ниже анализируются результаты клинических исследований тсБПВП у больных РА. Программы разработки ингибиторов янус-киназ при этом заболевании были сходными и предполагали изучение их эффективности в различных популяциях пациентов, в том числе не получавших метотрексат (МТ) или не отвечающих на лечение МТ, другими БПВП или генноинженерными биологическими препаратами (ГИБП; табл. 1). В настоящее время лечение РА начинают со стандартных БПВП, прежде всего МТ, в то время как применение ингибиторов янус-кинус в качестве препаратов первой линии не рекомендуется [6]. Соот вет ственно, результаты клинических исследований, в которых тсБПВП применяли у пациентов, не получавших МТ или другие стандартные БПВП (ORAL Start, RA-BEGIN и SELECT-EARLY), в данной статье не обсуждаются. В большинстве исследований лечение ингибиторами янус-киназ проводили в комбинации с
| Группы пациентов | Тофацитиниб | Барицитиниб | Упадацитиниб |
|---|---|---|---|
| Не получавшие МТ | ORAL-Start | RA-BEGIN | SELECT-EARLY |
| Неудовлетворительный ответ на МТ |
ORAL-Standard ORAL-Scan ORAL-Strategy |
RA-BEAM | SELECT-COMPARE SELECT- MONOTHERAPY |
| Неудовлетворительный ответ на БПВП |
ORAL-Solo | RA-BUILD | SELECT-NEXT |
| Неудовлетворительный ответ на ГИБП |
ORAL-Sync ORAL-Step |
RA-BEACON | SELECT-BEYOND SELECT-CHOICE |
МТ и/или другими стандартными БПВП, однако в исследованиях ORAL-Solo и SELECT-MONOTHERAPY изучалась эффективность монотерапии тофацитинибом и упадацитинибом, соответственно. В то же время комбинированная терапия ингибиторами янус-киназ и ГИБП не рекомендуется, а эффективность и безопасность такой стратегии лечения РА в клинических исследованиях не изучались. Во всех исследованиях определяли многочисленные первичные и вторичные конечные точки, позволяющие всесторонне оценить противовоспалительную активность тсБПВП и их влияние на прогрессирование РА. Однако ниже эффективность тсБПВП анализируется только на основании одного первичного критерия, который был общим для всех соответствующих исследований (в основном частоты ответа по критериям Американской коллегии ревматологов – АКР 20)
Необходимо отметить, что сопоставление данных, полученных в разных клинических исследованиях, не позволяет адекватно сравнить эффективность ингибиторов янус-киназ, учитывая неизбежные различия выборок пациентов по демографическим показателям, длительности и тяжести РА и другим факторам, влияющим на результаты лечения. При комбинированной терапии ключевое значение имеет также доза МТ, которую при хорошей переносимости препарата сегодня увеличивают до более высоких значений (25-30 мг/нед), чем в прошлом. При оценке сопоставимости выборок плацебо-контролируемых исследований ориентиром в определенной степени может служить частота ответа на прием плацебо.
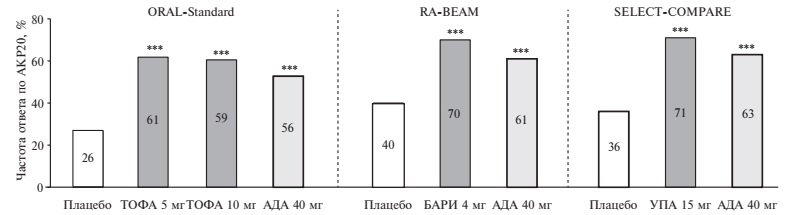
Пациенты, не отвечающие на лечение МТ и/или другими БПВП. Эффективность комбинированной терапии тофацитинибом 5 и 10 мг два раза в сутки, барицитинибом 4 мг один раз в сутки или упадацитинибом 15 мг один раз в сутки с МТ у пациентов с активным РА, не отвечающих на монотерапию МТ, изучали в плацебоконтролируемых исследованиях ORAL-Standard (n=717), RA-BEAM (n=1307) и SELECT-COMPARE (n=1629), соответственно [7-9]. Во всех трех исследованиях была выделена также группа больных, получавших адалимумаб 40 мг каждые 2 недели. Одной из первичных конечных точек была частота ответа по критериями АКР 20, которую оценивали через 6 мес в исследовании ORAL-Standard и через 3 мес в исследованиях RABEAM и SELECT-COMPARE. По частоте ответа по критериям АКР 20 через 3 мес как тофацитиниб и барицитиниб, не обладающие селективностью действия на янус-киназы, так и упадацитиниб, избирательно подавляющий JAK1, достоверно превосходили плацебо (p<0,001). Частота ответа на лечение была практически одинаковой при лечении барицитинибом и упадацитинибом (70% и 71%, соответственно) и несколько ниже при применении тофацитиниба (59-61%). Однако частота ответа на прием плацебо в исследовании ORALStandard, в котором изучался тофацитиниб, также была ниже, чем в двух других исследованиях (26% против 40% и 36%; рис. 2). Это могло отражать как более высокую резистентность больных к лечению, так и меньшие дозы МТ в исследовании ORAL-Standard, которое проводилось около 10 лет назад. Сопоставимые достоверные преимущества всех ингибиторов янус-киназ перед плацебо были выявлены и при анализе других показателей эффективности.
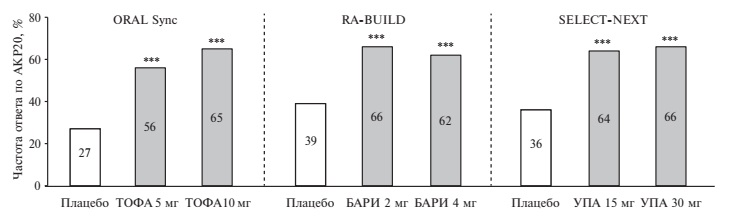
В клинической практике больным активным РА препараты второй линии (тсБПВП или ГИБП) назначают обычно после безуспешных попыток лечения не только МТ, но и другими стандартными БПВП (лефлуномидом, сульфасалазином, гидроксихлорохином), в том числе в виде различных комбинаций. Эффективность тофацитиниба 5 и 10 мг два раза в сутки, барицитиниба 2 и 4 мг один раз в сутки и упадацитиниба 15 и 30 мг один раз в сутки у пациентов, не отвечающих на различные стандартные БПВП, изучалась в плацебо-контролируемых исследованиях ORAL-Sync (n=792), RA-BUILD (n=684) и SELECT-NEXT (n=661), соответственно [10-12]. Во время исследований пациенты продолжали прием стандартного БПВП, чаще всего МТ. У части больных проводилась комбинированная терапия БПВП. Доля таких пациентов была выше в исследовании RA-BUILD (более половины) и ниже в исследованиях ORAL-Sync и SELECT NEXT (около 20-30%). Как и в предыдущих исследованиях, одной из основных первичных конечных точек была частота ответа по критериям АКР 20 через 3 мес (или через 6 мес в исследовании тофацитиниба). По этому критерию все три препарата достоверно превосходили плацебо (рис. 3). Частота ответа на лечение ингибиторами янус-киназ была сопоставимой, хотя частота ответа на прием плацебо в исследовании тофацитиниба была ниже, чем в двух других исследованиях.
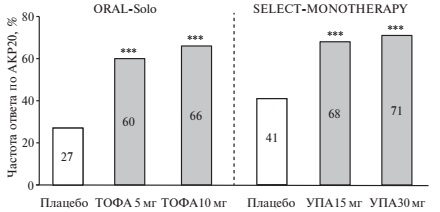
Как и ГИБП, ингибиторы янус-киназ рекомендуется применять в сочетании с МТ, однако на практике значительная часть пациентов с РА по тем или иным причинам, в частности из-за плохой переносимости стандартных БПВП, получают монотерапию тсБПВП. Эффективность монотерапии тофацитинибом 5 или 10 мг два раза в сутки и упадацитинибом 15 или 30 мг один раз в сутки у пациентов с активным РА, не ответивших на стандартные БПВП, изучалась в плацебо-контролируемых исследованиях ORAL-Solo (n=611) и SELECTMONOTHERAPY (n=648), соответственно [13,14]. Одной из общих первичных конечных точек была частота ответа по критериям АКР 20, которую оценивали через 12 недель в ORAL-Solo и через 14 недель в SELECT-MONOTHERAPY. По этому показателю как тофацитиниб, так и упадацитиниб в обеих дозах достоверно превосходили плацебо (рис. 4). Частота ответа на тофацитиниб (60-66%) была несколько ниже частоты ответа на лечение упадацитинибом (68-71%), однако сходные различия между двумя исследованиями отмечались и при анализе частоты ответа на плацебо (27% и 41%, соответственно).
Эффективность монотерапии тофацитинибом в дозе 5 мг два раза в сутки изучалась также в двойном слепом рандомизированном исследовании ORAL-Strategy у 1146 больных активным РА, не ответивших на МТ [15]. Больным основной группы проводилась монотерапия тофацитинибом, а пациенты двух групп сравнения получали комбинированную терапию тофацитинибом с МТ или адалимумабом с МТ. Частота ответа по критериями АКР 50 через 6 мес была сопоставимой в трех группах – 38,3%, 46,0% и 43,8%, соответственно. Однако статистический анализ не подтвердил, что монотерапия тофацитинибом не уступает по эффективности комбинации двух препаратов, в то время как обе схемы комбинированной терапии тофацитинибом/МТ или адалимумабом/МТ обладали сопоставимой эффективностью. Полученные данные свидетельствуют о том, что больным тяжелым и среднетяжелым РА, не отвечающим на МТ или другие стандартные БПВП, тофацитиниб лучше назначать в комбинации с МТ, хотя монотерапия тсБПВП все же возможна, если пациент не переносит МТ и другие стандартные БПВП или имеет противопоказания к их применению [16].
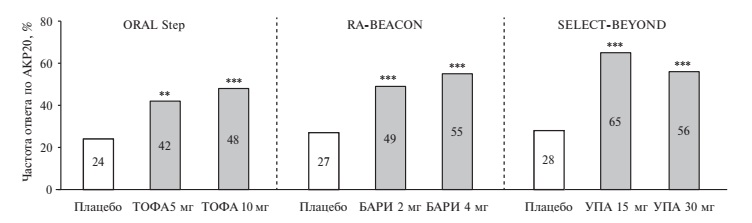
Пациенты, не отвечающие на лечение ГИБП. В настоящее время увеличивается доля больных активным РА, не отвечающих на лечение не только стандартными БПВП, но и ингибиторами фактора некроза опухоли альфа и другими ГИБП. Эффективность тофацитиниба, барицитиниба и упадацитиниба у пациентов, которым потребовалась замена ГИБП в связи с недостаточной эффективностью или плохой переносимостью, изучалась в плацебо-контролируемых исследованиях ORAL-Step (n=399), RA-BEACON (n=527) и SELECT-BEYOND (n=497), соответственно [17-19]. Все больные получали ингибиторы янус-киназ в комбинации с МТ или другими стандартными БПВП в стабильных дозах. Три тсБПВП во всех изученных дозах по эффективности достоверно превосходили плацебо (рис. 5). При сопоставимой частоте ответа по критериям АКР 20 на прием плацебо в трех исследованиях (24-28%) частота ответа через 12 недель была несколько выше при лечении упадацитинибом в рекомендуемой дозе 15 мг один раз в сутки, хотя при применении препарата в дозе 30 мг один раз в сутки она приближалась к таковой при лечении тофацитинибом и барицитинибом. Эффек тивность упадацитиниба в дозе 15 мг один раз в день в комбинации со стандартными БПВП у 612 пациентов, не ответивших на ГИБП, оценивали также в исследовании SELECT-CHOICE, в котором ингибитор янус-киназ сравнивали с абатацептом [20]. По первичным критериям эффективности, включавшим в себя изменение счета DAS28-СРБ и частоту ремиссии через 12 недель, упадацитиниб достоверно превосходил ингибитор костимуляции Т-лимфоцитов.
Таким образом, результаты рандомизированных плацебо-контролируемых исследований подтвердили эффективность всех трех зарегистрированных в России ингибиторов янус-киназ в лечении средне-тяжелого и тяжелого РА в различных популяциях пациентов, в том числе не ответивших на МТ, другие стандартные БПВП и ГИБП. Хотя эффективность тсБПВП не изучали в прямых сравнительных рандомизированных исследованиях, тем не менее приведенные данные свидетельствуют об их сопоставимых преимуществах перед плацебо по частоте ответа по критериям АКР 20, которая была одной из первичных конечных точек в программах 3 фазы.
Безопасность ингибиторов янус-киназ
Безопасность ингибиторов янус-киназ изучалась в двойных слепых рандомизированных исследованиях и открытых исследованиях, которые проводились в продолжение первых, а также в послерегистрационных исследованиях. Например, безопасность тофацитиниба, который был зарегистрирован для лечения РА раньше других ингибиторов янус-киназ (в США препарат был одобрен к применению в 2012 г.), оценивали в программе ORAL, состоявшей из нескольких рандомизированных контролируемых исследований, которые предполагали изучение различных схем терапии в разных популяциях больных РА. После завершения исследований 1-3 фаз часть больных продолжили лечение тофацитинибом в рамках двух международных откры тых исследований (длительность наблюдения до 9,5 лет). Кроме того, в настоящее проводится исследование 4 фазы ORAL Surveillance, в котором сравнивается профиль безопасности тофацитиниба и ингибиторов фактора некроза опухоли альфа более чем у 4300 больных в возрасте старше 50 лет по крайней мере с одним сердечно-сосудистым фактором риска (NCT02092467). Опубликованы также данные наблюдательных исследований, проводившихся в обычной клинической практике, в частности US Corrona Registry и Swiss Registry, которые дополняют результаты рандомизированных контролируемых исследований [21,22].
Данные о безопасности тсБПВП у пациентов с РА и другими заболеваниями постоянно обновляются по мере публикации результатов новых исследований. Основой для настоящего анализа послужили статьи, опубликованные в рецензируемых журналах [23-25]. В них обобщен опыт применения тофацитиниба у 7061 больного РА (22875 пациенто-лет), барицитиниба у 3492 пациентов c РА (6637 пациенто-лет) и упадацитиниба у 3834 больных РА (4020 пациенто-лет). Медиана длительности наблюдения пациентов, получавших три препарата, составила 3,1 года (до 9,6), 2,1 года (до 5,5) и около 1 года (до 2,5), соответственно (табл. 2). Как и в случае эффективности, непосредственно сравнивать частоту нежелательных явлений при применении ингибиторов янус-киназ в разных клинических исследованиях некорректно, так как риск их развития может зависеть от многих факторов, таких как возраст больных, сопутствующий прием глюкокортикостероидов и других иммуносупрессивных препаратов, длительность лечения, дизайн исследования и т.п. Оценить истинный риск развития потенциальных отдаленных нежелательных эффектов ингибиторов янус-киназ сложно, учитывая относительно непродолжительный срок приема плацебо в рандомизированных контролируемых исследованиях препаратов этой группы.
| Тофацитиниб | Барицитиниб | Упадацитиниб | |
|---|---|---|---|
| Примечание: *приведены обобщенные показатели при лечении тофацитинибом в дозах 5 и 10 мг два раза в сутки и барицитинибом в дозах 2 и 4 мг один раз в сутки; для упадацитиниба указана частота нежелательных явлений при применении препарата в дозах 15 и 30 мг один раз в сутки. **исключая немеланомный рак кожи. ВТЭО - венозные тромбоэмболические осложнения | |||
| Число больных | 7061 | 3492 | 3834 |
| Опыт применения, пациенто-лет | 22875 | 6637 | 4020 |
| Максимальная длительность лечения, лет | 9,6 | 5,5 | 2,5 |
| Частота на 100-пациенто-лет* | |||
| Серьезные инфекции | 2,5 | 2,9 | 3,8/6,2 |
| Опоясывающий герпес | 3,6 | 3,2 | 3,7/7,0 |
| Злокачественные опухоли** | 0,8 | 0,8 | 0,9/1,4 |
| ВТЭО | 0,3 | 0,5 | 0,6/0,3 |
| Сердечно-сосудистые исходы | 0,4 | 0,5 | 0,6/1,0 |
| Перфорация кишечника | 0,1 | 0,05 | 0,2/0,3 |
Инфекции. Как и другие БПВП и ГИБП, ингибиторы янус-киназ обладают иммуносупрессивной активностью и могут способствовать развитию инфекций, в том числе серьезных [26]. При лечении этими препаратами чаще всего встречаются бактериальные инфекции – внебольничная пневмония, инфекции мочевыхпутей, кожи и мягких тканей. В клинических исследованиях тофацитиниба частота серьезных инфекций составила 2,5 на 100 пациенто-лет [23]. Она постепенно снижалась по мере увеличения длительности терапии. Факторами риска серьезных инфекционных осложнений были доза препарата, пожилой возраст, мужской пол, лимфопения, лечение глюкокортикостероидами и некоторые сопутствующие заболевания, такие как сахарный диабет и хроническая обоструктивная болезнь легких. При применении барицитиниба частота серьезных инфекций была сходной и составила 2,9 на 100 пациенто-лет [24]. Риск их увеличивался примерно в два раза при одновременном лечении глюкокортикостероидами, однако такой же эффект наблюдался и у пациентов, получавших плацебо. Частота развития серьезных инфекций при лечении упадацитинибом в дозе 15 мг/сут равнялась 3,8 на 100 пациенто-лет и увеличилась до 6,2 на 100 пациенто-лет при назначении препарата в незарегистрированной дозе 30 мг/сут [25]. В целом риск серьезных инфекций при применении ингибиторов янус-киназ был сопоставимым с таковым при лечении ГИБП. По данным мета-анализа 88 исследований, частота серьезных инфекций при назначении абатацепта, ритуксимаба, тоцилизумаба и ингибиторов ФНО-α варьировалась от 3,04 до 5,45 на 100 пациентолет, а при применении тофацитиниба в дозах 5 и 10 мг два раза в сутки составляла 3,02 и 3,00 на 100 пациентолет, соответственно [27].
Опоясывающий герпес. В отличие от бактериальных инфекций, частота которых была сходной при лечении тсБПВП и ГИБП, терапия ингибиторами янус-киназ ассоциировалась с увеличением риска опоясывающего герпеса, что может быть связано с подавлением активности интерферона и ИЛ-15, которые играют ключевую роль в защите от вирусных инфекций [2]. Следует отметить, что у больных РА опоясывающий герпес встречается чаще, чем в общей популяции. Частота развития опоясывающего герпеса при применении тофацитиниба у пациентов с РА составила в среднем 3,6 на 100 пациенто-лет [23], а в плацебо-контролируемых исследованиях примерно в 1,5-2 раза превышала таковую при назначении плацебо [26]. Риск развития опоясывающего герпеса не увеличивался при более длительной терапии тофацитинибом. У 90% больных наблюдалось поражение одного дерматома, в то время как случаи поражения внутренних органов или смерти от герпетической инфекции зарегистрированы не были [23]. Дополнительными факторами риска опоясывающего герпеса при лечении тофацитинибом были возраст и сопутствующая терапия глюкокортикостероидами и/или МТ, а также этническая принадлежность (в Японии и Корее частота герпетической инфекции оказалась выше, чем в США и Европе) [28]. В рандомизированном плацебо-контролируемом исследовании тофацитиниб не влиял на безопасность и иммуногенность вакцины против герпеса у пациентов с РА [29]. В клинических исследованиях частота опоясывающего герпеса при лечении барицитинибом была выше, чем при приеме плацебо, и составила в среднем 3,2 на 100 пациенто-лет, т.е. была сопоставимой с таковой при лечении тофацитинибом [24]. Только у 9% больных наблюдалось поражение нескольких дерматомов, а случаев поражения внутренних органов отмечено не было. Сходные данные были получении и при изучении безопасности упадацитиниба [25]. Таким образом, все зарегистрированные в Российской Федерации ингибиторы янус-киназ вызывали увеличение риска развития опоясывающего герпеса у пациентов с РА. В подавляющем большинстве случаев герпетическая инфекция характеризовалась легким течением и поражением одного дерматома.
Оппортунистические инфекции. При применении всех ингибиторов янус-киназ отмечались случаи оппортунистических инфекций, таких как криптококкокоз, диссеминированный герпес, бронхо-легочный аспергиллез и др., однако частота их, как и туберкулеза, была низкой [23-25]. Случаи туберкулеза в основном регистрировались в странах, эндемичных по этому заболеванию. Тем не менее, перед началом лечения ингибиторами янус-киназ необходимо исключить туберкулезную инфекции, а при наличии латентного или активного туберкулеза показана стандартная антимикобактериальная терапия.
Злокачественные опухоли. Ингибиторы янус-киназ могут оказывать влияние на активность цитокинов и клеток, опосредующих противоопухолевый ответ иммунной системы человека [26]. Риск развития злокачественных опухолей при длительном лечении препаратами этой группы недостаточно изучен. Тем не менее, частота злокачественных опухолей (исключая немеланомный рак кожи) в клинических исследованиях тофацитиниба составила 0,8 на 100 пациенто-лет и не отличалась от таковой в общей популяции у больных РА [23]. В длительных открытых исследованиях риск развития злокачественных опухолей, который анализировали с 6-месячными интервалами, существенно не менялся. Сходные результаты были получены при изучении барицитиниба и упадацитиниба, хотя следует отметить меньшую длительность их применения в клинической практике [24,25].
Венозные тромбоэмболические осложнения. РА, как и другие иммуновоспалительные заболевания, ассоциируется с повышенным риском венозных тромбоэмболических осложнений (ВТЭО). В когортных исследованиях частота ВТЭО у пациентов с РА варьировалась от 0,3 до 0,8 на 100 пациенто-лет и по крайней мере в 2 раза превышала таковую в общей популяции [30-32]. При применении ингибиторов янус-киназ в клинических исследованиях частота ВТЭО была сходной и составила 0,3-0,6 на 100 пациенто-лет [23-25]. В контролируемых исследованиях она не отличалась между группами тофацитиниба, плацебо и адалимумаба [33]. При метаанализе 26 рандомизированных контролируемых исследований неселективных и селективных ингибиторов янус-киназ у больных РА также не было выявлено увеличения риска развития ВТЭО по сравнению с контролем (отношение рисков 1,16; 95% доверительный интервал 0,48-2,81) [34]. Тем не менее, в инструкциях по применению ингибиторов янус-киназ, одобренных в США и Европейском Союзе, содержится предостережение о том, что препараты этой группы повышают риск ВТЭО, поэтому их следует применять с осторожностью у пациентов с известными факторами рисками венозного тромбообразования. Основанием для внесения изменений в инструкции по применению препаратов этой группы послужили промежуточные результаты открытого клинического исследования А3921133, в котором сравнивали безопасность тофацитиниба и ингибиторов ФНО-α у 4362 больных в возрасте 50 лет и старше с РА и по крайней мере одним сердечно-сосудистым фактором риска [35]. В этом исследовании частота тромбоэмболии легочной артерии (ТЭЛА) при лечении тофацитинибом в дозах 5 и 10 мг два раза в сутки и ингибиторами ФНО-α составила 0,54, 0,27 и 0,09 на 100-пациенто-лет, соответственно, а частота тромбоза глубоких вен – 0,38, 0,30 и 0,18 на 100-пациенто-лет. Наиболее значительное увеличение риска развития ТЭЛА наблюдалось у пациентов с факторами риска ВТЭО. Следует отметить, что в наблюдательном когортном исследовании, проводившемся на основании анализа медицинских баз данных (Truven и Medicare), риск развития ВТЭО у больных РА, получавших тофацитиниб или ингибиторы ФНО-α, был сопоставимым [36]. Механизмы потенциальной связи терапии ингибиторами янус-киназ с повышенным риском ВТЭО остаются неясными и нуждаются в дополнительном изучении.
Сердечно-сосудистые исходы. Частота сердечно-сосудистых исходов при лечении тофацитинибом составила 0,4 на 100 пациенто-лет, существенно не отличалась при применении препарата в двух дозах и не менялась при увеличении длительности лечения [23]. Основными сердечно-сосудистыми событиями были фибрилляция предсердий, инфаркт миокарда и коронарная болезнь сердца. Частота сердечно-сосудистых осложнений была низкой и в клинических исследованиях барицитиниба и упадацитиниба [24,25]. При мета-анализе результатов рандомизированных клинических исследований не было выявлено увеличения риска сердечно-сосудистых исходов при лечении ингибиторами янус-киназ (отношение рисков 0,80; 95% доверительный интервал 0,361,75) [34].
Перфорация стенки кишечника. Лечение тоцилизумабом, ингибирующим рецепторы ИЛ-6, в редких случаях осложняется перфорацией кишечника, факторами риска которой является также прием нестероидных противовоспалительных препаратов и глюкокортикостероидов [37]. Ингибиторы янус-киназ подавляют активность ИЛ-6, поэтому в клинических исследованиях специально контролировали риск развития такого осложнения. При применении тофацитиниба были зарегистрированы немногочисленные случаи перфорации стенки желудочно-кишечного тракта, в основном нижних отделов кишечника (n=28) [23]. У большинства пациентов (93%) имелись различные факторы риска, такие как одновременная терапия НПВП или глюкокортикостероидами и другие состояния (дивертикулит, перфорация желудка в анамнезе, полип толстой кишки и т.д.). Отдельные случаи перфорации стенки кишечника были зарегистрированы и при лечении барицитинибом и упадацитинибом [24,25].
Изменения лабораторных показателей. В инструкциях по применению трех ингибиторов янус-киназ указано, что лечение этими препаратами может сопровождаться сходными изменениями лабораторных показателей, в том числе снижением числа нейтрофилов и лейкоцитов в крови, содержания гемоглобина, повышением активности аминотрансфераз, концентраций липидов и активности креатинфосфокиназы [38-40].
Гепатотоксичность при лечении ингибиторами янускиназ встречалась редко. В контролируемых клинических исследованиях, в которых изучали эффективность и безопасность тофацитиниба в комбинации с БПВП, частота повышения активности АЛТ и АСТ по крайней мере в 3 раза по сравнению с верхней границей нормы в течение первых 3 мес составила, соответственно, 1,2% и 0,5% в группе тофацитиниба 5 мг два раза в сутки и 0,9% и 0,7% в группе плацебо. При более длительной комбинированной терапии тофацитинибом 5 мг два раза в сутки и БПВП повышение активности АЛТ и АСТ наблюдали в 1,8% и <1,0% случаев, соответственно [38]. При монотерапии барицитинибом в дозе 4 мг один раз в сутки у больных РА частота повышения активности АЛТ и АСТ по крайней мере в 3 раза по сравнению с верхней границей нормы (1,0% и 0,8%, соответственно) была сопоставимой с таковой при приеме плацебо (1,0% и 0,8%), однако она увеличивалась при комбинированной терапии барицитинибом и гепатоксичными БПВП, такими как МТ (7,5% и 3,8%) [39]. В плацебоконтролируемых исследованиях увеличение активности АЛТ и АСТ по крайней мерез в 3 раза по сравнению с верхней границей нормы при комбинированной терапии упадацитинибом в дозе 15 мг один раз в сутки и БПВП было выявлено в 2,1% и 1,5% случаев, соответственно, а в группе плацебо – в 1,5% и 0,7% [40].
Все ингибиторы янус-киназ вызывали относительно небольшое повышение уровней липидов, в том числе общего холестерина, холестерина липопротеидов низкой (ЛНП) и высокой (ЛВП) плотности. В контролируемых клинических исследованиях при лечении тофацитинибом в дозе 5 мг два раза в сутки уровень холестерина ЛНП увеличился в среднем на 15% через 12 мес и на 16% через 24 мес, а уровень холестерина ЛВП – на 17% и 19%, соответственно [38]. При этом коэффициенты ЛНП/ЛВП и АпоВ/АпоА1 существенно не изменились. В длительных исследованиях тофацитиниба доля пациентов, получавших статины, постепенно увеличилась с 12,9% до 25,0% через 90-96 мес [23]. В контролируемых клинических исследованиях у больных РА частота повышения концентрации общего холестерина (≥5,17 ммоль/л) при применении барицитиниба в дозе 4 мг один раз в сутки и плацебо составила 49,1% и 15,8%, соответственно, холестерина ЛНП (≥3,36 ммоль/л) – 33,6% и 10,3%, холестерина ЛВП (≥1,55 ммоль/л) – 42,7% и 13,8% [39]. Сходные результаты были получены и при применении упадацитиниба в дозе 15 мг один раз в сутки [40]. Так, повышение уровня общего холестерина (≥5,17 ммоль/л) наблюдалось у 62% и 31% больных групп упадацитиниба и плацебо, соответственно, холестерина ЛНП (≥3,36 ммоль/л) – у 42% и 19%, холестерина ЛВП (≥1,03 ммоль/л) – у 89% и 61%. Следует отметить, что повышение содержания холестерина ЛВП при лечении ингибиторами янускиназ может нивелировать возможный атерогенный увеличения концентрации холестерина ЛНП.
В контролируемых клинических исследованиях у больных РА при лечении тофацитинибом в дозах 5-10 мг два раза в сутки снижение абсолютного числа лимфоцитов в крови менее 500 в мм3 отмечалось у 0,3% больных, а до 500-750 в мм3 – у 1,9%, в длительных клинических исследованиях – у 1,3% и 8,4%, соответственно [38]. Частота нейтропении <1000 в мм3 в контролируемых клинических исследованиях тофацитиниба составила 0,08%. При этом случаев снижения числа нейтрофилов менее 500 мм3 зарегистрировано не было. При более длительной терапии препаратом увеличения частоты нейтропении не отмечено. При лечении барицитинибом в клинических исследованиях частота нейтропении (<1000 в мм3), лимфопении (<500 в мм3) и анемии (<8 г/дл) была менее 1% [39]. При применении этого препарата у 2,0% больных РА отмечалось повышение числа тромбоцитов в крови >600000 в мм3, однако ассоциации тромбоцитоза с тромботическими осложнениями выявлено не было. Нейтропения, лимфопения и анемия в редких случаях (≤1%) регистрировались и в клинических исследованиях упадацитиниба [40]. Возможность снижения уровня гемоглобина при лечении селективным ингибитором янус-киназ может свидетельствовать о том, что он оказывает действие на JAK2, опосредующей активность факторов роста гемопоэза [25].
В редких случаях (<1%) при лечении ингибиторами янус-киназ отмечалось также увеличение активности КФК более чем 5 раз по сравнению с верхней границей нормы. Обычно оно было преходящим и бессимптомным и не требовало прекращения терапии [38-40].
Заключение
При отсутствии прямых сравнительных исследований судить о сопоставимости или различиях клинических эффектов неселективных (тофацитиниба и барицитиниба) и селективных (упадацитиниб) ингибиторов янус-киназ у больных РА сложно. Тем не менее, в контролируемых клинических исследованиях все три препарата по эффективности достоверно превосходили плацебо, а частота ответа на лечение была сходной. При применении трех ингибиторов янус-киназ были зарегистрированы одинаковые побочные эффекты, т.е. по безопасности они также существенно не отличались. Определенным недостатком тофацитиниба является необходимость приема два раза в день, однако в настоящее время зарегистрирована пролонгированная форма препарата, которую назначают один раз в день. Необходимы прямые сравнительные исследования ингибиторов янус-киназ для оценки возможных преимуществ отдельных препаратов этой группы. В настоящее время нет оснований считать, что селективность действия на определенные янус-киназы ассоциируется с повышением эффективности и/или безопасности у больных РА.
Используемые источники
- Shuai K, Liu, B. Regulation of gene-activation pathways by PIAS proteins in the immune system. Nat Rev Immunol 2005;5:593–605.
- Choy EH. Clinical significance of Janus kinase inhibitor selectivity. Rheumatology (Oxford) 2019;58(6):953-62.
- Virtanen AT, Haikarainen T, Raivola J, Silvennoinen O. Selective JAKinibs: prospects in inflammatory and autoimmune diseases. BioDrugs 2019;33:15–32.
- McInnes IB, Byers NL, Higgs RE, et al. Comparison of baricitinib, upadacitinib, and tofacitinib mediated regulation of cytokine signaling in human leukocyte subpopulations. Arthritis Res Ther 2019;21(1):183.
- Dowty ME, Lin TH, JessonMI, et al. Janus kinase inhibitors for the treatment of rheumatoid arthritis demonstrate similar profiles of in vitro cytokine receptor inhibition. Pharmacol Res Perspect 2019;7(6):e00537.
- Smolen JS, Landewé RBM, Bijlsma JWJ, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2019 update. Ann Rheum Dis 2020;79(6):685-99.
- van Vollenhoven RF, Fleischmann R, Cohen S, et al. Tofacitinib or adalimumab versus placebo in rheumatoid arthritis. N Engl J Med 2012;367(6):508-519.
- Taylor PC, Keystone EC, van der Heijde D, et al. Baricitinib versus placebo or adalimumab in rheumatoid arthritis. N Engl J Med 2017;376(7):652-62.
- Fleischmann R, Pangan AL, Song IH, et al. Upadacitinib versus placebo or adalimumab in patients with rheumatoid arthritis and an inadequate response to methotrexate: results of a phase III, double-blind, randomized controlled trial. Arthritis Rheumatol 2019;71(11):1788-800.
- Kremer J, Li ZG, Hall S, et al. Tofacitinib in combination with nonbiologic disease-modifying antirheumatic drugs in patients with active rheumatoid arthritis: a randomized trial. Ann Intern Med 2013;159:253–61.
- Dougados M, van der Heijde D, Chen YC, et al. Baricitinib in patients with inadequate response or intolerance to conventional synthetic DMARDs: results from the RA-BUILD study. Ann Rheum Dis 2017;76(1):88-95.
- Burmester GR, Kremer JM, Van den Bosch F, et al. Safety and efficacy of upadacitinib in patients with rheumatoid arthritis and inadequate response to conventional synthetic disease-modifying anti-rheumatic drugs (SELECT-NEXT): a randomised, double-blind, placebo-controlled phase 3 trial. Lancet 2018;391 (10139):2503-12.
- Fleischmann R, Kremer J, Cush J, et al. Placebo-controlled trial of tofacitinib monotherapy in rheumatoid arthritis. N Engl J Med. 2012;367(6):495-507.
- Smolen JS, Pangan AL, Emery P, et al. Upadacitinib as monotherapy in patients with active rheumatoid arthritis and inadequate response to methotrexate (SELECT-MONOTHERAPY): a randomised, placebo-controlled, double-blind phase 3 study. Lancet 2019;393(10188):2303-11.
- Fleischmann R, Mysler E, Hall S, et al. Efficacy and safety of tofacitinib monotherapy, tofacitinib with methotrexate, and adalimumab with methotrexate in patients with rheumatoid arthritis (ORAL Strategy): a phase 3b/4, doubleblind, head-to-head, randomised controlled trial. Lancet 2017;390(10093):457-68.
- Новиков П.И., Моисеев С.В. Исследование ORAL Strategy – стратегия лечения ревматоидного артрита. Клин фармакол тер 2017;26(5):66-72 [Novikov P, Moiseev S. ORAL Strategy trial: the choice of the strategy of treatment for rheumatoid arthritis. Clin Pharmacol Ther = Klinicheskaya farmako logiya i terapiya 2017;26(5):66-72 (In Russ.)].
- Burmester GR, Blanco R, Charles-Schoeman C, et al. Tofacitinib (CP-690,550) in combination with methotrexate in patients with active rheumatoid arthritis with an inadequate response to tumour necrosis factor inhibitors: a randomised phase 3 trial. Lancet 2013;381(9865):451-60.
- Genovese MC, Kremer J, Zamani O et al. Baricitinib in patients with refractory rheumatoid arthritis. N Engl J Med 2016;374:1243-52.
- Genovese MC, Fleischmann R, Combe B, et al. Safety and efficacy of upadacitinib in patients with active rheumatoid arthritis refractory to biologic diseasemodifying anti-rheumatic drugs (SELECT-BEYOND): a double-blind, randomised controlled phase 3 trial. Lancet 2018;391(10139):2513-24.
- Rubbert-Roth A, Enejosa J, Pangan AL, et al. Trial of upadacitinib or abatacept in rheumatoid arthritis. N Engl J Med 2020;383(16):1511-21.
- Kremer J, Bingham C, Cappelli L, et al. Post-approval comparative safety study of tofacitinib and biologic DMARDS: five-year results from a US-based rheumatoid arthritis registry. Ann Rheum Dis 2019;78:82–3.
- Kyburz D, Riek M, Herzog L, et al. Real-world use of tofacitinib in rheumatoid arthritis: data from the Swiss clinical quality management RA registry. Arthritis Rheumatol 2016;68:1637
- Cohen SB, Tanaka Y, Mariette X, et al Long-term safety of tofacitinib up to 9.5 years: a comprehensive integrated analysis of the rheumatoid arthritis clinical development programme RMD Open 2020;6:e001395.
- Smolen JS, Genovese MC, Takeuchi T, et al. Safety profile of baricitinib in patients with active rheumatoid arthritis with over 2 years median time in treatment. J Rheumatol 2019;46(1):7-18.
- Cohen SB, van Vollenhoven RF, Winthrop KL, et al. Safety profile of upadacitinib in rheumatoid arthritis: integrated analysis from the SELECT phase III clinical programme. Ann Rheum Dis 2020; published online ahead of print, 2020 Oct 28.
- Winthrop KL. The emerging safety profile of JAK inhibitors in rheumatic disease. Nat Rev Rheumatol 2017;13(4):234-43.
- Strand V, Ahadieh S, French J, et al. Systematic review and meta-analysis of serious infections with tofacitinib and biologic disease-modifying antirheumatic drug treatment in rheumatoid arthritis clinical trials. Arthritis Res Ther 2015;17:362
- Winthrop KL, Yamanaka H, Valdez H, et al. Herpes zoster and tofacitinib therapy in patients with rheumatoid arthritis. Arthritis Rheumatol 2014;66:2675–84.
- Winthrop KL, Wouters AG, Choy EH et al. The safety and immunogenicity of live zoster vaccination in patients with rheumatoid arthritis before starting tofacitinib: a randomized phase II trial. Arthritis Rheumatol 2017;69:1969-77.
- Holmqvist ME, Neovius M, Eriksson J, et al. Risk of venous thromboembolism in patients with rheumatoid arthritis and association with disease duration and hospitalization. JAMA 2012;308(13):1350–6.
- Choi HK, Rho YH, Zhu Y, et al. The risk of pulmonary embolism and deep vein thrombosis in rheumatoid arthritis: a UK population-based outpatient cohort study. Ann Rheum Dis 2013;72(7):1182–7.
- Ogdie A, Kay McGill N, et al. Risk of venous thromboembolism in patients with psoriatic arthritis, psoriasis and rheumatoid arthritis: a general population-based cohort study. Eur Heart J 2018;39(39):3608–14.
- Mease PJ, Kremer J, Cohen S, et al. Incidence of thromboembolic events in the tofacitinib rheumatoid arthritis, psoriasis, psoriatic arthritis and ulcerative colitis development programs [abstract]. Arthritis Rheumatol 2017;69(suppl 10).
- Xie W, Huang Y, Xiao S, et al. Impact of Janus kinase inhibitors on risk of cardiovascular events in patients with rheumatoid arthritis: systematic review and meta-analysis of randomised controlled trials. Ann Rheum Dis 2019;78(8):104854.
- Direct Healthcare Professional Communication. XELJANZ (tofacitinib): increased risk of venous thromboembolism and increased risk of serious and fatal infections. 7th February 2020.
- Desai RJ, Pawar A, Weinblatt ME, Kim SC. Comparative risk of venous thromboembolism in rheumatoid arthritis patients receiving tofacitinib versus those receiving tumor necrosis factor inhibitors: an observational cohort study. Arthritis Rheumatol 2019;71(6):892–900.
- Curtis JR, Lanas A, John A, et al. Factors associated with gastrointestinal perforation in a cohort of patients with rheumatoid arthritis. Arthritis Care Res (Hoboken) 2012;64:1819–28.
- https://www.ema.europa.eu/en/documents/product-information/xeljanz-eparproduct-information_en.pdf.
- https://www.ema.europa.eu/en/documents/product-information/olumiant-eparproduct-information_en.pdf.
- https://www.ema.europa.eu/en/documents/product-information/rinvoq-eparproduct-information_en.pdf.
