Характеристика пациентов с фибрилляцией предсердий и хронической сердечной недостаточностью, получающих прямые оральные антикоагулянты: данные одноцентрового регистра
В популяции пациентов с фибрилляцией предсердий (ФП) и хронической сердечной недостаточностью (ХСН) изучить клинико-эпидемиологические характеристики, сопутствующие заболевания, риск тромбоэмболических осложнений (ТЭО) и кровотечений, предпочтения врачей при назначении прямых оральных антикоагулянтов (ПОАК), частоту ошибок при дозировании ПОАК.
В ретроспективное исследование были включены 388 пациентов с сочетанием ФП и ХСН, получавших ПОАК и последовательно госпитализированных в центр ХСН (ГКБ им. В.В. Виноградова города Москвы) в 2021-2022 гг. в экстренном или плановом порядке. Проводился анализ клинического профиля пациентов, предпочтений врачей при назначении ПОАК, частоты ошибок при дозировании ПОАК.
Среди обследованных пациентов преобладали лица пожилого возраста, мужчины с высоким уровнем коморбидности и риском ТЭО (4,7±1,5 баллов по шкале CHA2 DS2-VASс). Основными факторами риска ТЭО были ХСН (100%), артериальная гипертония (94,8%) и возраст старше 75 лет (77,1%). Высокий риск геморрагических осложнений по шкале HAS-BLED (≥3 баллов) отмечался у 26,3% пациентов. Модифицируемые факторы риска кровотечения были выявлены у 88,7% больных. Чаще всего пациентам назначали ривароксабан (54,1%), реже – апиксабан (24,2%) и дабигатран (21,7%). Ошибки при выборе дозы ПОАК встречались у 101 (29,6%) из 341 пациента. В корректной дозировке чаще всего назначали дабигатран (в 95,2% случаев), в некорректной – апиксабан (в 43,4% случаев).
Для изучаемой популяции характерны высокие коморбидность и риск ТЭО. Риск кровотечений в большинстве случаев может быть минимизирован за счет коррекции модифицируемых факторов риска. Ошибки при дозировании ПОАК (преимущественно необоснованно сниженные дозы) встречаются почти у каждого третьего пациента с ФП и ХСН (чаще при назначении апиксабана).
Фибрилляция предсердий (ФП) – самая распространенная аритмия, которой в мире страдают более 30 млн человек [1]. ФП сопровождается значительным увеличением смертности и частоты тромбоэмболических осложнений [2]. ФП часто сочетается с хронической сердечной недостаточностью (ХСН) за счет общих факторов риска (ФР) и патофизиологических механизмов и существенно ухудшает прогноз [3]. Профилактика инсульта является одной из основных задач лечения таких больных. ХСН – это один из компонентов шкалы CHA2DS2-VASс, поэтому всем пациентам с ФП и ХСН независимо от фракции выброса левого желудочка показано назначение антикоагулянтов. ХСН ассоциирована также с состояниями, которые увеличивают риск кровотечений [4], поэтому на практике важное значение имеет управление рисками тромбоэмболических и геморрагических событий. В соответствии с рекомендациями Европейского общества кардиологов (ESC) 2020 года в первую очередь необходимо не формально оценивать риск кровотечений по шкале HAS-BLED, а выявлять и модифицировать отдельные ФР [5]. При назначении прямых оральных антикоагулянтов (ПОАК) для получения оптимальных результатов лечения важен индивидуальный выбор препарата, а также соблюдение режима его дозирования согласно инструкции по медицинскому применению [6].
Целью исследования было изучение особенностейпопуляции больных с сочетанием ФП и ХСН, структуры ФР тромбоэмболий и кровотечений, в том числепотенциально модифицируемых, предпочтений врачейпри назначении ПОАК и частоты ошибок при их дозировании.
Материал и методы
Ретроспективно были проанализированы истории болезни пациентов с ФП и ХСН, последовательно госпитализированных в центр ХСН (ГКБ им. В.В. Виноградова города Москвы) в 2021-2022 гг. в экстренном или плановом порядке. Из анализа исключали пациентов с клапанной ФП, больных, получавших варфарин, и пациентов, которым при выписке был рекомендован на выбор один из ПОАК, находящихся в обороте на территории Российской Федерации.
Регистрировали клинические и демографические показатели, в том числе пол, возраст, длительность симптомов ХСН, частоту госпитализаций по поводу ХСН, наличие сопутствующих заболеваний, результаты лабораторных и инструментальных исследований. Риск инсульта и системных эмболий оценивали по шкале CHA2DS2-VASc [7], риск кровотечений – по шкале HAS-BLED [8]. Дополнительно определяли частоту назначения определенных ПОАК и особенности соответствующей популяции пациентов, а также корректность выбора дозы ПОАК в соответствии с действующими инструкциями по медицинскому применению (табл. 1) [9-11].
| ПОАК | Критерии снижения дозы |
|---|---|
| Ривароксабан [9] |
Клиренс креатинина <50 мл/мин |
| Апиксабан [10] |
Дозу апиксабана
снижают до 2,5 мг 2 раза/сут у пациентов с клиренсом креатинина <30 мл/мин или при
сочетании двух или более характеристик:
|
| Дабигатран [11] |
Рекомендовано
снижение дозы до 110 мг 2 раза/сут пациентам старше 80 лет Снижение дозы по усмотрению
врача:
|
Для первичной обработки данных использовали методы описательной статистики. Для количественных переменных данные представлены в виде среднего значения ± стандартного отклонения, для качественных – в виде количества наблюдений (%). При оценке межгрупповых различий для количественных переменных использовали t-критерий Стьюдента или однофакторный дисперсионный анализ. С целью определения межгрупповых различий для качественных переменных выполняли построение таблиц сопряженности с последующим расчетом критерия хи-квадрат Пирсона. Различия считали статистически значимыми при уровне p<0,05. Для проведения анализа использовали пакет прикладного программного обеспечения Statistica (версия 10.0).
Результаты
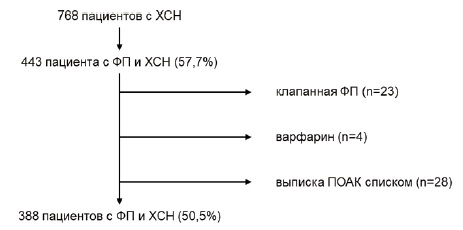
ФП была зарегистрирована у 443 (57,7%) из 768 пациентов с ХСН, госпитализированных в 2021-2022 гг. Из анализа были исключены 23 (5,2%) из 443 пациентов с клапанной ФП, 4 (0,9%) пациента, получавших варфарин, и 28 (6,3%) пациентов, которым при выписке был рекомендован на выбор один из ПОАК, зарегистрированных в Российской Федерации. Таким образом, были отобраны истории болезни 388 пациентов с сочетанием ФП и ХСН, получавших ПОАК (рис. 1). Среди них преобладали люди пожилого возраста, мужчины и пациенты с высокими риском тромбоэмболических осложнений и уровнем коморбидности (табл. 2).
| Параметр | Значение |
|---|---|
| Возраст, лет | 72,4±10,9 |
| Мужской пол, n (%) | 230 (59,3) |
| Индекс массы тела, кг/м2 | 36,2±20,5 |
| СКФ, мл/мин/1,73 м2 | 46,7±16,3 |
| Артериальная гипертония, n (%) | 368 (94,8) |
| Непароксизмальные формы ФП, n (%) | 226 (58,8) |
| CHA2DS2-VASc, баллы | 4,2±1,2 |
| HAS-BLED, баллы | 1,9±0,9 |
| Функциональный класс по NYHA, n (%) | |
| I | 30 (8,7) |
| II | 88 (25,4) |
| III | 166 (50,0) |
| IV | 62 (17,9) |
| Фракция выброса левого желудочка | |
| Средняя, % | 42,9±11,5 |
| ≤40%, n (%) | 162 (41,8) |
| >40%, n (%) | 226 (58,2) |
| Постинфарктный кардиосклероз, n (%) | 146 (37,6) |
| Инсульт в анамнезе, n (%) | 52 (13,4) |
| Сахарный диабет, n (%) | 126 (32,4) |
| Хроническая болезнь почек, n (%) | 292 (75,3) |
| Анемия, n (%) | 196 (50,5) |
| Онкологические заболевания, n (%) | 32 (8,2) |
| ХОБЛ/бронхиальная астма, n (%) | 82 (21,1) |
265 (68,3%) пациентов были госпитализированы экстренно с декомпенсацией ХСН, основными причинами которой были нарушения ритма сердца (n=123; 31,7%), отсутствие приверженности к терапии (n=64; 16,5%), дестабилизация течения артериальной гипертонии (n=49; 12,6%). У 29 (7,4%) пациентов причина неотложной госпитализации не была указана. Остальные больные поступили в стационар в плановом порядке.
Риск венозных тромбоэмболических осложнений по шкале CHA2DS2-VASс у пациентов с неклапанной ФП составил 4,7±1,5 баллов. Помимо ХСН среди факторов риска венозных тромбоэмболий преобладали артериальная гипертония (94,8%) и пожилой возраст (77,1% пациентов были старше 75 лет).
Средний балл по шкале HAS-BLED составил 1,9±0,9, однако высокий риск геморрагических осложнений по шкале HAS-BLED (≥3 баллов) отмечался у каждого четвертого пациента (26,3%). Наиболее распространенными факторами риска кровотечений были возраст старше 65 лет (78,9%) и анемия (50,5%). Распределение факторов риска кровотечений представлено в табл. 3. Важно отметить, что в изучаемой популяции модифицируемые ФР были выявлены у 344 (88,7%) больных.
| Фактор риска | Частота, % |
|---|---|
| Примечание: при оценке данного параметра использовался только критерий "Анемия" | |
| Артериальная гипертония | 9,8 |
| Нарушение функции печени | 16,5 |
| Нарушение функции почек | 3,1 |
| Ранее перенесенный инсульт | 13,4 |
| Предрасположенность к кровотечениям* | 50,5 |
| Лабильное МНО | 0 |
| Пожилой возраст | 78,9 |
| Лекарственные препараты или алкоголь | 21,6 |
Чаще всего пациентам назначали ривароксабан (n=210; 54,1%), реже апиксабан (n=94; 24,2%) и дабигатран (n=84; 21,7%) (табл. 4). Значения расчетной скорости клубочковой фильтрации (СКФ) у пациентов, которым были назначены ривароксабан и апиксабан, были ниже (46,3±16,7 ми 43,1±14,1 мл/мин/1,73 м2, соответственно), чем у пациентов, которым был назначен дабигатран (51,6±16,7 мл/мин/1,73 м2, p<0,05), что, вероятно, связано с ограничениями инструкции по медицинскому применению последнего (клиренс креатинина <30 мл/мин в разделе "Противопоказания") [11]. Дабигатран чаще принимали курящие пациенты и больные с диагнозом хронической обструктивной болезни легких (ХОБЛ). Эти особенности назначения, вероятно, носили случайный характер.
| Параметр | Дабигатран (n=84) | Ривароксабан (n=210) | Апиксабан (n=94) | p |
|---|---|---|---|---|
| Примечание: *Для групп пациентов, получающих ривароксабан и апиксабан, в сравнении с группой дабигатрана. | ||||
| Возраст, лет | 70,8±10,1 | 72,3±11,5 | 74,0±10,0 | нд |
| Мужчины, n (%) | 53 (63,1) | 126 (60,0) | 51 (54,3) | нд |
| Индекс массы тела, кг/м2 | 33,7±7,1 | 33,7±7,7 | 32,0±6,1 | нд |
| СКФ, мл/мин/1,73 м2 | 51,6±16,6 | 46,3±16,7 | 43,1±14,1 | <0,05* |
| Артериальная гипертония, n (%) | 81 (96,4) | 197 (93,8) | 90 (95,7) | нд |
| CHA2DS2-VASc, баллы | 4,2±1,3 | 4,2±1,2 | 4,3±1,0 | нд |
| HAS-BLED, баллы | 2,0±1,0 | 1,9±0,9 | 1,9±0,9 | нд |
| Фракция выброса левого желудочка, % | 41,7±10,6 | 42,9±11,8 | 44,0±11,6 | нд |
| Постинфарктный кардиосклероз, n (%) | 32 (38,1) | 75 (35,7) | 39 (41,5) | нд |
| Инсульт в анамнезе, n (%) | 14 (16,7) | 24 (11,4) | 14 (14,9) | нд |
| Сахарный диабет, n (%) | 26 (31,0) | 66 (31,4) | 34 (36,2) | нд |
| Хроническая болезнь почек, n (%) | 69 (58,0) | 158 (75,2) | 76 (80,9) | нд |
| Анемия, n (%) | 41 (48,8) | 113 (53,8) | 40 (42,6) | нд |
| ХОБЛ/бронхиальная астма, n (%) | 33 (39,3) | 26 (12,4) | 23 (24,5) | <0,001*< /td> |
| Курение, n (%) | 28 (33,3) | 32 (15,2) | 16 (17,0) | 0,002* |
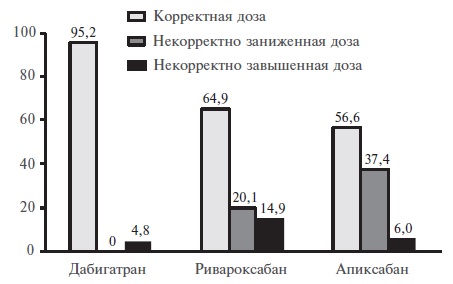
Корректность дозирования оценивали у 341 пациента, у которых в электронную базу данных были внесены все необходимые параметры для анализа. Ошибки при выборе дозы ПОАК встречались у 101 (29,6%) из 341 пациента (рис. 2). Дабигатран, в отличие от ингибиторов фактора Xa, чаще назначали в корректной дозе (95,2% случаев), что, вероятно, связано с менее жесткими критериями выбора дозы. Напротив, некорректное дозирование апиксабана отмечалось в 43,4% случаях от всех его назначений, что может быть обусловлено более сложным алгоритмом, требующим одновременной оценки нескольких параметров (креатинин, клиренс креатинина, возраст, масса тела).
Обсуждение
В настоящее время не вызывает сомнений необходимость организации локальных регистров пациентов с ХСН, сочетающейся с другими заболеваниями, в том числе ФП [12]. В данном одноцентровом исследовании изучались характеристики пациентов с ФП и ХСН, последовательно поступивших в стационар как в экстренном, так и плановом порядке. Сравнение популяции, включенной в анализ, с данными других работ представляет затруднения, поскольку в аналогичных публикациях преимущественно описаны как госпитализированные пациенты, так и больные, находящиеся на амбулаторном наблюдении, с преобладанием последних. В целом клиническая и демографическая характеристика пациентов, участвовавших в нашем исследовании, была сопоставимой с таковой в крупном российском регистре РИФ-ХСН [13]. Так, для больных в обоих исследованиях были характерны пожилой возраст, преобладание непароксизмальных форм ФП, тяжелая ХСН, высокие коморбидность и риск тромбоэмболических осложнений. В нашем исследовании пациенты были старше (средний возраст 72 и 68 лет, соответственно). Кроме того, у них значительно чаще встречалось нарушение функции почек (75,3% и 14,5%, соответственно). Характеристика пациентов, включенных в анализ, была также сопоставимой с таковой в наиболее крупном исследовании с участием госпитализированных больных с ФП и декомпенсацией ХСН – GWTG-HF, что свидетельствует о репрезентативности выборки нашего регистра [14].
По данным регистра GARFIELD-AF (52072 пациента с ХСН, ФП в 22,6% случаев), сочетание ФП и ХСН сопровождается увеличением относительного риска инсульта и системных эмболий на 24% (скорректированное отношение рисков 1,24, 95% доверительный интервал 1,07-1,43, p<0,0001) [15]. При этом наличие ХСН дает один балл по шкале CHA 2DS2-VASc и в соответствии с действующими российскими и европейскими рекомендациями является показанием к антикоагулянтной терапии [5,16]. В нашем исследовании среднее количество баллов по шкале CHA2DS2-VASc составило 4,2±1,2. Однако у пациентов с ХСН часто встречаются состояния, которые сопряжены с увеличением риска кровотечений, что может приводить к необоснованному отказу от назначения антикоагулянтной терапии [4]. В данном контексте важно отметить, что риск кровотечений обычно ниже риска тромбоэмболических осложнений, особенно при высоком количестве баллов по шкале HAS-BLED [17]. В популяции нашего исследования отмечался формально низкий геморрагический риск (среднее количество баллов по шкале HAS-BLED 1,9), однако в 26,3% случаях количество баллов по шкале HAS-BLED было не менее трех. При этом риск кровотечений является динамической величиной. Так, по данным недавно опубликованного ретроспективного исследования у 24490 пациентов с ФП (Тайваньский регистр), через один год наблюдения три и более балла по шкале HAS-BLED регистрировались у 20,9% пациентов с исходно низким геморрагическим риском и почти у 100% пациентов через 15 лет [18]. В структуре впервые выявленных факторов риска кровотечений преобладали артериальная гипертония, инсульт, перенесенное кровотечение и лекарственная терапия. Часть из этих факторов риска являются потенциально модифицируемыми.
В соответствии с российскими и европейскими рекомендациями выявление и коррекция факторов риска кровотечений, наряду с интенсивным динамическим наблюдением, являются неотъемлемым компонентом ведения пациентов с ФП и высоким индексом по шкале HAS-BLED (≥3) [5,16]. Модифицируемые факторы риска часто встречаются в популяции больных с ФП. Так, по данным проспективного исследования XANTUS POOLED, коррекция факторов риска была возможна у 39% пациентов, перенесших большое кровотечение, что свидетельствует о важности профилактических мероприятий [19]. В нашем исследовании коррекция факторов риска была возможной еще чаще – в 88,7% случаев. При оценке структуры факторов риска кровотечений полученные нами данные отчасти согласуются с ранее опубликованными работами (субанализ исследования ARISTOTLE, Тайваньский регистр), в которых наблюдались сопоставимая частота критериев "возраст ≥65 лет" и "ранее перенесенный инсульт". В то же время распространенность неконтролируемой артериальной гипертонии значительно отличалась между нашим исследованием (9,8%), Тайваньским регистром (56,9%) и субанализом исследования ARISTOTLE (3,5%), что, вероятно, связано с особенностями популяции больных, ведение которых осуществлялось в специализированном центре ХСН, в различных лечебных учреждениях и рандомизированном исследовании [18,20]. Обращает на себя внимание, что, в отличие от других работ, в нашей популяции больных гораздо чаще встречались нарушения функции печени и почек, а также анемия, которые могут быть потенциально обратимыми последствиями ХСН и могут уменьшиться при ведении больных в соответствии с клиническими рекомендациями [21,22].
При назначении антикоагулянтной терапии пациентам с ФП врачи могут использовать необоснованно сниженные дозы ПОАК для предотвращения кровотечений, особенно у больных с высоким риском геморрагических осложнений. В действительности такая практика может привести к увеличению количества тромбоэмболических осложнений и госпитализаций [23]. В нашем исследовании частота ошибок при выборе дозы ПОАК составила 29,6%. Чаще всего они отмечались при назначении апиксабана. Полученные данные согласуются с результатами крупного когортного исследования у госпитализированных пациентов с ФП, в котором апиксабан не только чаще других ПОАК использовали в некорректной дозировке на амбулаторном этапе, но также его назначение было сопряжено с наибольшей частотой ошибок дозирования при выписке из стационара, в том числе при попытке коррекции дозы [24]. В трех недавно опубликованных регистрах у амбулаторных пациентов с ФП частота применения корректных дозировок была сопоставимой для отдельных ПОАК, однако при назначении апиксабана чаще наблюдалось использование необоснованно низких доз препарата (14,4-38,5% случаев и 37,3% случаев в нашем исследовании) [25-27]. Нельзя исключить, что полученные результаты, связаны с более сложным алгоритмом подбора дозы апиксабана в соответствии с инструкцией по медицинскому применению [9-11]. Так, при назначении апиксабана следует учитывать четыре критерия (клиренс креатинина, креатинин, возраст, масса тела), а при применении других ПОАК – только по одному (возраст и клиренс креатинина).
Настоящее исследование обладает рядом ограничений, среди которых следует отметить ретроспективный дизайн и сравнительно небольшую популяцию больных. Однако сопоставимость с результатами других работ свидетельствует о валидности полученных данных. Другим ограничением работы является отсутствие информации о ранее перенесенных кровотечениях, включение которой могло бы изменить частоту компонента B (bleeding – кровотечения) шкалы HAS-BLED. Однако учитывая высокую распространенность анемии в нашем исследовании (50,5%) и тот факт, что в исследовании ARISTOTLE частота кровотечений в анамнезе составила 16,7% [20], значительные изменения кумулятивного геморрагического риска в изучаемой популяции представляются маловероятными.
Заключение
Для пациентов с ФП и ХСН характерны высокие коморбидность и риск тромбоэмболических осложнений. Высокий риск кровотечений наблюдается у каждого четвертого пациента. Количество геморрагических осложнений может быть минимизировано за счет коррекции модифицируемых факторов риска (преимущественно анемии – у 50,5% пациентов), которые были широко распространены в изучаемой популяции. Ошибки дозирования ПОАК встречаются почти у каждого третьего пациента с ФП и ХСН (чаще при назначении апиксабана). Чаще всего отмечалось назначение препаратов в необоснованно сниженных дозах.
Используемые источники
- Lippi G, Sanchis-Gomar F, Cervellin G. Global epidemiology of atrial fibrillation: An increasing epidemic and public health challenge. Int J Stroke 2021;16(2):217-21.
- Marini C, De Santis F, Sacco S, et al. Contribution of atrial fibrillation to incidence and outcome of ischemic stroke: results from a population-based study. Stroke 2005;36(6):1115-9.
- Marzlin KM. Atrial fibrillation and heart failure. AACN Adv Crit Care 2020;31(4):431-4.
- Budnik M, Gawałko M, Lodziński P, et al. Heart failure in patients with atrial fibrillation: Insights from Polish part of the EORP-AF general long-term registry. ESC Heart Fail 2023;10(1):637-49.
- Hindricks G, Potpara T, Dagres N, et al. ESC Scientific Document Group. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2021;42(5):373-498.
- Steffel J, Collins R, Antz M, et al. 2021 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Europace 2021;23(10):1612-76.
- Lip GY, Nieuwlaat R, Pisters R, et al. Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factorbased approach: the Euro Heart Survey on atrial fibrillation. Chest 2010;137(2):263-72.
- Pisters R, Lane DA, Nieuwlaat R, et al. A novel user-friendly score (HAS-BLED) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the Euro Heart Survey. Chest 2010;138(5):1093-100..
- Инструкция по медицинскому применению лекарственного препарата Ксарелто® 15/20 мг (ЛП-001457)
- Инструкция по медицинскому применению лекарственного препарата Эликвис® (ЛП-002007)
- Инструкция по медицинскому применению лекарственного препарата Прадакса® (ЛП-000872)
- Filippatos G, Khan SS, Ambrosy AP, et al. International Registry to Assess Medical Practice with Longitudinal Observation for Treatment of Heart Failure (REPORT-HF): rationale for and design of a global registry. Eur J Heart Fail 2015;17(5):527–33.
- Жиров И.В., Сафронова Н.В., Осмоловская Ю.Ф., Терещенко С.Н. Прогностическое значение фибрилляции предсердий у пациентов с сердечной недостаточностью с разной фракцией выброса левого желудочка: результаты многоцентрового регистра РИФ-ХСН. Российский кардиологический журнал 2021;26(1):4200 [Zhirov IV, Safronova NV, Osmolovskaya YuF, Тereschenko SN. Prognostic value of atrial fibrillation in patients with heart failure and different left ventricular ejection fraction: results of the multicenter RIF-CHF register. Russian Journal of Cardiology 2021;26(1):4200 (In Russ.)].
- Mountantonakis SE, Grau-Sepulveda MV, Bhatt DL, et al. Presence of atrial fibrillation is independently associated with adverse outcomes in patients hospitalized with heart failure: an analysis of get with the guidelines-heart failure. Circ Heart Fail 2012;5(2):191-201.
- Ambrosio G, Camm AJ, Bassand JP, et al; GARFIELD-AF Investigators. Characteristics, treatment, and outcomes of newly diagnosed atrial fibrillation patients with heart failure: GARFIELD-AF. ESC Heart Fail 2021;8(2):1139-49.
- Аракелян М.Г., Бокерия Л.А., Васильева Е.Ю. и др.Фибрилляция и трепетание предсердий у взрослых. Клинические рекомендации 2020. Российский кардиологический журнал 2021;26(7):4594 [Arakelyan MG, Bockeria LA, Vasilieva EYu, et al. 2020 Clinical guidelines for Atrial fibrillation and atrial flutter. Russian Journal of Cardiology 2021;26(7):4594 (In Russ.)].
- Friberg L, Rosenqvist M, Lip GY. Net clinical benefit of warfarin in patients with atrial fibrillation: a report from the Swedish atrial fibrillation cohort study. Circulation 2012;125(19):2298-307.
- Chao TF, Chan YH, Chiang CE, et al. Continuation or discontinuation of oral anticoagulants after HAS-BLED scores increase in patients with atrial fibrillation. Clin Res Cardiol 2022 Jan;111(1):23-33.
- Kirchhof P, Haas S, Amarenco P, et al. Impact of modifiable bleeding risk factors on major bleeding in patients with atrial fibrillation anticoagulated with rivaroxaban. J Am Heart Assoc 2020;9(5):e009530.
- Lopes RD, Al-Khatib SM, Wallentin L, et al. Efficacy and safety of apixaban compared with warfarin according to patient risk of stroke and of bleeding in atrial fibrillation: a secondary analysis of a randomised controlled trial. Lancet 2012;380(9855):1749-58.
- McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021;42(36):3599-726.
- Хроническая сердечная недостаточность. Клинические рекомендации 2020. Российский кардиологический журнал 2020;25(11):4083.
- Wu X, Hu L, Liu J, Gu Q. Off-label underdosing or overdosing of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation: A meta-analysis. Front Cardiovasc Med 2021;8:724301.
- Angel Y, Zeltser D, Berliner S, et al. Hospitalization as an opportunity to correct errors in anticoagulant treatment in patients with atrial fibrillation. Br J Clin Pharmacol 2019;85(12):2838-47.
- Giner-Soriano M, Prat-VallverdЬ O, et al. Sex and gender differences in the use of oral anticoagulants for non-valvular atrial fibrillation: A population-based cohort study in primary health care in catalonia. Front Pharmacol 2023;14:1110036.
- Khachatryan A, Doobaree IU, Spentzouris G, et al. Direct oral anticoagulant (DOAC) dosing in patients with non-valvular atrial fibrillation (NVAF) in the United Kingdom: A retrospective cohort study using CPRD Gold Database. Adv Ther 2023;40(2):504-20.
- Díez-Villanueva P, Cosín-Sales J, Roldán-Schilling V, et al. Use of direct acting oral anticoagulants in elderly patients with atrial fibrillation: A multicenter, crosssectional study in Spain. J Clin Med 2023;12(3):1224.
