Оценка фракционного резерва кровотока при эндоваскулярном лечении пациентов с хроническим коронарным синдромом и многососудистым поражением коронарного русла
Изучить влияние оценки фракционного резерва кровотока (ФРК) на выбор стратегии реваскуляризации, основанной на данных ангиографии, и ее отдаленные результаты у пациентов со стабильной ишемической болезнью сердца и многососудистым поражением коронарного русла.
В исследование были включены 163 пациента с хроническим коронарным синдромом и многососудистым поражением коронарного русла. У 45 пациентов основной группы чрескожные коронарные вмешательства выполняли на основании ангиографических данных и ФРК (полная функциональная реваскуляризация), а у 118 пациентов контрольной группы – на основании ангиографической выраженности поражения коронарных артерий (полная анатомическая реваскуляризация). Через 12 мес после вмешательства оценивали суммарную частоту неблагоприятных сердечно-сосудистых событий, включая смерть от всех причин, нефатальный инфаркт миокарда и повторную реваскуляризацию.
У 25 (55,6%) из 46 пациентов основной группы после измерения ФРК была изменена стратегия эндоваскулярного лечения, запланированная на основании результатов ангиографии. У 18 (40,0%) из них стеноз коронарных артерий, выявленный при ангиографии, оказался функционально незначимым, что позволило отказаться от стентирования соответствующей артерии. Непосредственные результаты лечения в основной и контрольной группах были одинаково хорошими, однако среднее количество имплантированных стентов было достоверно ниже в основной группе (1,76±0,57 и 2,29±0,54, р<0,0001). В течение 12 мес после вмешательства суммарная частота неблагоприятных сердечно-сосудистых событий не отличалась между двумя группами.
Определение ФРК у пациентов с хроническим коронарным синдромом и многососудистым поражением коронарного русла более чем в половине случаев привело к изменению запланированной стратегии реваскуляризации миокарда и уменьшению среднего количества имплантированных стентов, что не сопровождалось увеличением частоты основных неблагоприятных сердечно-сосудистых событий в течение 12 мес после вмешательства.
Современные рекомендации по реваскуляризации миокарда у пациентов с хроническим коронарным синдромом основываются на концепции доказанной ишемии миокарда, наличие которой подтверждается результатами пробы с физической нагрузкой на тредмиле или велоэргометре, стресс-эхокардиографии и/или перфузионной сцинтиграфии [1,2] Главным недостатком неинвазивных методов является невозможность выявления региональной ишемии миокарда у пациентов с многососудистым поражением коронарного русла [3].
Для оценки анатомических особенностей коронарных артерий и тяжести их поражения используют коронарографию. Стеноз крупных эпикардиальных артерий более 90% считается гемодинамически значимым и служит показанием к реваскуляризации миокарда. Однако подавляющее большинство поражений, выявляемых при плановой коронароангиографии, находятся в промежуточном диапазоне 40-90%, что требует дополнительных данных для выбора тактики лечения пациента, учитывая высокую вероятность переоценки или недооценки тяжести поражений при ангиографии за счет индивидуальных особенностей пациента или техники исследования. К ним относят выбранный ракурс проекции, наличие бифуркационных поражений, извитость, эксцентричность стеноза, особенности контрастирования и многие другие. Определить поражение коронарных артерий, ответственное за ишемию миокарда, нередко бывает сложным у пациентов, перенесших аортокоронарное шунтирование. Для выявления гемодинамически или функционально значимого коронарного стеноза, вызывающего ишемию миокарда, определяют фракционный резерв кровотока (ФРК) [46]. Применение этого показателя в дополнении к данным ангиографии повышает вероятность правильной оценки стеноза коронарных артерий, требующего коррекции, у пациентов с хроническим коронарным синдромом и многососудистым поражением.
Целью исследования было изучение влияния ФРК на выбор стратегии вмешательства, основанного на данных ангиографии, и его отдаленные результаты у пациентов со стабильной ишемической болезнью сердца и многососудистым поражением коронарного русла.
Материл и методы
В исследование включали пациентов с хроническим коронарным синдромом (стабильная стенокардия напряжения III-IV функционального класса по классификации Канадского общества кардиологов) и многососудистым поражением коронарного русла (наличие стеноза более 40% по крайней мере двух крупных эпикардиальных артерий). Критериями исключения были нестабильная стенокардия, острый инфаркт миокарда и противопоказания к назначению двойной антиагрегантной терапии.
Всем пациентам была выполнена коронарная ангиография по методике Judkins через радиальный доступ. Пациенты были распределены на две группы: в основной группе чрескожные коронарные вмешательства выполняли на основании данных ангиографии и функциональной оценки значимости промежуточных поражений путем измерения ФРК, в контрольной – только на основании ангиографической выраженности поражений. ФРК измеряли после завершения диагностической коронарографии путем селективной катетеризация коронарной артерии проводниковым катетером 6 Fr. Коронарный проводник с датчиком давления позиционировали у кончика проводникового катетера и измеряли давление перед стенозом. Далее коронарный проводник проводили через стенозированный сегмент в дистальное русло артерии и выполняли гиперемическую стимуляцию АТФ в дозе 140 мкг/кг/мин внутривенно. После достижения максимальной гиперемии измеряли давление за стенозом и рассчитывали ФРК как отношение давления дистальнее стеноза к давлению до стеноза. Стеноз считали функционально значимым, если ФРК составлял менее 0,80.
Всем пациентам была проведена полная функциональная или полная анатомическая реваскуляризация миокарда. Под полной функциональной реваскуляризацией понимали отсутствие поражений со значением ФРК менее 0,80 в артериях диаметром ≥2 мм в зоне жизнеспособного миокарда, под полной анатомической реваскуляризацией миокарда – отсутствие поражений ≥70% в артериях диаметром ≥2 мм в зоне жизнеспособного миокарда.
Ангиографическим успехом процедуры считали отсутствие остаточного стеноза или наличие остаточного стеноза в стентированном сегменте менее 10% и кровоток по артерии TIMI-III без признаков диссекций любого типа, дистальной эмболии, окклюзии значимых боковых ветвей и признаков тромбоза в бассейне стентированной артерии. Под клиническим успехом понимали ангиографический успех в сочетании с полным исчезновением проявлений стенокардии напряжения или увеличением толерантности к физической нагрузке не менее чем на два функциональных класса при отсутствии инфаркта миокарда и инсульта во время госпитализации.
Через 12 мес оценивали суммарную частоту неблагоприятных сердечно-сосудистых событий, включая смерть от всех причин, нефатальный инфаркт миокарда и повторную реваскуляризацию.
Статистический анализ проводили с использованием программы MedCalc. Частоту событий сравнивали с помощью критерия Х2.
Результаты
С января 2020 г. по август 2022 г. в исследование были включены 163 пациента с хроническим коронарным синдромом и многососудистым поражением коронарного русла. У 45 пациентов основной группы чрескожные коронарные вмешательства выполняли на основании ангиографических данных и ФРК, а у 118 пациентов контрольной группы – на основании ангиографической выраженности поражения коронарных артерий (табл. 1). Две группы были сопоставимы по демографическим и клиническим показателям, в том числе частоте поражения двух и трех коронарных артерий.
| Показатели | Основная группа (n=45) |
Контрольная группа (n=118) |
p | |
|---|---|---|---|---|
| Возраст, лет | 62,9±9,5 | 62,3±11,8 | 0,76 | |
| Мужчины, n (%) | 35 (77,8) | 81 (68,6) | 0,25 | |
| Курение, n (%) | 28 (62,2) | 77 (65,3) | 0,72 | |
| Ожирение, n (%) | 16 (35,6) | 41 (34,7) | 0,92 | |
| Артериальная гипертония, n (%) | 39 (86,7) | 107 (90,7) | 0,46 | |
| Инфаркт миокарда в анамнезе, n (%) | 14 (31,1) | 34 (28,8) | 0,77 | |
| Реваскуляризация в анамнезе, n (%) | 8 (17,8) | 15 (12,7) | 0,41 | |
| Фракция выброса ЛЖ, % | 55,8±5,8 | 56,2±9,1 | 0,78 |
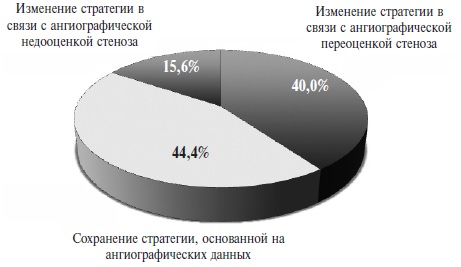
У 25 (55,6%) из 45 пациентов основной группы после определения ФРК была изменена планируемая стратегия эндоваскулярного лечения (рис. 1). У 18 (40,0) пациентов ангиографическая оценка значимости поражения эпикардиальной артерии была завышена, в связи с чем после определения ФРК от выполнения ангиопластики и стентирования соответствующего сосуда было принято решение отказаться. У 7 (15,6%) пациентов степень стеноза, выявленного при ангиографии, составляла 50%, однако ФРК был менее 0,80, в связи чем проведена реваскуляризация миокарда в бассейне данной артерии.
| Показатели | Основная группа (n=45) |
Контрольная группа (n=118) |
p |
|---|---|---|---|
| Количество пораженных сосудов, n (%) |
0,48 | ||
| Два | 32 (71,1) | 77 (65,3) | |
| Три | 13 (28,9) | 41 (34,7) | |
| Полная анатомическая/ функциональная реваскуляризация миокарда,n (%) |
45 (100) | 118 (100) | >0,05 |
| Количество стентов на пациента | 1,76±0,57 | 2,29±0,54 | <0,0001 |
| Ангиографический успех, n (%) | 45 (100) | 118 (100) | >0,05 |
| Клинический успех, n (%) | 45 (100) | 117 (99,2) | 0,54 |
Ангиографический успех в двух группах был достигнут у всех пациентов, а клинический – у всех пациентов основной группы и 117 (99,2%) из 118 пациентов контрольной группы (табл. 2). У одного пациента отмечалось повышение кардиоспецифических ферментов в раннем послеоперационном периоде в связи с закрытием мелкой ветви тупого края (менее 2 мм) при ангиопластике и стентировании огибающей артерии. В основной группе среднее количество имплантированных стентов на пациента было значительно меньше, чем в контрольной группе (1,76±0,57 и 2,29±0,54, соответственно; р<0,0001).
| Событие | Основная группа (n=45) |
Контрольная группа (n=118) |
Относительный риск (95% доверительный интервал) |
p |
|---|---|---|---|---|
| Смерть, инфаркт миокарда или повторная реваскуляризация | 2 (4,4) | 5 (4,2) | 1,05 (0,19-5,62) | 0,95 |
| Смерть | 0 | 0 | - | - |
| Нефатальный инфаркт миокарда | 1 (2,2) | 2 (1,7) | 1,31 (0,12-14,90) | 0,82 |
| Повторная реваскуляризация | 1 (2,2) | 3 (2,5) | 0,87 (0,09-8,60) | 0,91 |
Суммарная частота и частота отдельных основных сердечно-сосудистых событий в течение 12 мес между группами не отличалась (табл. 3).
Обсуждение
Широкое внедрение инвазивных методов лечения ишемической болезни сердца, несомненно, является одним из ключевых достижений современной кардиологии. Коронароангиография остается золотым стандартом визуализации коронарных артерий, хотя, как указано выше, этот метод имеет ограничения. В нашем исследование более чем в половине случаев после измерения ФРК была изменена стратегия эндоваскулярного лечения, которую планировали на основании ангиографической оценки поражения коронарного русла. В 40% случаев выявленный промежуточный стеноз коронарных артерий (в диапазоне 70-90%) оказался функционально незначимым, что позволило не проводить пластику и стентирование соответствующих артерий и достоверно уменьшить среднее количество имплантированных стентов на пациента.
В крупном исследовании ISCHEMIA реваскуляризация миокарда у пациентов с хронической ИБС вызывала более выраженное улучшение качества жизни по сравнению с оптимальной медикаментозной терапией, в то время как частота основных неблагоприятных сердечно-сосудистых событий была сходной в группах сравнения [12]. Определение ФРК при лечении пациентов со стабильной стенокардией и многососудистым поражением коронарного русла позволяет уточнить показания к реваскуляризации миокарда и уменьшить количество имплантированных стентов без увеличения частоты больших кардиальных событий. Уменьшение протяженности стентированного участка, которая является "механическим" предиктором развития рестеноза, при более длительном периоде наблюдения может привести к снижению частоты повторных вмешательств на коронарных артериях.
Заключение
Определение ФРК при лечении пациентов с хроническим коронарным синдромом и многососудистым поражением коронарного русла в 55,6% случаев привело к изменению стратегии реваскуляризации миокарда, запланированной на основании результатов ангиографии, и уменьшению среднего количества имплантированных стентов на пациента. Изменение стратегии инвазивного лечения не сопровождалось увеличением частоты основных неблагоприятных сердечно-сосудистых событий в течение 12 мес после вмешательства.
Используемые источники
- Knuuti J, Wijns W, Saraste A, et al; ESC Scientific Document Group. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 2020;41(3):407-77.
- Lawton J, Tamis-Holland J, Bangalore S, et al. 2021 ACC/AHA/SCAI Guideline for Coronary Artery Revascularization. J Am Coll Cardiol 2022;79(2)e21–129.
- Knuuti J, Ballo H, Juarez-Orozco LE, et al. The performance of non-invasive tests to rule-in and rule-out significant coronary artery stenosis in patients with stable angina: a meta-analysis focused on post-test disease probability. Eur Heart J 2018;39(35):3322-30.
- Алекян Б.Г., Карапетян Н.Г., Мелешенко Н.Н., Ревишвили А.Ш. Эффективность применения показателя моментального резерва коронарного кровотока в оптимизации реваскуляризации миокарда. Эндоваскулярная хирургия 2020;7(3):218–27 [Alekyan BG, Karapetyan NG, Meleshenko NN, Revishvili ASh. Efficiency of application of the indicator of instantaneous wavefree ratio in optimizing myocardial revascularization. Russian Journal of Endovascular Surgery 2020;7(3):218–27 (in Russ.)].
- Максимкин Д.А., Боливоги Ж.М., Файбушевич А.Г. и др. Роль внутрисосудистых методов исследования коронарных артерий при отборе пациентов с диффузным и многососудистым поражением для реваскуляризации миокарда. Инновационная медицина Кубани 2021;(4):5-12 [Maximkin DA, Bolivogu JM, Faybushevich AG, et al. The role of intravascular methods of examination of coronary arteries in the selection of patients with diffuse and multivessel lesions for myocardial revascularization. Innovative Medicine of Kuban 2021;(4):5-12 (In Russ.)].
- Демин В.В., Бабунашвили А.М., Шугушев З.Х. и др. Российский регистр по использованию внутрисосудистых методов визуализации и физиологии: итоги первого года. Журнал Диагностическая и интервенционная радиология 2022;16(3);27-39 [Demin VV, Babunashvili AM, Shugushev ZKh, et al. The Russian registy of the use of intravascular methods of imaging and physiology: the first year results. Journal of diagnostic and interventional radiology 2022;16(3);27-39 (In Russ.)].
- Zimmermann FM, Ferrara A, Johnson NP, et al. Deferral vs. performance of percutaneous coronary intervention of functionally non-significant coronary stenosis: 15-year follow-up of the DEFER trial. Eur Heart J 2015;36(45):3182-8.
- Tonino PA, De Bruyne B, Pijls NH, et al; FAME Study Investigators. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention. N Engl J Med 2009;360(3):213-24.
- Van Nunen LX, Zimmermann FM, Tonino PA, et al. Fractional flow reserve versus angiography for guidance of PCI in patients with multivessel coronary artery disease (FAME): 5-year follow-up of a randomised controlled trial. Lancet 2015;386(10006):1853–60..
- Xaplanteris P, Fournier S, Pijls NHJ, et al; FAME 2 Investigators. Five-year outcomes with PCI guided by fractional flow reserve. N Engl J Med 2018;379:250-9.
- Härle T, Zeymer U, Hochadel M, et al. Real-world use of fractional flow reserve in Germany: results of the prospective ALKK coronary angiography and PCI registry. Clin Res Cardiol 2017;106(2):140–50.
- Mavromatis K, Jones P, Ali Z, et al. Complete revascularization and angina-related health status in the ISCHEMIA Trial. J Am Coll Cardiol 2023;82(4):295–313.
