COVID-19 и клиническая фармакология
В статье рассматривается роль клинической фармакологии в управлении пандемией COVID-19, в частности разработке лекарственных средств, оказывающих действие на коронавирусную инфекцию. Предлагаются различные стратегии и горизонты изучения данной инфекции и анализируются отдельные группы лекарств. Подробно обсуждаются текущие клинические исследования при COVID-19, основные тренды, проблемы и задачи, стоящие перед клинической фармакологией, роль клинических рекомендаций. Приведены результаты применения различных лекарственных средств в реальной клинической практике и рассматриваются основные направления работы врача клинического фармаколога и дисциплины в целом при коронавирусной инфекции.
Долгие годы коронавирус (CoV), открытый в 1960 г. D. Tyrrell, а затем описанный J. Almeida и соавт. в Nature в 1968 г., был лишь причиной острых респираторных инфекций легкого течения [1,2]. В связи с этим не было оснований для выделения человеческих и финансовых ресурсов с целью разработки этиотропной терапии коронавирусной инфекции. Если проанализировать клинические рекомендации 2018 г. по лечению простуды у детей и взрослых, все предлагаемые симптоматические средства имели крайне низкую доказательную базу, а некоторые рассматривались как нежелательные или даже опасные, например, антибиотики у взрослых или блокаторы H1-гистаминовых рецепторов у детей, соответственно [3,4]. Лекарственные средства, оказывающие действие на CoV, в этих рекомендациях отсутствовали, однако пандемия COVID-19 (COronaVIrus Disease 2019) изменила такое снисходительное отношение к коронавирусам.
Научно-исследовательские работы в области лекарственных средств
Философия создания лекарственных средств формировалась на протяжении предыдущего столетия. В основном это была реакция фармацевтической индустрии на основные вехи социально-экономического развития человечества и в чем-то системы здравоохранения (рис. 1). С целью стандартизации процесса изучения лекарственных средств в 80-е гг. прошлого столетия была предложена GCP (Good Clinical Practice, Надлежащая клиническая практика). Для разработки большинства лекарственных средств (от малых молекул до генно-инженерных биологических препаратов), включая лабораторные, доклинические и клинические исследования, и одобрения их клинического применения требуется от 8 до 10 лет [6,7]. Одним из самых длительных процессов являются клинические исследования, которые проводятся в четыре фазы и позволяют оценить действенность (efficacy) лекарственного препарата. На основании этих данных производится его регистрация регулирующими органами [8]. Как правило, действенность изучается в рандомизированных клинических исследованиях (РКИ), которые предполагают строгое выполнение утвержденного протокола исследования, соблюдение принципов GCP и высокую приверженность к лечению. Результаты таких исследований публикуются в научных журналах и доступны для медицинской общественности. Медицина, основанная на доказательствах, преимущественно, но не только, оперирует действенностью, однако на основании результатов клинических исследований нельзя в полной мере судить об эффективности лекарственного средства в общей популяции больных, в том числе в разных странах (даже в разных медицинских организациях) и разных группах, отличающихся по полу, возрасту, функции печени и почек, наличию сопутствующих заболеваний и сопутствующей терапии и т.д. [6]. Для подтверждения эффективности (effectiveness) проводят дополнительные обсервационные исследования в условиях реальной клинической практики – real world data (RWD) [9].
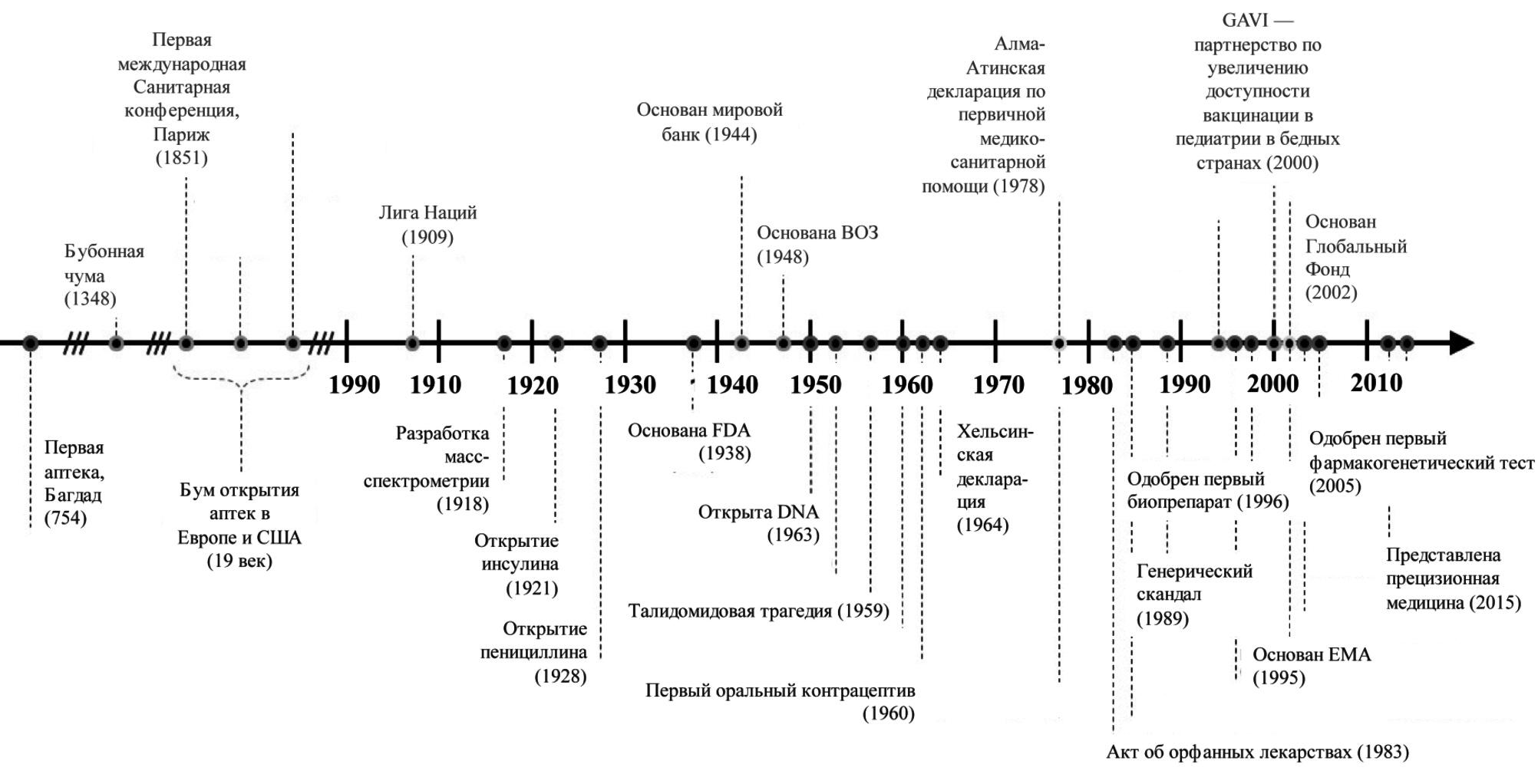
Стратегии изучения лекарственных средств для лечения COVID-19
Пандемии COVID-19 предшествовали вспышки тяжелого острого респираторного синдрома (Severe acute respiratory syndrome, SARS) и ближневосточного респираторного синдрома (Middle East respiratory syndrome, MERS), которые были зафиксированы в Китае (2003 г.) и Саудовской Аравии (2012 г.), соответственно. Поиск противовирусных препаратов показал, что многочисленные химические соединения могут влиять на проникновение и/или репликацию CoV в клеточной культуре [10,11]. Был накоплен и небольшой клинический опыт применения различных лекарств, в том числе рибавирина, интерферона альфа, метилпреднизолона, лопинавира/ритонавира, а также реконвалесцентной плазма и комбинации этих средств в той или иной последовательности [12]. Одновременно были предложены стратегии разработки эффективных и безопасных лекарственных средств для лечения и профилактики CoV инфекции. Первая – продолжение тестирования уже зарегистрированных противовирусных препаратов, активность которых в отношении РНК-вирусов была показана ранее в клинических исследованиях разного качества и дизайна: интерферон альфа (вирус гепатита С), рибавирин (вирус гепатита С, респираторно-синцитиальный вирус, возбудитель геморрагической лихорадки), лопинавир/ритонавир (ВИЧ), фавипиравир (вирус гриппа). Вторая – использование существующих молекулярных баз данных для скрининга молекул с различным механизмом действия, которые могут оказывать действие на коронавирус: хлорохин и гидроксихлорохин, ремдесивир. Третья стратегия предполагает целевую разработку новых противовирусных препаратов на основе изучения геномной информации и патогенных свойств различных коронавирусов [12]. Однако интенсивные научные исследования с выделением значимых финансовых и человеческих ресурсов проведены не были. Причины такого пассивного поведения будут, наверное, изучены в будущем.
Гортизонты разработки лекарственных средств для лечения COVID-19
31 декабря 2019 г. городская комиссия по здравоохранению г. Ухань (Китай) зарегистрировала несколько случаев пневмонии неизвестной этиологии, а в июне 2020 г. число случаев инфекции, вызванной SARS-CoV-2, практически во всех странах мира превысило 11 млн [13]. Выделяют три горизонта для разработки методов лечения и профилактики COVID-19, которые включают в себя не только этиотропное действие на CoV, но и лечение острого респираторного дистресс-синдрома (ОРДС), синдрома высвобождения цитокинов, или цитокинового шторма (cytokine release syndrome, CRS), сопутствующих бактериальных и грибковых инфекции [14]. Первый краткосрочный горизонт (недели – месяцы) – перепрофилирование существующих (зарегистрированных) лекарственных средств. Совпадает с первой и второй стратегиями, предложенными в 2016 г. A. Zumla и соавт. после вспышек SARS и MERS [12]. Среднесрочный горизонт (месяцы – годы) – это прежде всего создание вакцин. И, наконец, долгосрочный горизонт (годы) – разработка инновационных лекарственных веществ, обладающих новыми механизмами действия (третья стратегия, описанная выше) [14].
По данным международного реестра клинических исследований COVID-19 (Global Coronavirus COVID-19 Clinical Trial Tracker), который объединяет базы китайского реестра клинических испытаний, Сlinical-Trials.gov, информационной службы клинических исследований Республики Корея, регистра клинических испытаний Евросоюза, базы Всемирной организации здравоохранения (ВОЗ) – ISRCTN, иранского реестра клинических испытаний, сеть первичных реестров Японии, немецкий регистр клинических испытаний, данные Роздравнадзора РФ, на 20 июня 2020 г. в мире проводятся или планируются 1457 клинических исследований у пациентов с COVID-19 (табл. 1). Большинство исследований относятся к первом горизонту, т.е. первой и второй стратегиям, и предполагают попытку перепрофилирования уже известных лекарственных средств для лечения COVID-19. Долгосрочный горизонт на этапах клинических исследований не обнаружен.
| Горизонт 1 (зарегистрированные показания), кол-во исследований (первая/вторая стратегии) | Горизонт 2, кол-во исследований | Горизонт 3 (третья стратегия) |
|---|---|---|
| Примечание: В таблице указаны первые 10 исследуемых лекарственных средств. 1Тофацитиниб, барицитиниб, 2руксолитиниб; CAR-T - клеточная терапия через T-клетки с химерным антигенным рецептором; *можно отнести клинические исследования моноклональных антител к CoV | ||
|
Гидроксихлорохин и хлорохин (малярия; системная красная волчанка; ревматоидный артрит), n=272 Лопинавир/ритонавир (ВИЧ), n=83 Азитромицин (бактериальные инфекции), n=73 Тоцилизумаб (ревматоидный артрит; цитокиновый шторм после CAR-T терапии), n=51 Интерферон альфа или бета, n=51 Кортикостероиды (множество показаний), n = 45 Фавипиравир (грипп), n=35 Витамины, n=30 Антикоагулянты, n=27 Ингибиторы янус-киназ (ревматоидный артрит 1 ; миелофиброз 2 ), n=24 Другие лекарственные средства, n=796 Всего n=1457 |
Вакцины, n=49 | Не ясно* |
Фармакодинамические подходы к лечению COVID-19 можно разделить на несколько категорий (рис. 2). В 272 клинических исследованиях более чем в 400 центрах изучаются противомалярийные препараты (гидроксихлорохин или хлорохин). В основном эти исследования проводятся в США (n=112), Иране (n=46) и Испании (n=46). Завершено только 16 из них, а результаты 3 исследований опубликованы. В 308 клинических центрах проводится набор пациентов, а в 111 – он еще не начат. Многие исследования являются рандомизированными, в основном у пациентов с подтвержденным COVID-19. Необходимо отметить, что в марте 2020 г. было начато международное рандомизированное клиническое исследование SOLIDARITY, организованное ВОЗ, в котором планировалось изучение хлорохина и гидроксихлорохина, а также лопинавира/ритонавира и интерферона бета. Врачи, участвующие в этом исследовании, должны сообщать о том, какие лекарственные препараты доступны в конкретной больнице, а затем на веб-сайте ВОЗ производится рандомизация пациента в одну из соответствующих групп. Национальные исследования противомалярийных препаратов были также начаты в Великобритании (RECOVERY), США (СТАР), Франции (DISCOVERY) [17-19]. Механизмы возможного эффекта противомалярийных средств на CoV остаются до конца неясными (рис. 2): взаимодействие, опосредованное эндосомами (нарушение созревание лизосом), ингибирование гликозилирования гликопротеинов мембраны челове ческой клетки или подавление продукции фактора некроза опухоли альфа стимулированными моноцитами/макрофагами [20,21].
Далее по числу проводимых клинических исследований следуют ингибиторы протеазы – лопинавир/ритонавир (n=83). Этот комбинированный препарат стал одним из первых средств, которые рекомендовали для лечения COVID-19 [21,22]. Завершено только 12 клинических исследований (результаты 3 из них опубликованы), в 52 исследованиях продолжается набор пациентов, а в 16 – он еще не начат. К ингибиторам протеазы относится также дарунавир, который изучается по крайней мере в одном клиническом исследованием.
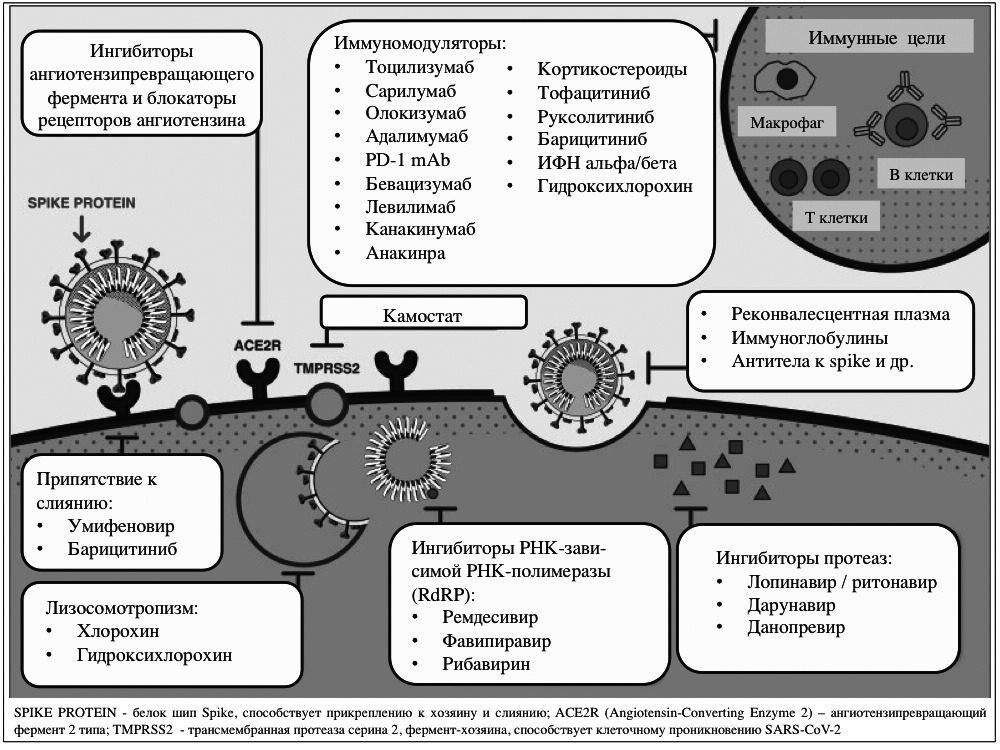
Третьей, наиболее изучаемой группой лекарственных средств, являются различные иммуномодуляторы, обладающие противовоспалительной активностью, в том числе глюкокортикостероиды, моноклональные антитела, блокирующие эффекты интерлейкина (ИЛ)-6 (тоцилизумаб, сарилумаб, олокизумаб) и ИЛ-1 (анакинра, канакинумаб), и ингибиторы янус-киназ (барицитиниб, тофацитиниб, руксолитиниб). Среди перечисленных препаратов следует прежде всего выделить тоцилизумаб (55 клинических исследований), метилпреднизолон (39) и три ингибитора янус-киназ (31). Цель применения указанных лекарственных средств – подавление синдрома высвобождения цитокинов, или цитокинового шторма, который считают одной из ведущих причин тяжелого поражения легких при COVID-19. Ранее этот синдром, ведущую роль в патогенезе которого играет ИЛ-6, был описан при лечении острого лимфобластного лейкоза CAR-T (chimeric antigen receptor) [23], а также некоторых других состояниях. Единственным зарегистрированным лекарственным средством для лечения синдрома высвобождения цитокинов является тоцилизумаб. К июню 2020 были завершены только два клинических исследования тоцилизумаба, а в 41 – продолжается набор пациентов. В многочисленных клинических исследованиях изучаются также глюкокортикоиды, которые оказывают действие на все фазы воспаления – от стабилизации мембран лизосом до угнетения продукции ИЛ (результаты 5 исследования опубликованы) [1,2].
Четвертой группой наиболее активно изучаемых лекарственных средств являются ингибиторы РНКзависимой РНК-полимеразы фавипиравир (37 исследований) и ремдесивир (19). Первый первоначально был разработан для лечения гриппа, а второй – лихорадки, вызванной вирусом Эбола. Механизм действия этих лекарственных средств теоретически позиционирует их как препараты широкого спектра, которые могут обладать активностью в отношении любых РНК-вирусов [21]. К июню 2020 г. были завершены только 1 клиническое исследование ремдесивира (в 11 продолжается набор пациентов) и 3 исследования фавипиравира (в 21 продолжается набор пациентов).
Представители других групп лекарственных средств изучаются в единичных исследованиях. Так, существует высокий интерес к ингибиторам ангиотензипревращающего фермента и блокаторам рецепторов ангиотензина II [24]. Необходимо отметить белок приманку (рекомбинантный человеческий ангиотензинпревращающий фермент 2) ACE2 APN01, разработка которого была начата после вспышки SARS-CoV в 2003 году [25]. Еще одна группа лекарственных веществ – это низкомолекулярные лиганды, вызывающие конформационные изменения ACE2 (ангиотензинпревращающего фермента 2, открытого в 2000 году) [26]. Выделяют около 10 лекарственных средств, которые могут проявлять подобную активность, например, хлорпротиксен. Известно, что CoV использует человеческий рецептор ACE2 для доступа в клетки человека при участии сериновой протеазы TMPRSS2, поэтому блокада взаимодействия между ACE2 и spike-белком вируса может препятствовать развитию вирусной инфекции. Мощ ны ми ингибиторами TMPRSS2 являются камостат и нафамостат [27].
Безусловно, нейтрализующие моноклональные антитела к CoV имеют потенциал как для терапевтического, так и профилактического применения и могут помочь при разработке вакцин. Моноклональные антитела для COVID19 готовят из В-клеток пациентов, которые восстановились после заболевания, а также производят гибридомным методом [28]. В Китае завершено клиническое исследование (NCT04275245) меплазумаба, блокирующего белковый рецептор хозяина (CD147), который способствует проникновению вируса в клетки [29].
Изучение действенности (efficacy) лекарственных средств при COVID-19
Распространение COVID-19 сопровождается беспрецедентным увеличением числа клинических исследований лекарственных средств для лечения инфекции. Например, с марта 2020 г. регистрировали до 160 клинических исследований в неделю (рис. 3). Большинство исследований проводились или проводятся в Китае, Западной Европе и США, в то время как на долю Российской Федерации в июне 2020 г. приходилось только 1% исследований. Всего в мире в клинические исследования при COVID-19 вовлечено более 110000 человек. По фазам клинические исследования в марте 2020 г. распределялись следующим образом: I фаза – 9,1% исследований, II – 34,9%, III – 27,2%, IV – 7,1%, нельзя классифицировать – 21,7%. К июню 2020 г. тренд остался тем же: I фаза – 5,8%, II – 26,7%, III – 17,5%, IV – 4,4%, нельзя классифицировать – 45,6% [22].
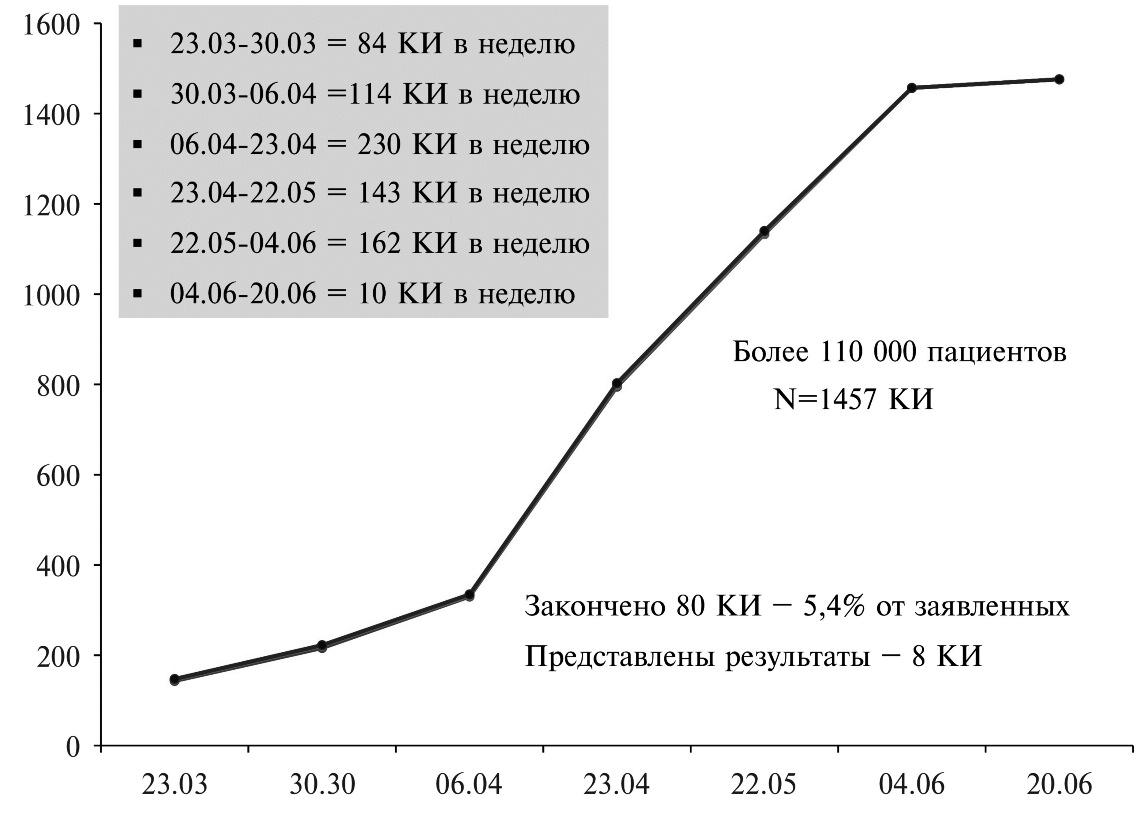
За 6 месяцев произошло постепенное смещение тренда от сравнения одного лекарства с плацебо к сравнению нескольких лекарственных средств друг с другом. Большинство исследований (от 63% до 71%) представляют собой интервенционные клинические испытания, хотя проводятся и обсервационные исследования, в которых изучается эффективность (effectiveness). Конечными точками клинических исследований являются выздоровление, облегчение течения заболевания (оценка симптомов, таких как лихорадка, кашель, диарея, миалгия, одышка, в баллах), отсутствие нарастания одышки, частота и длительность искусственной вентиляции легких, перевода в отделение интенсивной терапии и т.д. При проведении клинических исследований у пациентов с COVID-19 были отмечены существенные и практически непреодолимые пока проблемы [30].
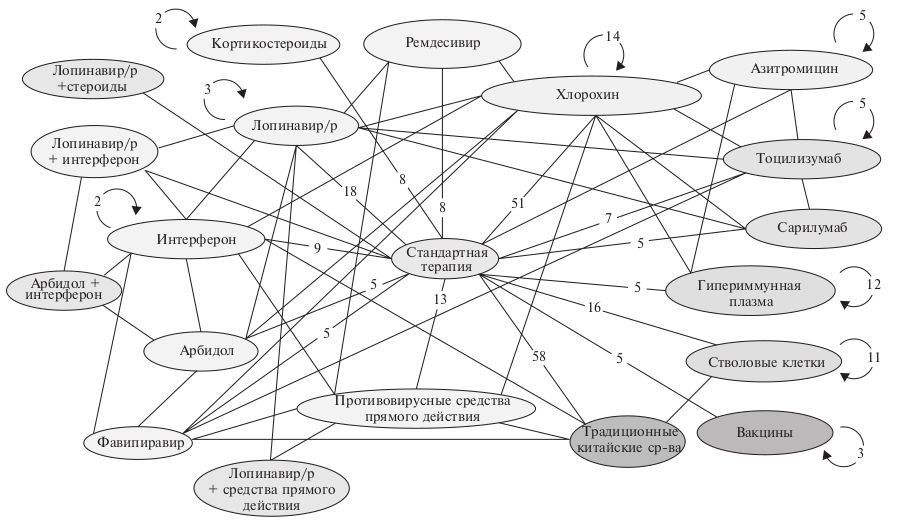
Во-первых, во многих исследованиях изучаемые препараты применяются в сочетании с многочисленными другими средствами (рис. 4). При этом количество включенных больных часто ограниченное, что не позволяет провести адекватный вторичный анализ в подгруппах.
Во-вторых, дизайн части текущих исследований был разработан до появления информации о патогенезе COVID-19, многие аспекты которого до сих пор остаются неясными. Так, возможно, что противовирусные препараты могут быть эффективными на ранних этапах развития вирусной инфекции, в то время как при тяжелом течении SARS-CoV-2 пневмонии, осложнившейся ОРДС, большие надежды возлагают на иммуномодуляторы, подавляющие воспалительный каскад. Более того, хотя в некоторых исследованиях удавалось сократить продолжительность искусственной вентиляции легких или длительность пребывания в стационаре, полученные данные не позволяют сделать вывод о том, что использованные лекарственные средства "излечивают" COVID-19.
В-третьих, в клинических исследованиях у пациентов с COVID-19 нередко оценивают сроки устранения симптомов, улучшения лабораторных показателей или рентгенологических изменений или частоту использования искусственной вентиляции легких. Лишь немногие исследования будут достаточно мощными для того, чтобы установить разницу в летальности между группами сравнения, в то время как интерпретация таких результатов, как разрешение симптомов, может быть проблематичной [30].
С целью изменить такой негативный тренд в мае 2020 г. Американская администрация по контролю за пищевыми продуктами и лекарствами (FDA) предложила оценивать в клинических исследованиях III фазы следующие клинические исходы: летальность от всех причин в течение не менее 28 дней, дыхательная недостаточность, в том числе необходимость в кислоротерапии, неинвазивной вентиляции легких, искусственной вентиляции легких, экстракорпоральной мембранной оксигенации, перевод в отделение реанимации и интенсивной терапии, необходимость госпитализации на основании четких показаний, устойчивое клиническое выздоровление (например, устранение симптомов). Изучение элиминация вируса с помощью полимеразной цепной реакции (ПЦР) целесообразно только в клинических исследованиях II фазы [32].
Изучение эффективности лекарственных средств в реальной клинической практике
На фоне активного изучения действенности лекарственных средств в лечении COVID-19 в предрегистрационных клинических исследованиях параллельно во всем мире выпускаются клинические (в Российской Федерации методические) рекомендации или руководства. Данные документы случат источником информации, необходимой для принятия решений в обычной клинической практике. Если в клинических исследованиях в мире принимают участие более 100 тыс пациентов, то на практике те же лекарства получали или получают миллионы людей. Однако неясно, как часто их эффекты мониторируются и анализируются исследователями. Пока опубликованные исследования вызывали большое количество вопросов и трактовались экспертами, как правило, негативно [33].
16 января 2020 года Национальная комиссия здравоохранения Китая (National Health Commission, NHC) выпустила первый из 7 протоколов диагностики и лечения COVID-19 [34,35]. Позднее были опубликованы рекомендации ВОЗ [33]. 29 января была разработана первая версия российских временных методических рекомендаций [37]. В качестве противовирусных средств сразу были предложены ингаляции интерферона-α2b, лопинавир/ритонавир, рибавирин, хлорохин/ гидроксихлорохин и умифеновир, т.е. активно стали использовать первую стратегию – перепрофилирование лекарств с другими показаниями [34]. В первых рекомендациях фигурировали также метилпреднизолон, реконвалесцентная плазма, внутривенное введение иммуноглобулинов и тоцилизумаба. В последующем в различные клинические рекомендации в разных странах мира стали включать многочисленные лекарственные средства – от ремдесивира и фавипиравира до силденафила и талидомида [38,39]. Однако эти рекомендации основывались на результатах единичных клинических исследований низкого качества, в которых принимало участие небольшое количество пациентов. В лучшем случае их результаты можно было считать генерирующими гипотезы. Соответственно, любая терапия COVID-19, указанная в клинических или методических рекомендаций, фактически остается исследуемой [22]. В данном контексте необходимо привести позицию Центрa по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention, CDC), который призвал к незамедлительным действиям в первом руководство для врачей по лечению COVID-19 [40]. Такой же позиции придерживались и регуляторные органы в других странах мира. Соответственно, список лекарственных средств, в том числе не зарегистрированных в конкретной стране, которые применяются для лечения COVID-19 off-label, т.е. по неодобренным показаниям, постоянно увеличивается. Широкие применение различных препаратов было отмечено не только в стационарах, прежде всего у пациентов с тяжелым течением заболевания, но и в амбулаторной практике [36].
Роль клинической фармакологии при COVID-19
Традиционно, клиническая фармакология оперирует таким тезисом, как "правильное лекарство в необходимой дозе для конкретного пациента" [41]. Однако в контексте пандемии COVID-19 необходимо добавить и "как можно скорее". Стремительное распространение инфекции диктует потребность в лекарственных средствах, способных как минимум прекратить передачу SARS-CoV-2 от человека к человеку, а у госпитализированных пациентов, особенно находящихся в ОРИТ, – предупредить развитие ОРДС и присоединения госпитальной бактериальной и грибковой инфекции и нормализовать показатели свертывающей системы крови.
В арсенале клинических фармакологов имеются обширные знания о различных аспектах применения лекарственных средств [14], в том числе фармакокинетике лекарств в особых группах, роли таких факторов, как возраст, пол, функция почек и печени, лекарственном взаимодействии, фармакогеномике, связи между фармакокинетикой и фармакодинамическим ответом, фармаконадзоре [42]. Результаты изучения потенциально эффективных методов лечения COVID-19 могут быть интегрированы в количественные фармакологические модели, которые, в свою очередь, могут быть использованы для моделирования и оптимизации дизайна клинических исследований, включая выбор биомаркеров, а также дозирования лекарственных средств у пациентов. Так, M.Garcia-Cremades и соавт. на основании полученных ранее и появляющихся доклинических и клинических данных о фармакокинетике, противовирусной активности и безопасности аминохинолиновых производных разработали модель дозирования гидроксихлорохина у пациентов с COVID19 [43]. По мнению авторов, их исследование имеет очевидные ограничения, связанные с тем, что на момент публикации доказательства действенности гидроксихлорохина при SARS-CoV-2 инфекции отсутствовали. Тем не менее, использование моделей позволяет интегрировать всю доступную информацию из различных источников, делает все допущения прозрачными и обеспечивает основу для количественной оценки неопределенности [14].
В некоторых странах пандемия привлекла внимание научного сообщества к исследованиям, которые уже давно входят в сферу интересов клинической фармакологии. Например, во всем мире клинических фармакологов считают лидерами в использовании байесовских методов и анализе данных реальной клинической практики (Real world evidence, RWE) [44,45]. Действительно, последние все чаще используются при принятии решений в системе здравоохранения [46,47]. В недавно опубликованном комментарии европейских регулирующих органов отмечена необходимость в изучении эффективности и безопасности лекарственных средств на основе данных, полученных в обычной клинической практике, а также указано, как сделать их приемлемыми для регулирующих органов [48]. Именно при изучении данных реальной клинической практики могут быть выделены биомаркеры и "суррогатные" конечные точки, которые крайне необходимы для разработки методов лечения новой инфекции [49,50].
Фармакогеномика – важная область клинической фармакологии. Примерами ресурсов, которые позволяют внедрять достижения фармакогеномики в систему здравоохранения, могут служить Pharmacogene Variation Consortium (PharmVar) [51], База знаний по фармакогеномике (PharmGKB) [52], Консорциум по реализации клинической фармакогенетики (CPIC) [53]. В Рос сий ской Федерации с 2015 г. издается журнал "Фармако генетика и фармакогеномика", который является официальным печатным органом Общества фармакогенетики, фармакокинетики и персонализированной терапии [54]. Необходимо отметить, что на сайте PharmGKB создана страница, ориентированная на COVID-19, где размещена информация о терапевтических вариантах лечения, опираясь на данные фармакогенетики [55]. Конечно, необходимо указать, что эксперты в области клинической фармакологии во всем мире активно создают информационные ресурсы по CОVID-19. В нашей стране примером может служить Информационный центр по вопросам фармакотерапии у пациентов с новой коронавирусной инфекцией "ФармаCOVID" на базе РМАНПО Минздрава России [56].
Обсуждение
20 января 2020 года Национальная служба здравоохранения Китая отнесла новую коронавирусную инфекцию к самому высокому уровню опасности – классу А инфекционных заболеваний [34]. 11 марта T. Gheb rey esus, генеральный директор ВОЗ, заявил, что ситуацию с распространением COVID-19 можно охарактеризовать как пандемию [13]. Коронавирусные инфекции были известны давно (с середины 60-х гг.), но долгое время оставались вне поля интересов фармакологов и представителей фармацевтической индустрии [1,2]. Даже тяжелые инфекции, сопровождающиеся развитием острого респираторного синдрома, такие как SARS и MERS, не изменили такого отношения к коронавирусам. Частично это связано с тем, что инфекции были локализованы в странах Юго-Восточной Азии и Ближнего востока и не затронули страны с высоким индексом человеческого развития (Human Development Index, HDI). Вероятно, полагали, что коронаровирусные инфекции в виде генерализованных форм не выйдут за границы этих стран.
Если рассматривать историю философии создания лекарств, безусловно, на данной хронологической карте скоро появится новая точка, обусловленная пандемией 2019-2020 г. При этом COVID-19 не просто останется в истории, инфекция изменила всю парадигму исследования лекарственных веществ. По мнению P. der Graaf и соавт., разработка лекарств для лечения COVID-19 находится на принципиально иной временной шкале [14]. Однако к июню 2020 г. почти все клинические исследования предполагали перепрофилирование уже известных лекарственных средств, хотя, как показали J. Magagnoli и соавт., такой подход скорее всего будет неэффективным, и к нему следует относиться критически с учетом экспертных мнений клинических фармакологов [57].
В условиях пандемии нет возможности дожидаться результатов классических клинических исследований, проводимых в соответствии с принципами GCP, для завершения которых требуется много времени. В связи с этим, сложилась парадоксальная ситуация, когда параллельно происходит изучение действенности лекарственных средств по установленным правилам (протокол, GCP, мониторинг клинического исследования) и отмечается широкое применение тех же препаратов off label в клинической практике, но без строго определенных правил и, зачастую, без анализа исходов. При этом, количество пациентов, получающих лекарственные средства off label, в десятки или сотни раз превышает количество больных, включенных в клинические исследования. Нельзя также забывать о безопасности лекарственных средств, учитывая высокий риск возникновения серьезных и ранее неизвестных нежелательных эффектов. Примером могут быть противомалярийные средства, вызывающие ретинопатию и оказывающие кардиотоксическое действие [58,59]. Необ ходимо подчеркнуть также важность системы фармаконадзора, учитывая регистрацию некоторых лекарственных средств по ускоренной процедуре, которая в Российской Федерации предусмотрена постановлением Правительства No441 от 3 апреля 2020 г. К июню 2020 г. в России были зарегистрированы фавипиравир (Авифарин тм и Арепливир тм ) и левилимаб (Илсира тм ). При применении первого препарата необходимо тщательно контролировать серьезные нежелательные явления типа D, учитывая тератогенность и эмбриотоксичность в опытах животных [60]. Риск развития серьезных нежелательных явлений при лечении моноклональными антителами также хорошо известен, а система фармаконадзора для них требует особых условий [61]. Опубликованы данные о высокой частоте развития грибковых инфекций при применении моноклональных антител к рецепторам ИЛ-6 при COVID-19 [62].
Чтобы свести к минимуму указанные выше риски, рекомендуют проводить адаптивные клинические исследования, имеющие относительно гибкий дизайн, который позволяет вносить изменения в ходе исследования [63]. После завершения таких клинических исследований возможна адаптивная практика регистрации лекарственных средств. Исследование лекарственного средства производится поэтапно, начиная с группы пациентов, у которых лучше потенциальное соотношение пользы и риска, с последующим переходом на другие группы больных в порядке снижения возможной пользы по сравнению с риском. Одновременно собираются доказательства эффективности и безопасности в обычной клинической практике, которые дополняют результаты клинических исследований [64]. Процесс лицензирования осуществляется при тесном сотрудничестве фармпроизводителей и государственных органов надзора. Например, 25 июня 2020 г. в Евросоюзе было выдано условное маркетинговое разрешение на применение ремдесивира (Веклури тм ). При этом производитель должен будет предоставить окончательные отчеты об исследованиях к концу года и соблюдать план управления рисками.
К июню 2020 г. лидерами среди изучаемых лекарств были противомалярийные средства. Хотя результаты единичных клинических исследований показали определенную пользу применения этих препаратов у пациентов с COVID-19, тем не менее, в целом надежды, которые возлагались на аминохинолиновые производные, не оправдались, и нельзя исключить, что в ближайшие месяцы их изучение в мире будет прекращено [65-69]. Так, 5 июня 2020 г. в Великобритании было остановлено рандомизированное исследование гидроксихлорохина (RECOVERY), так как смертность через 28 дней не отличалась между группами сравнения (25,7% и 23,5%, соответственно) [17]. В конце июня в США также было остановлено слепое плацебо-контролируемое рандомизированное клиническое исследование гидрохлорохина (ORCHID) у 500 взрослых госпитализированных пациентов с COVID-19, учитывая отсутствие преимуществ исследуемого препарата перед плацебо [70].
К сожалению, результаты клинических исследований не подтвердили значимого позитивного эффекта лопинавира/ритонавира у пациентов с COVID-19 [71]. Это не удивительно, так как подавляющая концентрация препарата in vitro для SARS-CoV-2 более чем в 200 раз превышает таковую для ВИЧ [72] и не может быть достигнута в клинической практике [73]. Между народная организация по изучению сепсиса (SCC; The International Surviving Sepsis Campaign) заявила, что не рекомендует использовать лопинавир/ритонавир для лечения пациентов с COVID-19 [74].
Перспективным подходом к лечению COVID-19 считают применение препаратов, обладающих противовоспалительными и иммуномодулирующими свойствами. У пациентов с COVID-19 могут быть высокими уровни ряда воспалительных цитокинов, однако это не всегда следует трактовать именно как синдром высвобождения цитокинов, или цитокиновый шторм. Причинами резкого ухудшения состояния больных SARS-CoV-2 пневмонией, в том числе развития шока, могут быть бактериальные инфекции, гиповолемия, связанная с желудочно-кишечным кровотечением, или нарушение функции сердца [74,75]. Первым препаратом этой группы, который стали изучать в клинических исследованиях у пациентов с COVID-19, стал тоцилизумаб, представляющий собой моноклональное антитело к рецептору ИЛ-6 [76]. Началось же все с китайских ученых, которые первыми опубликовали обнадеживающие результаты применения тоцилизумаба у 20 пациентов [77].
Данные по применению глюкокортикостероидов при COVID-19 пока остаются крайне противоречивыми – от оптимизма до полного отрицания [39,78,79]. При мета-анализе клинических исследований у пациентов с ОРДС было показано, что препараты этой группы не влияют на позднюю смертность от всех причин (отношение шансов 0,99; 95% доверительный интервал (ДИ) от 0,64 до 1,52) и продолжительность искусственной вентиляции легких (средняя разница -4,30; 95% ДИ от -9,72 до 1,12) [80].
Ремдесивир первоначально применялся в рамках программы Сompassionate use, организованной производителем, а не в рамках клинических исследований [81]. Опубликованы крайне противоречивые результаты нескольких клинических исследований, в которых изучалась действенность ремдесивира у госпитализированных пациентов с тяжелым течением COVID-19 [82-84]. Обращает внимание, что для данного лекарственного средства часто публикуются не окончательные, а предварительные результаты, которые вызывают восторженные отзывы у регуляторных органов ряда стран, в том числе США, Евросоюза, Японии и Южной Кореи.
Фавипиравир с 2014 г. применяется в Японии для лечения гриппа [85]. По данным первых клинических исследований, фавипиравир может быть эффективным у пациентов со средне-тяжелой формой инфекции [86,87]. В Российской Федерации к июню 2020 г. фавипиравир был зарегистрирован для лечения COVID-19 под двумя торговыми названиями – Авифарин и Арепливир.
В настоящее время у пациентов с COVID-19 активно изучается гипериммунная плазма, которую получают от пациентов, перенесших вирусную инфекции. В крупнейшем исследовании М. Joyner и соавт. вводили от 1 до 2 единиц реконвалесцентной плазмы 5000 пациентам с тяжелой или опасной для жизни SARS-CoV-2 инфекцией. Частота тяжелых нежелательных явлений составила всего 1%, а летальность в течение 7 дней – 14,9%, что соответствует естественному течению тяжелой инфекции [88]. Ранее было показано, что использование реконвалесцентной плазмы уменьшает выделение вируса, но не влияет на выживаемость крайне тяжелых больных. Это может указывать на целесообразность более раннего ее введения [89]. По данным систематического обзора Cochrane, опубликованного 14 мая 2020 г., благоприятное влияние реконвалесцентной плазмы на летальность и клинические симптомы остается недоказанным [90].
Одним из самых удивительных событий в области клинической фармакологии стало беспрецедентно широкое использование off label лекарственных средств при COVID-19 во всем мире, когда различные препараты были включены в клинические (методические) рекомендации и руководства, не дожидаясь результатов клинических исследований, в том числе на фоне отрицательного отношения к некоторым из них профессиональных экспертных организаций [39,75]. Понимая потенциальную опасность широкого применения лекарственных средств off label, в ряде стран были выпущены рекомендации по минимизации возможных рисков. Например, FDA разрешила применение противомалярийных препаратов для лечения COVID-19 (Emergency Use Authorization, EUA), однако указала, что их можно назначать только госпитализированным пациентам, а также рекомендовала всем медицинским работникам и пациентам извещать о нежелательных явлениях национальную систему фармаконадзора (MedWatch) [91]. Однако учитывая сомнительную пользу этих препаратов при COVID-19 и сообщения о серьезных нежелательных реакциях со стороны сердца и других органов и систем, позднее это разрешение в США было отозвано. 16 апреля 2020 г. в Российской Федерации вышло Распоряжение Правительства No1030-р, в котором указана необходимость обязательного мониторинга эффективности и безопасности лекарств, используемых при COVID-19 [92]. Роль и место вакцин в настоящей статье не обсуждается.
Заключение и рекомендации
1. Целый ряд международных экспертов в области клинической фармакологии считают, что пандемия COVID-19 может стать определяющим моментом для развития клинической фармакологии и "нет никаких оснований полагать, что дисциплина не готова принять этот вызов" [14]. Безусловно, отечественная клиническая фармакология должна соответствовать данным трендам.
2. В настоящее время нет этиотропной и патогенетической терапии, которая обладала бы доказанными действенностью, эффективностью и безопасностью при COVID-19. Проводимые сейчас в мире клинические исследования предполагают в основном перепрофилирование лекарственных средств, зарегистрированных по другим показаниям. Ускоренная публикация предварительных данных, которые лишь "намекают" на то, что окончательные результаты могут быть положительными, выгодны только фармацевтическим компаниям и не приносят пользы клиницистам.
3. Скорее всего, пациенты с более тяжелым течением COVID-19 нуждаются в комбинированном лечении, в том числе противовирусными и иммуносупрессивными средствами.
4. За 6 месяцев пандемии остается высокой частота применения лекарственных средств off label, что определяет необходимость строгого мониторинга их эффективности и безопасности. Возможный механизм – создание регистров пациентов с COVID-19 и наблюдение за ними после выздоровления. Безусловно, крайне важен российский практический опыт применения лекарств в условия коронавирусной инфекции.
5. Пандемия предоставляет уникальную возможность для продвижения парадигмы RWD/RWE, науки о дизайне клинических испытаний с акцентом на исследования у пациентов с инфекциями.
Используемые источники
- Mahase E. Covid-19: Coronavirus was first described in The BMJ in 1965. BMJ 2020;369:m1547.
- Almeida JD, Berry D, Cunningham C, еt al. Coronaviruses. Nature 1968;220:16.
- van Driel M, Scheire S, Deckx L, et al. What treatments are effective for common cold in adults and children? BMJ 2018;363:k3786.
- Motola D, Donati M. Biagi C, et al. Safety profile of H1-antihistamines in pediatrics: an analysis based on data from VigiBase. Pharmacoepidemiol Drug Saf 2017;26(10):1164-71.
- Barrett J, Heaton P. Real world data: an unrealized opportunity in global health? Clin Pharmacol Ther 2019;106(1):57-9.
- Белоусов Д.Ю, Зырянов С.К., Колбина А.С. (редакторы). Управление клиническими исследованиями. М. Буки Веди, Издательство ОКИ, 2017, 676 с.
- Darrow J, Avorn J, Kesselheim А. FDA approval and regulation of pharmaceuticals, 1983-2018. JAMA 2020;323(2):164-76.
- European Union Pharmaceutical Forum, High Level Pharmaceutical Forum 2005–2008. [Electronic resource]. https://op.europa.eu/en/publication-detail/-/publication/4fddf639-47cc-4f90-9964-142757d2515a.
- Wang X, Lahoz R, Jawla S, et al. Identification and mapping of worldwide sources of generic real-world data. Pharmacoepidemiol Drug Saf 2019;28(7):899-905.
- Cheng V, Lau S, Woo P, Yuen K. Severe acute respiratory syndrome coronavirus as an agent of emerging and reemerging infection. Clin Microbiol Rev 2007;20:660–94.
- Chan J, Lau S, To K, et al. Middle East respiratory syndrome coronavirus: another zoonotic betacoronavirus causing SARS-like disease. Clin Microbiol Rev 2015;28:465–522.
- Zumla A, Chan J, Azhar E, et al. Coronaviruses – drug discovery and therapeutic options. Nat Rev Drug Discov 2016;15:327-47.
- https://www.euro.who.int/ru/health-topics/health-emergencies/coronavirus-covid-19/news/news/2020/3/who-announces-covid-19-outbreak-a-pandemic.
- der Graaf P, Giacomini K. COVID-19: a defining moment for clinical pharmaco-logy? Pharmacol Ther 2020;108(1):11-5.
- The Lancet Digital Health. https://www.covid-trials.org/.
- Fragkou P, Belhadi D, Peiffer-Smadja N, et al. Review of trials currently testing treatment and prevention of COVID-19. Clin Microbiol Infect 2020;S1198-743X(20)30296-2.
- https://www.recoverytrial.net/.
- https://www.fda.gov/news-events/fda-voices-perspectives-fda-leadership-and-experts/path-forward-coronavirus-treatment-acceleration-program.
- https://presse.inserm.fr/lancement-dun-essai-clinique-europeen-contre-le-covid-19/38737.
- Колбин А.С. Лечение COVID-19 антималярийными средствами с клиникофармакологических позиций. Клин микробиол антимикроб химиотер 2020;3 (в печати).
- Savarino A, Boelaert J, Cassone A, et al. Effects of chloroquine on viral infections: an old drug against today's diseases. Lancet Infect Dis 2003;3(11):722–7.
- Колбин А.С. Ранняя оценка эффективности лекарственных средств при лечении больных с COVID-19. Инфекция и иммунитет 2020;10(2):277–86.
- Borrega J, Gödel P, Rüger M, et al. In the eye of the storm: immune-mediated toxicities associated with CAR-T cell therapy. Hemasphere 2019;3(2):e191.
- Patel A, Verma А. COVID-19 and angiotensin-converting enzyme inhibitors and angiotensin receptor blockers: what is the evidence? JAMA 2020. doi: 10.1001/jama.2020.4812.
- https://clinicaltrials.gov/ct2/show/NCT00886353?term=NCT00886353&draw=2&rank=1.
- Brogi S, Calderone V. Off-target ACE2 ligands: possible therapeutic option for COVID-19? Br J Clin Pharmacol 2020;86(6):1178-9.
- Hoffmann M, Kleine-Weber H, Schroeder S, et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell 2020;181:1–10.
- Marovich M, Mascola J, Cohen M. Monoclonal antibodies for prevention and treatment of COVID-19. JAMA 2020. doi: 10.1001/jama.2020.10245. [Epub ahead of print].
- https://www.medrxiv.org/content/10.1101/2020.03.21.20040691v1.full.pdf.
- Bauchner H, Fontanarosa P. Randomized clinical trials and COVID-19: managing expectations. JAMA 2020. doi: 10.1001/jama.2020.8115. [Epub ahead of print]
- Thorlund K, Dron L, Park J, et al. A real-time dashboard of clinical trials for COVID-19. Lancet Digital Health 2020;2(6):e286-7.
- U.S. Department of Health and Human Services Food and Drug Administration Center for Drug Evaluation and Research (CDER) Center for Biologics Evaluation and Research (CBER) May 2020.
- Mehra M, Desai S, Ruschitzka F, Patel A. Hydroxychloroquine or chloroquine with or without a macrolide for treatment of COVID-19: A Multinational Registry Analysis. Lancet 2020 May 22;S0140-6736(20)31180-6.
- Peng F, Tu L, Yang Y, et al. Management and treatment of COVID-19: The Chinese experience. Can J Cardiol 2020;36(6):915–30.
- http://en.nhc.gov.cn/2020-03/29/c_78469.htm.
- World Health Organisation. Clinical management of severe acute respiratory infection (SARI) when COVID-19 disease is suspected. 2020. Available at: https://www.who.int/publications-detail/clinical-management-of-severe-acute-respiratory-infection-when-novel-coronavirus-(ncov)-infection-is-suspected. Accessed March 13, 2020.
- Временные методические рекомендации. Профилактика, диагностика и лечение новой короновирусной инфекции (COVID-19). Версия 1. 29 января 2020, МЗ РФ.
- Alpern J, Gertner E. Off-label therapies for COVID-19 – are we all in this together? Pharmacol Ther 2020;10.1002/cpt.1862.
- Рекомендации Национального института здоровья США (National Institutes of Health, NIH) https://www.covid19treatmentguidelines.nih.gov/whats-new/.
- https://www.cdc.gov/coronavirus/2019-ncov/hcp/therapeutic-options.html.
- Dollery CT. Clinical pharmacology, the first 75 years and a view of the future. Brit J Clin Pharmacol 2006;61:650–5.
- Powell JR, Cook J, Wang Y, et al. Drug dosing recommendations for all patients: a roadmap for change. Clin Pharmacol Ther 2020. doi: 10.1002/cpt.1923 [Epub ahead of print].
- Garcia-Cremades M, Solans B, Hughes M, et al. Optimizing hydroxychloroquine dosing for patients with COVID-19: an integrative modeling approach for effective drug repurposing. Clin Pharmacol Ther 2020;10.1002/cpt.1856. doi: 10.1002/cpt.1856. [Epub ahead of print].
- Schmidli H, H ring D, Thomas M, et al. Beyond randomized clinical trials: use of external controls. Clin Pharmacol Ther 2020;107(4):806-16.
- Ramamoorthy А, Huang SM. What does it take to transform real-world data into real-world evidence? Clin Pharmacol Ther 2019;106(1):10-8. .
- FDA. Frameword for FDA’s real-world evidence program. 2018. https:// www.fda.gov/media/120060/download.
- Andre E, Honig P. Overcoming regulatory aversion to novel methods of evidence generation. Clin Pharmacol Ther 2020;107(5):1057-8.
- Eichler H, Koenig F, Arlett P, et al. Are novel, nonrandomized analytic methods fit for decision making? The need for prospective, controlled, and transparent validation. Clin Pharmacol Ther 2020;107(4):773-9.
- Jones N, Yoshida K, Salphati L, et al. Complex DDI by fenebrutinib and the use of transporter endogenous biomarkers to elucidate the mechanism of DDI. Clin Pharmacol Ther 2020;107(1):269-77.
- Bao X, Wu J, Xie Y, et al. Protein expression and functional relevance of efflux and uptake drug transporters at the blood-brain barrier of human brain and glioblastoma. Clin Pharmacol Ther 2020;107(5):1116-27.
- Gaedigk A, Whirl-Carrillo M, Pratt V, et al. PharmVar and the landscape of pharmacogenetic sesources. Clin Pharmacol Ther 2020;107(1):43-6.
- Volpi S, Bult C, Chisholm R, et al. Research directions in the clinical implementation of pharmacogenomics: an overview of US programs and projects. Clin Pharmacol Ther 2018;103(5):778-86.
- Relling M, Klein T, Gammal R, et al. The Clinical Pharmacogenetics Implementation Consortium: 10 years later. Clin Pharmacol Ther 2020;107(1):171-5.
- https://www.pharmacogenetics-pharmacogenomics.ru/jour.
- https:// www.pharmgkb.org/disease/PA166197121/overview.
- https://rmapo.ru/pharmacovid.html.
- Magagnoli J, Narendran S, Pereira F, et al. Outcomes of hydroxychloroquine usage in United States veterans hospitalized with Covid-19. medRxiv 2020; 2020.04.16.20065920.
- Browning D. Pharmacology of chloroquine and hydroxychloroquine. Hydroxychlo roquine and chloroquine retinopathy. 2014:35–63.
- Chatre C, Roubille F, Vernhet H, et al. Cardiac complications attributed to chloroquine and hydroxychloroquine: a systematic review of the literature. Drug Saf 2018;41(10):919-31.
- Delang L, Abdelnabi R, Neyts J. Favipiravir as a potential countermeasure against neglected and emerging RNA viruses. Antiviral Res 2018;153:85-94.
- Колбин А.С., Зырянов С.К., Белоусов Д.Ю. (редакторы). Фармаконадзор. М.: Издательство ОКИ: Буки Веди, 2019, 248 с.
- Antinori S, Bonazzetti C, Gubertini G, et al. Tocilizumab for cytokine storm syndrome in COVID-19 pneumonia: an increased risk for candidemia? Autoimmun Rev 2020;19(7):102564.
- Sato A, Shimura M, Gosho M. Practical characteristics of adaptive design in phase 2 and 3 clinical trials. J Clin Pharm Ther 2018;43(2):170-80.
- Oye K, Eichler H, Hoos A, et al. Pharmaceuticals licensing and reimbursement in the European Union, United States, and Japan. J Clin Pharmacol Ther 2016; 100(6):626-32.
- Borba M, Almeida Val F, Sampaio V, et al. CloroCovid-19 Team. Effect of high vs low doses of chloroquine diphosphate as adjunctive therapy for patients hospitalized with severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) infection: a randomized clinical trial. JAMA Netw Open 2020;3(4):e208857.
- Geleris J, Sun Y, Platt J, et al. Observational study of hydroxychloroquine in hospitalized patients with Covid-19. N Engl J Med 2020. doi: 10.1056/NEJMoa 2012410. [Epub ahead of print].
- Rosenberg E, Dufort E, Udo T, et al. Association of treatment with hydroxychloroquine or azithromycin with in-hospital mortality in patients with COVID-19 in New York State. JAMA 2020. doi: 10.1001/jama.2020.8630. [Epub ahead of print].
- Singh A, Singh A, Singh R, Misra A. Hydroxychloroquine in patients with COVID-19: A systematic review and meta-analysis. Diabetes Metab Syndr 2020;14(4):589-96.
- Hernandez A, Roman Y, Pasupuleti V, et al. Hydroxychloroquine or chloroquine for treatment or prophylaxis of COVID-19: a living systematic review. Ann Intern Med 2020. doi: 10.7326/M20-2496. [Epub ahead of print].
- https://www.nih.gov/news-events/news-releases/nih-halts-clinical-trial-hydroxyc-hloroquine.
- Cao B, Wang Y, Wen D, et al. A trial of lopinavir-ritonavir in adults hospitalized with severe Covid-19. N Engl J Med 2020;382(19):1787-99.
- Choy K, Wong A, Kaewpreedee P, et al. Remdesivir, lopinavir, emetine, and homo harringtonine inhibit SARS-CoV-2 replication in vitro. Antiviral Res 2020;178:104786.
- Schoergenhofer C, Jilma B, Stimpfl T, et al. Pharmacokinetics of lopinavir and ritonavir in patients hospitalized with Coronavirus Disease 2019 (COVID-19). Ann Intern Med 2020;M20-1550.
- Alhazzani W, Møller M, Arabi Y, et al. Surviving Sepsis Campaign: Guidelines on the management of critically ill adults with Coronavirus Disease 2019 (COVID-19). Crit Care Med 2020;48(6):e440-69.
- https://www.covid19treatmentguidelines.nih.gov/overview/management-of-covid-19/.
- ClinicalTrials.gov Identifier: NCT04317092. https://clinicaltrials.gov/ct2/show/ NCT04317092?cond=COVID-19&draw=6.
- Xu X, Han M, Li T, et al. Effective treatment of severe COVID-19 patients with tocilizumab. Proc Natl Acad Sci USA 2020;117(20):10970-5.
- Fadel R, Morrison A, Vahia A, et al. Early short course corticosteroids in hospitalized patients with COVID-19. Clin Infect Dis 2020;ciaa601. [Epub ahead of print].
- Russell С, Millar J, Baillie J. Clinical evidence does not support corticosteroid treatment for 2019-nCoV lung injury. Lancet 2020;395(10223):473-5.
- Lewis S, Pritchard M, Thomas C, Smith A. Pharmacological agents for adults with acute respiratory distress syndrome. Сochrane Database Syst Rev 2019;7(7): CD004477.
- Grein J, Ohmagari N, Shin D, et al. Compassionate use of remdesivir for patients with severe Covid-19. N Engl J Med 2020;382(24):2327-36.
- Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet 2020;395(10236):1569-78.
- Beigel J, Tomashek K, Dodd L, et al. Remdesivir for the treatment of Covid-19 preliminary report. N Engl J Med 2020;NEJMoa2007764. [Epub ahead of print].
- https://www.gilead.com/news-and-press/press-room/press-releases/2020/6/gile-ad-announces-results-from-phase-3-trial-of-remdesivir-in-patients-with-modera-te-covid-19.
- Furuta Y, Komeno T, Nakamura Е. Favipiravir (T-705), a broad spectrum inhibitor of viral RNA polymerase. Proc Jpn Acad Ser B Phys Biol Sci 2017;93(7): 449-63.
- Chen C, Zhang Yi, Huang J, et al. Favipiravir versus Arbidol for COVID-19: a randomized clinical trial. medRxiv. Preprint posted March 27, 2020. doi:10.1101/ 2020.03.17.20037432.
- Cai Q, Yang M, Liu D, et al. Experimental treatment with favipiravir for COVID-19: an open-label control study. Engineering (Beijing) 2020. doi: 10.1016/ j.eng.2020.03.007. [Epub ahead of print].
- Joyner M, Wright S, Fairweather D, et al. Early safety indicators of COVID-19 convalescent plasma in 5,000 patients. medRxiv. Preprint posted online May 14, 2020. doi:10.1101/2020.05.12.20099879.
- Zeng Q, Yu Z, Gou J, et al. Effect of convalescent plasma therapy on viral shedding and survival in patients with Coronavirus Disease 2019. J Infect Dis 2020;222(1):38-43.
- Valk S, Piechotta V, Chai K, et al. Convalescent plasma or hyperimmune immunoglobulin for people with COVID-19: a rapid review. Сochrane Database Syst Rev 2020;5(5):CD013600.
- https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-reiterates-importance-close-patient-supervision-label-use?utm_cam-paign=042420_PR_FDA%20Notes%20Importance%20of%20Patient%20Supervis ion%20of%20Antimalarial%20Drug%20Use&utm_medium=email&utm_source= Eloqua.
- http://publication.pravo.gov.ru/Document/View/0001202004160037.
