Современные европейские рекомендации по артериальной гипертонии: обновленные позиции и нерешенные вопросы
Несмотря на усилия врачей, направленные на контроль артериального давления (АД) и снижение сердечно-сосудистого риска, распространенность артериальной гипертонии (АГ) в мире продолжает расти, и по прогнозам к 2025 году число больных АГ достигнет 1,5 млрд. Это обусловливает необходимость разработки новых, более эффективных подходов к диагностике и лечению АГ. Целью данного обзора является детальный сравнительный анализ рекомендаций по ведению пациентов с АГ Европейского общества кардиологов и Европейского общества по АГ 2018 и 2013 гг. В статье представлен подробный разбор глав и разделов рекомендаций, которые касаются диагностики АГ, оценки сердечно-сосудистого риска, целевых диапазонов АД, выбора тактики лечения пациентов в зависимости от возраста и сопутствующих заболеваний.
Анонсирование новой версии рекомендаций Европейского общества кардиологов (ЕОК) и Европейского общества по артериальной гипертонии (ЕОАГ) стало главным событием 28-го конгресса по артериальной гипертонии (АГ) и сердечно-сосудистой профилактике в июне 2018 г. Официальное представление рекомендаций, публикация полного текста документа и его детальное обсуждение состоялись на Европейском конгрессе кардиологов в Мюнхене в августе 2018 г. Целью пересмотра и обновления существующего документа стала разработка практических рекомендаций, направленных на улучшению диагностики и лечения АГ, а также повышение частоты контроля артериального давления (АД) с использованием простых и эффективных стратегий лечения. Основанием для обновленных рекомендаций послужили опубликованные в 2013-2018 гг. ре зуль таты серий крупных исследований и сетевых мета-анализов [1–22]. Детальная проработка полученных данных позволила экспертам дать ответы на существовавшие вопросы относительно диагностики и лечения АГ.
В рекомендациях 2018 г., как и в предыдущей версии, были использованы те же классы и уровни доказанности (рис. 1) [23]. Почти две трети (64,4%) рекомендаций относятся к классу I. По сравнению с вариантом 2013 г. увеличилось количество рекомендаций класса IA (с 27 до 50). К III классу отнесены 9,7% рекомендаций. В целом однозначная стратегия лечения определена по абсолютному большинству позиций (74,1%), хотя около четверти рекомендаций отнесены к классу II и, соответственно, требуют дальнейших исследований.
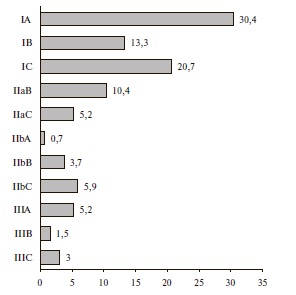
Основные отличия рекомендаций 2018 г. от предыдущей версии
Рекомендации 2018 г. заметно отличаются по многим позициям от предыдущей версии (табл. 1).
| Примечание: АГ – артериальная гипертония; АД – артериальное давление; АК – антагонисты кальция; БРА – блокаторы рецепторов ангиотензина II; СКАД – самоконтроль АД; АПФ – ангиотензинпревращающий фермент |
| • Измерение АД |
| - Более широкое использование СМАД и/или СКАД для измерения АД вне офиса, особенно СКАД, для диагностики АГ, выявления гипертонии “белого халата” и маскированной гипертонии, а также с целью контроля АД |
| • Менее консервативное лечение АД у пациентов пожилого и старческого возраста |
| - Низкие пороговые значения АД и целевые показатели АД для пожилых пациентов с акцентом на биологический, а не паспортный возраст (важность “хрупкости”, потребности в уходе и переносимости лечения) |
| - Отказ от лечения или его отмена не должны базироваться на возрасте при условии хорошей переносимости лечения |
| • Стратегия лечения фиксированной комбинацией нескольких антигипертензивных агентов в 1 таблетке для улучшения контроля АД |
| - Предпочтительное использование двухкомпонентной комбинированной терапии для первичного лечения большинства пациентов с АГ |
| - При назначении лечения отдавать предпочтение фиксированной комбинации нескольких антигипертензивных агентов в одной таблетке для лечения АГ у большинства пациентов |
| - Упрощенные алгоритмы лечения с предпочтительным применением ингибиторов АПФ или БРА в сочетании с АК и/или тиазидным или тиазидоподобным диуретиком в качестве основной стратегии лечения для большинства пациентов (β-адреноблокаторы при наличии конкретных показаний). |
| • Новые целевые диапазоны АД у пациентов, получающих лечение |
| - Целевые диапазоны АД для пациентов, получающих лечение, для лучшего определения рекомендуемой мишени АД в зависимости от возраста пациента и конкретных сопутствующих заболеваний |
| - Нижние границы безопасности при лечении АД |
| • Выявление низкой приверженности к медикаментозному лечению |
| - Акцент на важности оценки приверженности к лечению как одной из основных причин плохого контроля АД. |
| • Ключевая роль медсестер и фармацевтов в долгосрочном лечении АГ |
| - Подчеркивается важная роль медсестер и фармацевтов в обучении, поддержке и последующем лечении пациентов с АГ как часть общей стратегии улучшения контроля АД. |
По сравнению с рекомендациями 2013 г. классификация уровней АД и критерии определения АГ по результатам офисного и амбулаторного измерений АД не изменились. Как и в предыдущих версиях Евро пей ских рекомендаций, эксперты предлагают выделять оптимальное (систолическое АД [САД] <120 мм рт. ст. и диастолическое АД [ДАД] <80 мм рт. ст.), нормальное (САД 120129 мм рт. ст. и/или ДАД 80-84 мм рт. ст.), высокое нормальное (САД 130-139 мм рт. ст. и/или ДАД 85-89 мм рт. ст.) АД, три степени АГ и изолированную систолическую АГ (IC) [23,24]. Эта классификация применяется у пациентов любого возраста за исключением детей и подростков, у которых используют центильные значения АД [26].
Артериальная гипертония, как и прежде, диагностируется при уровне САД ≥140 мм рт. ст. и/или ДАД ≥90 мм рт. ст. при офисных измерениях, ≥130 и/или ≥80 мм рт. ст. за сутки, ≥135 и/или ≥85 мм рт. ст. за день, ≥120 и/или ≥70 мм рт. ст. за ночь при суточном мониторировании АД (СМАД) и ≥135 и/или ≥85 мм рт. ст. при самоконтроле АД (СКАД).
Диагностика АГ может основываться не только на измерениях офисного АД, но и на результатах амбулаторных методов диагностики – СМАД или СКАД при их экономической и логистической целесообразности (IC). В новых рекомендациях детально отражены преимущества и недостатки обоих методов диагностики. Более широкое использование амбулаторных методов оценки АД позволяет выявить гипертонию “белого халата” и маскированную гипертонию, а также оценить эффективность назначенной антигипертензивной терапии и причины нежелательных лекарственных явлений (медикаментозной гипотонии) (IA).
Важность регулярной оценки уровня АД отражена в новом разделе, посвященном скринингу АГ. Все лица старше 18 лет должны знать уровень своего АД, а результаты измерений АД должны быть зарегистрированы в амбулаторной медицинской карте (IB). Частота повторного скрининга определяется значениями АД: у здоровых людей с оптимальным офисным АД его следует измерять не реже одного раза в 5 лет (IC), у людей с нормальным АД – 1 раз в 3 года (IC), с высоким нормальным АД – ежегодно (IC). У пациентов старше 50 лет эксперты рекомендуют проводить скрининговое обследование чаще в зависимости от выявленного уровня АД из-за постепенного повышения САД с возрастом (IIaC).
Изменения терминологии
В обновленных рекомендациях на смену привычного термина “поражение органов-мишеней” пришло словосочетание “поражение органов, обусловленное гипертонией” (ПООГ), которое по мнению экспертов точнее отражает структурные и/или функциональные изменения в органах (сердце, головном мозге, сетчатке глаз, почках и сосудах), вызванные наличием АГ. Впервые в рекомендациях 2018 г. выделены стадии гипертонической болезни (ГБ) с учетом степени повышения АД, сердечно-сосудистых факторов риска, ПООГ, ассоциированных клинических состояний (АКС) и коморбидной патологии, которые соответствуют существующей в России классификации ГБ.
Стратификация сердечно-сосудистого риск
Изменения в новых рекомендациях 2018 года коснулись спектра факторов риска, ПООГ и АКC (табл. 2). В число факторов риска, влияющих на прогноз, с 2018 г. добавлены мочевая кислота, семейный анамнез раннего возникновения АГ, ранняя менопауза, малоподвижный образ жизни, психосоциальные и социально-экономические факторы, а также частота сердечных сокращений более 80 в минуту в покое.
| Рекомендации 2013 г. | Рекомендации 2018 г. |
|---|---|
| Примечание: ГЛЖ – гипертрофия левого желудочка; ИБС – ишемическая болезнь сердца; ЛЖ – левый желудочек; ЛП – левое предсердие; ММЛЖ – масса миокарда левого желудочка; ОТС – относительная толщина стенок; рСКФ – расчетная скорость клубочковой фильтрации; ТИМ – толщина интима-медиа; ХБП – хроническая болезнь почек; ФП – фибрилляция предсердий | |
| Факторы риска | |
| Мужской пол | |
| Возраст | |
| Курение | Курение в настоящее время и в прошлом |
| Общий холестерин | |
| Общий холестерин сыворотки >4,9 ммоль/ли/или | ХС ЛВП |
| ХС ЛВП <1,0 ммоль/л у мужчин и <1,2 ммоль/л у женщини/или | |
| ХС ЛНП >3,0 ммоль/ли/или | |
| Триглицериды >1,7 ммоль/л | |
| – | + Мочевая кислота |
| Глюкоза плазмы натощак 5,6-6,9 ммоль/л (102-125 мг/дл) | - |
| Нарушение толерантности к глюкозе | - |
| + Сахарный диабет | |
| Ожирение | Избыточная масса тела или ожирение |
| Абдоминальное ожирение (окружность талии ≥102 см у мужчин и ≥88 см у женщин) | - |
| Семейный анамнез ранних сердечно-сосудистых заболеваний (<55 лет у мужчин, <65 лет у женщин) | |
| - | + Семейный анамнез ранней АГ |
| + Ранняя менопауза | |
| + Малоподвижный образ жизни | |
| + Психосоциальные и социально-экономические факторы | |
| + ЧСС (>80 в минуту в покое) | |
| Поражение органов, обусловленное АГ | |
| Артериальная жесткость: пульсовое АД (у лиц пожилого и старческого возраста) ≥60 мм рт. ст.; скорость каротидно-феморальной пульсовой волны >10 м/с | |
| ЭКГ-признаки ГЛЖ (индекс Соколова-Лайона >35 мм, RaVL ≥11 мм; индекс Корнелла >2440 мм × м) | |
| Эхокардиографические признаки ГЛЖ (индекс ММЛЖ >115 г/м2 у мужчин, >95 г/м2 у женщин) | Эхокардиографические признаки ГЛЖ (2013 г.) у лиц с нормальной массой тела |
| + ММЛЖ/рост2,7 (>50 г/м2,7 у мужчин, >47 г/м2,7 у женщин) при ожирении | |
| Эхокардиографическое определение концентрической геометрии | |
| ОТС >0,42 | ОТС >0,43 |
| - | Конечный диастолический диаметр ЛЖ/рост >3,4 см/м у мужчин, >3,3 см/м у женщин |
| - | Объем ЛП/рост2 >18,5 мл/м2 у мужчин, >16,5 мл/м2 у женщин |
| Лодыжечно-плечевой индекс <0,9 | |
| Альбуминурия (30-300 мг/сут) или повышение соотношения альбумин/креатинин (&rt;30-300 мг/г; 3,4-34 мг/ммоль) в утренней моче | |
| Умеренная ХБП с рСКФ 30-59 мл/мин/1,73 м2 | Умеренная ХБП с рСКФ 30-59 мл/мин/1,73 м2 или тяжелая ХБП с рСКФ <30 мл/мин/1,73 м2 |
| Утолщение стенки сонных артерий (ТИМ <0,9 мм) или атеросклеротическая бляшка | Утолщение стенки сонных артерий ТИМ <0,9 мм считается повышенным, но оценивать необходимо в соответствии с возрастом |
| - | + Значимая ретинопатия: кровоизлияния или экссудаты, отек соска зрительного нерва |
| Ассоциированные клинические состояния | |
| ИБС: инфаркт миокарда, стенокардия, реваскуляризация миокарда | |
| Сердечная недостаточность, включая сердечную недостаточность с сохраненной фракцией выброса левого желудочка | |
| Заболевания периферических артерий | |
| ХБП с рСКФ <30 мл/мин/1,73 м2 | → ПООГ |
| Тяжелая ретинопатия: кровоизлияния или экссудаты, отек соска зрительного нерва | → ПООГ |
| + Наличие атеросклеротической бляшки при визуализации артерий + ФП | |
| + ФП | |
Спектр бессимптомного ПООГ также претерпел изменения. К параметрам, оцениваемым по данным эхокардиографии, добавлены формула расчета массы миокарда левого желудочка у пациентов с ожирением и оценка размера левого предсердия. К ПООГ с 2018 г. отнесены не только умеренная хроническая болезнь почек (ХБП) с расчетной скоростью клубочковой фильтрации (СКФ) <60 мл/мин/1,73м2, но и тяжелая ХБП с СКФ <30 мл/мин/1,73м2 (расчет по формуле CKD-EPI), а также выраженная ретинопатия с геморрагиями или экссудатами, отеком соска зрительного нерва. Показатель толщины интимы-медии (ТИМ) сонной артерии более 0,9 мм в новой версии рекомендаций не является критерием ПООГ, хотя и считается повышенным.
Перечень ассоциированных сердечно-сосудистых заболеваний дополнен наличием атеросклеротических бляшек по результатам визуализирующих методов и фибрилляцией предсердий.
В 2018 г. сохранен подход к оценке 10-летнего сердечно-сосудистого риска по шкале SCORE, которую эксперты рекомендуют использовать у пациентов с АГ из категории низкого или умеренного риска – без сердечно-сосудистых заболеваний, патологии почек или сахарного диабета (СД), а также одного выраженного фактора риска (например, уровня холестерина) или гипертрофии левого желудочка (ГЛЖ) (IB). Такое пристальное внимание к оценке сердечно-сосудистого риска у пациентов с АГ обусловлено влиянием установленной категории риска на выбор дальнейшей тактики ведения и временные рамки инициации лекарственной терапии. Сердечно-сосудистый риск, оцениваемый по шкале SCORE, значительно повышается при наличии дополнительных факторов риска, таких как социальная депривация, ожирение (увеличение индекса массы тела) и центральное ожирение (увеличение окружности талии), отсутствие физической активности, психологический стресс, семейный анамнез раннего развития сердечно-сосудистых заболеваний, аутоиммунные и другие воспалительные заболевания, значимые психические расстройства, лечение инфекций при наличии вируса иммунодефицита человека, фибрилляция предсердий, ГЛЖ, ХБП, синдром обструктивного апноэ сна. Наличие модифицирующих факторов у пациентов из категории низкого или умеренного риска по шкале SCORE позволяет установить более высокий сердечнососудистый риск, что влечет за собой выбор более агрессивной тактики лечения и коррекции факторов риска.
Неизменной осталась позиция относительно выявления у всех пациентов с АГ бессимптомного ПООГ, наличие которого может приводить к увеличению категории сердечно-сосудистого риска, особенно у людей молодого и среднего возраста.
Целевые диапазоны и границы безопасного снижения АД
В Европейских рекомендациях 2013 г. для большинства пациентов с АГ выделяли единый целевой уровень САД – менее 140 мм рт. ст. [23]. Исключение составляли пациенты пожилого и старческого возраста, для которых целевой диапазон САД составлял 140-150 мм рт. ст. (IA). В качестве целевого ДАД был рекомендован уровень менее 90 мм рт. ст., а у пациентов с СД – менее 85 мм рт. ст. [23]. В новых рекомендациях 2018 г. появились два целевых порога АД: менее 140/90 мм рт. ст. у всех пациентов и, при условии хорошей переносимости, последующее снижение АД до 130/80 мм рт. ст. и ниже у большинства пациентов (IA).
Такое решение экспертов обусловлено появлением убедительных доказательств пользы снижения САД <140 и <130 мм рт. ст. по результатам крупного метаанализа рандомизированных клинических исследований [4]. При снижении САД <130 мм рт. ст. установлено значительное уменьшение риска развития основных ассоциированных с АГ сердечно-сосудистых осложнений, в том числе ИБС – на 12%, инсульта – на 27%, сердечной недостаточности – на 25%, основных сердечно-сосудистых событий – на 13%, смерти от любой причины – на 11%. Снижение риска основных сердечно-сосудистых исходов при достижении САД <130 мм рт. ст. или ДАД <80 мм рт. ст. было также продемонстрировано в другом мета-анализе [16].
Обращает на себя внимание тот факт, что целевой уровень АД не может быть одинаковым у всех пациентов с АГ. Целевые значения АД отличаются в зависимости от возраста и сопутствующих заболеваний. Для пациентов моложе 65 лет с АГ, сочетающейся с СД, ИБС и/или инсультом/транзиторной ишемической атакой предложены более низкие целевые уровни САД – 130 мм рт. ст. или ниже при условии хорошей переносимости, но не ниже 120 мм рт. ст. Пациентам в возрасте 65 лет и старше или больным с ХБП рекомендуется достижение целевого уровня САД в диапазоне 130-139 мм рт. ст.
Целевое значение ДАД составляет <80 мм рт. ст. у всех пациентов независимо от величины риска и сопутствующих заболеваний (IIaB).
Еще одним важным нововведением в рекомендациях 2018 г. стало выделение нижней границы безопасного целевого значения АД, которая для САД составляет 120 мм рт. ст., а для ДАД – 70 мм рт. ст. Такое решение обусловлено увеличением риска нежелательных явлений, который превышал положительные эффекты антигипертензивной терапии у пациентов, включенных в рандомизированные клинические исследования, на фоне низких значений АД [27].
Тактика лечения пациентов с АГ
Модификация образа жизни и коррекция имеющихся факторов риска рекомендованы всем пациентам с АГ или высоким нормальным АД. В 2018 г. эксперты рекомендовали более жесткое ограничение употребления соли пациентам с АГ – менее 5 г/сут против 5-6 г/сут в 2013 г. Рекомендовано также избегать обильного систематического употребления алкоголя (IIIC) – не более 14 единиц в неделю у мужчин и не более 8 единиц в неделю у женщин (1 единица соответствует 125 мл вина или 250 мл пива).
Сроки инициации антигипертензивной терапии (одновременно с немедикаментозными методами или через несколько месяцев) определяются уровнем АД, величиной сердечно-сосудистого риска, наличием ПООГ или сердечно-сосудистых заболеваний. Как и прежде, немедленное назначение медикаментозной антигипертензивной терапии рекомендуется всем пациентам с АГ 2 и 3 степени независимо от уровня сердечно-сосудистого риска (IA). При этом целевой уровень АД должен быть достигнут в течение 3 месяцев.
В рекомендациях 2013 г. нерешенными оставались вопросы, связанные с лечением пациентов с АГ 1 степени, относящихся к группам низкого или среднего риска, пациентов с гипертонией “белого халата”, маскированной гипертонией, пациентов с высоким нормальным АД и пожилых пациентов с уровнем АД 140-160 мм рт. ст. В новой версии рекомендаций эксперты дали ответы на эти вопросы. Для пациентов с низким и средним риском и 1 степенью АГ без сердечно-сосудистых заболеваний, заболеваний почек и ПООГ рекомендовано назначить медикаментозное лечение, если через 3-6 месяцев после изменения образа жизни не достигнуты целевые значения АД (IA против IIaB в предыдущей версии рекомендаций). У пациентов с АГ 1 степени и высоким или очень высоким сердечно-сосудистым риском, с сердечно-сосудистыми заболеваниями, заболеваниями почек или признаками ПООГ назначение медикаментозной антигипертензивной терапии рекомендуется одновременно с коррекцией образа жизни (IA против IB в предыдущей версии рекомендаций).
Изменились взгляды и на ведение пациентов с высоким нормальным АД (130-139/85-89 мм рт. ст.). В рекомендациях 2013 г. назначение медикаментозной антигипертензивной терапии пациентам с высоким нормальным АД не было показано (IIIA) [23]. Однако мета-анализ 24 рандомизированных клинических исследований показал, что назначение антигипертензивной терапии снижает риск сердечно-сосудистых заболеваний у пациентов с высоким нормальным и нормальным АД и очень высоким сердечно-сосудистым риском [28]. Поэтому в рекомендациях 2018 г. указано, что медикаментозное лечение возможно у пациентов с высоким нормальным АД и сердечно-сосудистыми заболеваниями, особенно с ИБС (IIbА).
Существенным изменением европейских рекомендаций 2018 г. стали достаточно лояльные подходы к контролю АД у пожилых людей. Это стало возможным благодаря результатам исследований SPRINT, HOPE-3 и анализа подгруппы пожилых пациентов из исследования HYVET [29–31]. Предложены более низкие исходные уровни АД для начала антигипертензивной терапии у пожилых пациентов. Сделан акцент на важности оценки именно биологического, а не паспортного возраста больного, с учетом его способности к самообслуживанию, переносимости терапии и наличия старческой астении. Достижение пациентом определенного возраста (80 лет и более) не является основанием для отмены лечения или отказа от назначения антигипертензивной терапии при условии ее хорошей переносимости (IIIА). Медикаментозная антигипертензивная терапия и модификация образа жизни у “активных” пожилых пациентов (fit older; даже в возрасте старше 80 лет) рекомендуются при уровне САД ≥160 мм рт. ст. (IA). При условии хорошей переносимости медикаментозное лечение возможно и у хрупких пожилых пациентов (IIbB).
Подходы к медикаментозному лечению АГ
Несмотря на прилагаемые усилия, более 50% пациентов с АГ не достигают целевых значений АД менее 140/90 мм рт. ст. на фоне назначенной антигипертензивной терапии [32,33]. В связи с этим, в отличие от предыдущей версии документа [23], в которой выбор медикаментозной стратегии (монотерапия или комбинация антигипертензивных препаратов) был основан на степени повышения АД и категории сердечно-сосудистого риска, в 2018 г. рекомендовано начинать медикаментозное лечение АГ у большинства пациентов с комбинации двух препаратов (IA) [34]. Исключение составляют пациенты с низким сердечно-сосудистым риском и АГ 1 степени (в частности, при САД >150 мм рт. ст.), пациенты с высоким нормальным АД и очень высоким сердечно-сосудистым риском и хрупкие пожилые больные, которым рекомендована монотерапия [34].
Исходное назначение комбинированной терапии антигипертензивными препаратами даже в низких дозах эффективнее снижает АД, чем терапия одним препаратом в максимальной дозе [35]. Стартовое назначение комбинации из двух антигипертензивных препаратов безопасно и хорошо переносится даже пациентами с АГ 1 степени, а небольшое увеличение риска развития эпизодов артериальной гипотензии не приводит к частому прекращению лечения [22,35,36].
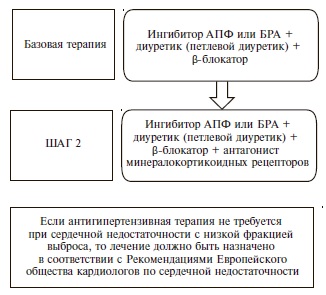
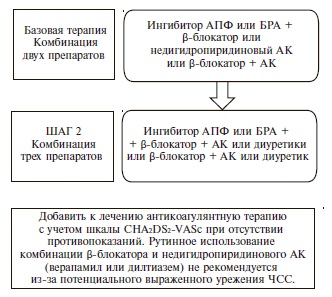
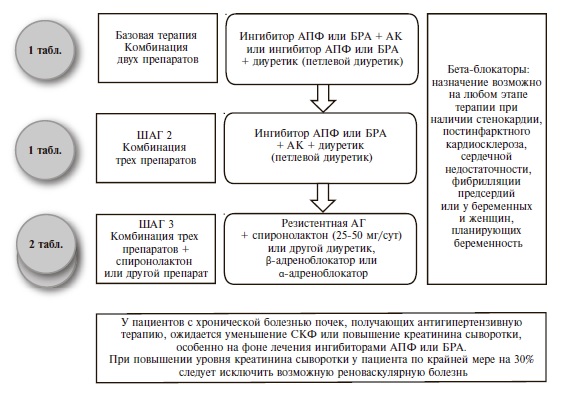
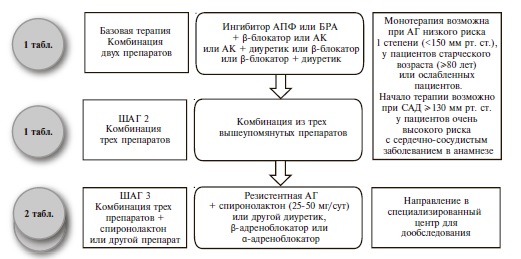
Как и раньше, основными классами препаратов для лечения АГ остаются ингибиторы АПФ, блокаторы рецепторов ангиотензина II (БРА), антагонисты кальция (АК), диуретики (тиазидные и тиазидоподобные) и β-адреноблокаторы (ББ) (IA). В рекомендациях 2018 г. предложены четкие схемы лечения пациентов с неосложненной АГ (рис. 2) и сопутствующей патологией, в том числе ИБС (рис. 3), сердечной недостаточностью (рис. 4), фибрилляцией предсердий (рис. 5) и ХБП (рис. 6) [34]. Алгоритм назначения базовой терапии при неосложненной АГ также подходит для пациентов с ПООГ, цереброваскулярной болезнью, СД или заболеванием периферических артерий (рис. 2).
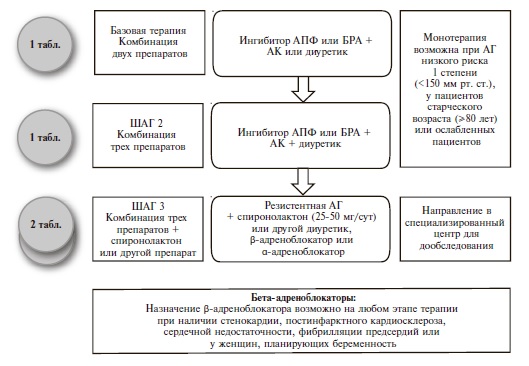
По мнению экспертов, максимальное упрощение режима приема препаратов будет способствовать повышению приверженности пациентов к лечению, поэтому необходимо отдавать предпочтение фиксированным комбинациям двух или более антигипертензивных агентов в 1 таблетке (IB). Предпочтительными комбинациями являются сочетание блокатора ренин-ангиотензиновой системы (ингибитора АПФ или БРА) с АК или диуретиком (IA). ББ могут быть использованы для снижения АД при наличии особых клинических ситуаций – стенокардии, перенесенного инфаркта миокарда, сердечной недостаточности, аритмии (IA).
В случае недостаточного контроля АД на фоне комбинированной терапии двумя препаратами рекомендовано добавление третьего препарата (комбинация блокатора ренин-ангиотензиновой системы с АК и тиазидным/тиазидоподобным диуретиком, предпочтительно в одной таблетке) (IA). Эксперты не рекомендуют исходно назначать комбинацию трех антигипертензивных препаратов.
При неэффективности комбинированной терапии тремя препаратами рекомендовано добавить к лечению спиронолактон в низкой дозе, а при его непереносимости – эплеренон, амилорид, более высокие дозы тиазидных/тиазидоподобных диуретиков или петлевой диуретик, ББ или α-адреноблокатор (IВ).
В отличие от предыдущей версии рекомендаций [23], в текущем варианте применение технических устройств для лечения АГ не рекомендовано в рутинной клинической практике (IIIB). Исключением может стать использование устройств в рамках клинических исследований, пока не будут получены доказательства их безопасности и эффективности [34].
В текст документа 2018 г. добавлены новые разделы, которые будут детально рассмотрены ниже (табл. 3). В новых рекомендациях 2018 г. расширен раздел, посвященный вторичной АГ. Несмотря на относительно невысокую распространенность вторичных форм АГ, которая достигает 5-15% в популяции пациентов с АГ [37], рассмотрены наиболее частые причины ее развития, а также распределение форм вторичной АГ в зависимости от возраста. Учитывая, что скрининг вторичных форм АГ среди всех пациентов с высоким АД затруднителен, представлены характеристики, которые помогают заподозрить вторичную АГ: пациенты молодого возраста (<40 лет) с АГ 2-й степени или развитием АГ любой степени в детском возрасте; внезапное ухудшение течения АГ у пациентов с документированной стабильной нормотонией в прошлом; резистентная АГ; тяжелая (степень 3) АГ или неотложные состояния, обусловленные АГ; наличие выраженного поражения органов, обусловленного АГ; клинические или биохимические признаки, свидетельствующие о наличии эндокринной причины АГ или ХБП; признаки синдрома обструктивного ночного апноэ; признаки феохромоцитомы или семейный анамнез феохромоцитомы. Основу диагностики вторичных форм АГ составляют анализы крови и мочи, ультразвуковое исследование брюшной полости и эхокардиография. Отдельно в этом разделе представлен список лекарственных и химических веществ, которые приводят к повышению АД, а также редкие генетические заболевания, которые являются причиной вторичной АГ (синдром Лиддла, синдром Гордона и др.).
| Примечание: ХОБЛ – хроническая обструктивная болезнь легких; SCORE – Systematic COronary Risk Evaluation |
| • Когда подозревать и как выявлять причины вторичной гипертонии |
| • Лечение гипертонических кризов |
| • Обновленные рекомендации по коррекции АД при остром инсульте |
| • Обновленные рекомендации по лечению гипертонии у женщин во время беременности |
| • АГ в разных этнических группах |
| • АГ и ХОБЛ |
| • АГ, фибрилляция предсердий и другие аритмии |
| • Применение перорального антикоагулянта при АГ |
| • АГ и сексуальная дисфункция |
| • Лечение АГ и противоопухолевая терапия |
| • Периоперационное лечение АГ |
| • Препараты для снижения уровня глюкозы и АД |
| • Обновленные рекомендации по оценке и коррекции риска: (1) использование системы SCORE для оценки риска у пациентов без сердечно-сосудистых заболеваний; (2) важность оценки ПООГ в изменении сердечно-сосудистого риска; и (3) использование статинов и аспирина для профилактики сердечно-сосудистых заболеваний. |
По сравнению с предыдущей версией рекомендаций в 2018 г. значительно изменен и дополнен раздел по неотложным состояниям, обусловленным АГ. Под робно перечислены неотложные состояния, требующие немедленного снижения АД с помощью внутривенного введения антигипертензивных препаратов, необходимые исследования, а также перечень лекарственных препаратов, дозировки и особенности их введения при неотложных ситуациях. Подчеркивается, что пациенты с тяжелой АГ (3-й степени) без признаков острого ПООГ не нуждаются в госпитализации. Снижение АД и коррекцию терапии у таких больных следует проводить амбулаторно согласно алгоритму, представленному на рис. 2. Более детально эта информация отражена в консенсусе 2018 г. по ведению пациентов с неотложными состояниями, обусловленными АГ [38].
Раздел по ведению пациентов с цереброваскулярной болезнью, в частности, по коррекции АД при остром инсульте, в рекомендациях 2018 г. был значительно дополнен новыми положениями. У пациентов с острым геморрагическим инсультом не рекомендуется быстрое снижение АД, если САД составляет <200 мм рт. ст. (III А), однако при чрезмерно повышенном АД (САД ≥220 мм рт. ст.) целесообразно осторожное его снижение путем внутривенных инфузий антигипертензивных препаратов до <180 мм рт. ст. (IIаВ). У пациентов с острым ишемическим инсультом также не рекомендуется рутинное снижение АД (IIIА). Исключение составляют пациенты, которым планируется проведение внутривенной тромболитической терапии. В этом случае следует снизить АД и поддерживать его на уровне <180/105 мм рт. ст. в течение 24 ч после тромболизиса (IIаВ). У больных с чрезмерно повышенным АД (САД ≥220 мм рт. ст. или ДАД ≥120 мм рт. ст.), которым не проводился фибринолиз, решение о его снижении необходимо принимать на основании клинической оценки состояния (IIbС). В рекомендациях 2018 г. определены время начала медикаментозного лечения АГ после перенесенного цереброваскулярного события и целевой уровень АД. Начинать антигипертензивную терапию необходимо сразу после транзиторной ишемической атаки (IА) и через несколько дней после ишемического инсульта (IА) для достижения целевых значений САД 120-130 мм рт. ст. (IIаВ). Основой медикаментозного лечения АГ, направленного на предупреждение инсульта, является блокатор ренин-ангиотензиновой системы в сочетании с АК или тиазидоподобным диуретиком (IА).
В документе 2018 г. обновлен и расширен раздел по ведению АГ у беременных женщин. Изменились позиции в отношении величины АД для назначения антигипертензивной терапии. В версии 2013 г. медикаментозная терапия рекомендовалась при тяжелой АГ у беременных (САД >160 мм рт. ст. или ДАД >110 мм рт. ст.; IC) и считалась целесообразной у беременных со стойким повышением АД ≥150/95 мм рт. ст., а также у пациенток с АД ≥140/90 мм рт. ст. при наличии гестационной АГ, субклинического ПООГ или клинических симптомов (IIbC). В новом документе рекомендовано начинать антигипертензивное лечение у пациенток с гестационной АГ, хронической АГ или АГ с субклиническим ПООГ или клиническими симптомами при уровне САД ≥140 мм рт. ст. или ДАД ≥90 мм рт. ст. (IC), во всех других случаях – при уровне САД ≥150 мм рт. ст. или ДАД ≥95 мм рт. ст. (IC). Значения САД ≥170 мм рт. ст. или ДАД ≥110 мм рт. ст. у беременной женщины рассматриваются как неотложное состояние, требующее госпитализации (IC). Неизменными остаются препараты выбора для контроля АД у беременных женщин – метилдопа (IB), лабеталол (IC) и АК (IC). Ингибиторы АПФ, БРА или прямой ингибитор ренина не рекомендованы во время беременности (IIIC). Определены сроки родоразрешения для пациенток с гестационной гипертонией или легкой преэклампсией – 37-я неделя гестации (IB).
Принципиально новый раздел, появившийся в рекомендациях 2018 г., касается ведения АГ в разных этнических группах. В качестве начальной терапии для большинства чернокожих пациентов рекомендуется комбинация из двух медикаментов в одной таблетке (IC), а препаратами выбора должны быть диуретик или АК, либо в комбинации, либо с блокатором ренинангиотензиновой системы (IB). В качестве последнего предпочтительнее назначение сартанов из-за частого развития ангионевротического отека на фоне приема ингибиторов АПФ в этой когорте пациентов [39,40]. Стартовая монотерапия возможна у больных с АГ 1 степени и “хрупких” пожилых пациентов. В других этнических группах снижение АД может основываться на базовом алгоритме лечения АГ, представленном на рис. 2 (IIbC).
АГ является самой частой сопутствующей патологией у пациентов с ХОБЛ [41]. Учитывая этот факт, общие факторы риска двух заболеваний, а также возможное негативное влияние препаратов для лечения ХОБЛ на сердечно-сосудистую систему, в рекомендациях 2018 г. появился отдельный раздел, посвященный вопросам выбора оптимальной антигипертензивной терапии у пациентов с АГ и ХОБЛ [41,42]. Сделан акцент на важности коррекции факторов риска и модификации образа жизни у пациентов с АГ и ХОБЛ. Эксперты рекомендуют начинать антигипертензивную терапию с АК, БРА или ингибитора АПФ или комбинации АК с блокатором ренин-ангиотензиновой системы. В случае недостаточного ответа или в зависимости от наличия сопутствующей патологии возможно назначение селективных β1-адреноблокаторов и тиазидных или тиазидоподобных диуретиков, однако их рутинное применение у пациентов с ХОБЛ не рекомендовано с учетом возможных побочных эффектов [41,43].
Фибрилляция предсердий является не только фактором риска развития инсульта и сердечной недостаточности, но и проявлением гипертонической кардиопатии [44]. Поэтому в рекомендациях 2018 г. подчеркивается важность обследования всех больных с фибрилляцией предсердий для исключения АГ (IC). В качестве антигипертензивного лечения следует использовать блокатор ренин-ангиотензинвой системы, который можно сочетать с ББ или недигидропиридиновым АК в случае необходимости контроля частоты желудочковых сокращений (рис. 6) (IIaB). В новой версии документа раздел, посвященный АГ и фибрилляции предсердий, дополнен информацией о применении пероральных антикоагулянтов у пациентов с АГ. Профилактику инсульта больным АГ и фибрилляцией предсердий эксперты рекомендуют проводить с помощью пероральных антикоагулянтов, если число баллов по шкале CHA2DS2-VASc составляет ≥2 у мужчин и ≥3 у женщин (IA) [45,46]. Назначение пероральных антикоагулянтов больным с фибрилляцией предсердий целесообразно даже в тех случаях, когда АГ является единственным дополнительным фактором риска, а число баллов по шкале CHA2DS2-VASc составляет 1 (IIаВ) [45,46]. У пациентов с неконтролируемой АГ (САД ≥180 мм рт. ст. и/или ДАД ≥100 мм рт. ст.) следует с осторожностью подходить к назначению антикоагулянтов из-за высокого риска церебральных кровоизлияний [45]. При назначении антикоагулянтов необходимо предпринять меры для снижения уровня САД <140 мм рт. ст. и оценить возможность достижения целевого САД <130 мм рт. ст. (IIаВ) [45].
Известно, что сексуальная дисфункция, которая часто встречается у пациентов с АГ, приводит не только к ухудшению качества жизни, но и к снижению приверженности к лечению или полному отказу от приема антигипертензивных препаратов [47]. В рекомендациях 2018 г. подчеркивается важность сбора анамнеза о сексуальных нарушениях у всех больных АГ не только в начале лечения, но и в ходе наблюдения. Особое внимание следует обращать на их возможную связь с нежеланием принимать назначенную терапию или с низкой приверженностью к лечению. При наличии сексуальной дисфункции у мужчин рекомендуется избегать препаратов, назначение которых может быть ассоциировано с этим нежелательным эффектом (например, ББ без вазодилатирующих свойств и тиазидных или тиазидоподобных диуретиков), если только их использование не является необходимым по другим показаниям. У женщин среднего и старшего возраста не было выявлено ассоциации уровней АД или приема антигипертензивных препаратов с сексуальной дисфункцией [48]. У пациентов с высоким сердечно-сосудистым риском и тяжелой неконтролируемой АГ представляется разумным отсрочить сексуальную активность до стабилизации состояния, после чего может быть начато лечение по поводу эректильной дисфункции [49]. Препаратами выбора для лечения сексуальной дисфункции остаются ингибиторы фосфодиэстеразы-5.
Еще один новый раздел в рекомендациях 2018 г. посвящен АГ и противоопухолевой терапии. Необхо ди мость его включения в рекомендации обусловлена несколькими факторами: распространенностью повышенного АД среди пациентов с онкологическими заболеваниями (до трети пациентов) и прессорным эффектом некоторых противоопухолевых препаратов, в частности ингибиторов фактора роста эндотелия сосудов (бевацизумаб, сорафениб, сунитиниб и пазопаниб) и ингибиторов протеасом (карфизомиб) [50,51]. Реко мендуется контролировать офисное АД еженедельно в течение первого цикла терапии и каждые 2-3 недели в дальнейшем, так как повышение АД обычно наблюдается у ≤30% пациентов в течение первого месяца после начала лечения [52]. В дальнейшем после завершения первого цикла противоопухолевого лечения следует измерять АД во время посещения врача или с помощью СКАД в случае стабильных цифр АД. При развитии АГ (≥140/90 мм рт. ст.) или повышении ДАД на ≥20 мм рт. ст. по сравнению с исходным уровнем необходимо назначить или оптимизировать антигипертензивную терапию с помощью блокаторов ренин-ангиотензиновой системы и/или АК.
В рекомендациях 2018 г. существенно расширен раздел по ведению пациентов с АГ в периоперационном периоде. В отличие от предыдущей версии, в новом документе при впервые выявленной АГ перед плановым хирургическим вмешательством рекомендуется провести обследование не только с целью оценки сердечно-сосудистого риска, но и для выявления ПООГ (IC). У пациентов с АГ 1 и 2 степени можно не откладывать проведение некардиохирургической операции (IIbC). Однако при уровне САД ≥180 мм рт. ст. и/или ДАД ≥110 мм рт. ст. желательно отложить вмешательство, если оно не является экстренным, до достижения контроля АД. Целесообразно отменить блокаторы ренин-ангиотензиновой системы перед хирургическим вмешательством (IIаС) в отличие от ББ и препаратов центрального действия (клонидин). Внезапная отмена последних потенциально опасна и не рекомендуется (IIIВ). Следует избегать выраженных колебаний АД в периоперационном периоде (IC).
Учитывая опубликованные данные о влиянии сахароснижающих препаратов на уровень АД, в рекомендациях 2018 г. появился новый раздел, посвященный этому вопросу. Ингибиторы натрий-глюкозного ко транс портера 2-го типа эмпаглифлозин и канаглифлозин способствуют снижению АД вне зависимости от влияния массы тела на этот показатель, снижают риск развития сердечной недостаточности и смерти от любых и сердечно-сосудистых причин, а также оказывают нефропротективное действие [53,54]. Применение ингибиторов дипептидилпептидазы-4 и агонистов глюкагоноподобного пептида-1 также приводило к некоторому снижению АД [55, 56].
В новой версии рекомендаций 2018 г. отражены изменения позиций экспертов относительно коррекции сопутствующих сердечно-сосудистых факторов риска [57]. Так, пациентам с АГ и очень высоким сердечнососудистым риском следует назначать статины для достижения целевого уровня липопротеидов низкой плотности (ЛНП) <1,8 ммоль/л или снижения на ≥50% от исходного уровня 1,8-3,5 ммоль/л (IB); с высоким риском – для достижения ЛНП <2,6 ммоль/л или снижения на ≥50% от исходного уровня 2,6-5,2 ммоль/л (IB). Пациентам с АГ и низким/средним риском целесообразно назначить статины для достижения целевого уровня ЛНП <3 ммоль/л (IIaC), так как согласно результатам исследований JUPITER и HOPE-3 это позволяет снизить частоту развития сердечно-сосудистых событий у этой категории больных на 24-44% [58,59].
Важным отличием новой версии рекомендаций является изменение позиций аспирина, назначение которого для первичной профилактики пациентам без сердечно-сосудистых заболеваний не рекомендовано (IIIB). Низкие дозы аспирина, как и прежде, рекомендованы с целью вторичной профилактики у пациентов с АГ (IA).
Нерешенные вопросы
Эксперты сформулировали новый перечень нерешенных вопросов (табл. 4). Возможно, ответы на них будут получены и представлены уже в следующей версии рекомендаций.
| Примечание: ХОБЛ – хроническая обструктивная болезнь легких; SCORE – Systematic COronary Risk Evaluation |
| Измерение АД |
| • Оптимальная программа скрининга населения для выявления АГ |
| • Оптимальный метод измерения АД у пациентов с ФП |
| • Польза для прогнозирования сердечно-сосудистого риска при дополнении офисного измерения АД данными СМАД и/или СКАД |
| • Дополнительное значение центрального АД по сравнению с периферическим АД при оценке риска и его уменьшении на фоне лечения |
| Клиническая оценка пациентов с АГ |
| • Дополнительная польза оценки ПООГ при АГ в реклассификации сердечно-сосудистого риска у пациентов с АГ? |
| Границы и целевой уровень АД |
| • Оптимальные целевые значения САД/ДАД у более молодых пациентов с АГ |
| • Оптимальные целевые значения САД/ДАД при определенных условиях (например, у пациентов с диабетом, ХБП, после инсульта) |
| • Оптимальные целевые значения САД/ДАД по данным СКАД и СМАД |
| • Оптимальные целевые значения САД/ДАД для пациентов с различными исходными уровнями сердечно-сосудистого риска |
| Необходимость в результатах дополнительных исследований |
| • Оценка преимуществ лечения АД у пожилых людей |
| • Сравнение стационарного и амбулаторного ведения |
| • Сравнение лечения для контроля АД и уменьшения ПООГ, особенно у молодых людей |
| • У лиц с высоким нормальным АД |
| • У пациентов с резистентной гипертонией |
| Стратегии лечения гипертонии |
| • Воздействие стратегии лечения одной таблеткой против нескольких на клинические исходы, приверженность к лечению и контроль АД |
| • Сравнение исходов между стратегиями лечения на основе первоначальной монотерапии против начальной комбинированной терапии |
| • Сравнение исходов лечения АД с классическими и вазодилатирующими β-адреноблокаторами |
| • Сравнение исходов лечения на основе тиазидных и тиазидоподобных диуретиков? |
| • Оптимальное лечение гипертонии в разных этнических группах? |
| • Защитный эффект антигипертензивной терапии у пациентов с когнитивной дисфункцией или слабоумием |
| • Роль антигипертензивной терапии в лечении гипертонии белого халата и маскированной гипертонии |
Заключение
Процесс непрерывного обновления наших знаний, поступление новых доказательств и обобщение ранее полученных данных в гипертензиологии позволили в новых рекомендациях 2018 г. расставить акценты, добавить детали к “портрету артериальной гипертонии” и задать новые актуальные вопросы.
Используемые источники
- Aburto NJ, Ziolkovska A, Hooper L et al. Effect of lower sodium intake on health: systematic review and meta-analyses. BMJ 2013; 346:f1326.
- Brunström M, Carlberg B. Effect of antihypertensive treatment at different blood pressure levels in patients with diabetes mellitus: systematic review and meta-analyses. BMJ 2016; 352:i717.
- Emdin CA, Rahimi K, Neal B et al. Blood pressure lowering in type 2 diabetes: a systematic review and meta-analysis. JAMA 2015;313(6):603–15.
- Ettehad D, Emdin CA, Kiran A et al. Blood pressure lowering for prevention of cardiovascular disease and death: a systematic review and meta-analysis. Lancet 2016;387(10022):957–67.
- Flegal KM, Kit BK, Orpana H, Graubard BI. Association of all-cause mortality with overweight and obesity using standard body mass index categories: a systematic review and meta-analysis. JAMA 2013;309(1):71–82.
- He FJ, Li J, Macgregor GA. Effect of longer term modest salt reduction on blood pressure: Cochrane systematic review and meta-analysis of randomised trials. BMJ 2013;346:f1325.
- Lv J, Ehteshami P, Sarnak MJ, et al. Effects of intensive blood pressure lowering on the progression of chronic kidney disease: a systematic review and meta-analysis. CMAJ 2013;185(11):949–57.
- Malhotra R, Nguyen HA, Benavente O, et al. Association between more intensive vs less intensive blood pressure lowering and risk of mortality in chronic kidney disease stages 3 to 5: A systematic review and meta-analysis. JAMA Intern Med 2017;177(10):1498–505.
- Odden MC, McClure LA, Sawaya BP, et al. Achieved blood pressure and outcomes in the secondary prevention of small subcortical strokes trial. Hypertension 2016;67(1):63–69.
- Piper MA, Evans CV, Burda BU et al. Diagnostic and predictive accuracy of blood pressure screening methods with consideration of rescreening intervals: a systematic review for the U.S. Preventive Services Task Force. Ann Intern Med 2015;162(3):192–204.
- Sundström J, Arima H, Jackson R et al. Effects of blood pressure reduction in mild hypertension: a systematic review and meta-analysis. Ann Intern Med 2015;162(3):184–91.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood pressure lowering on out come incidence in hypertension: 2. Effects at different baselie and achieved blood pressure levels--overview and meta-analyses of randomized trials. J Hyper - tens 2014;32(12)2296–304.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood pressure lowering on outcome incidence in hypertension. 1. Overview, meta-analyses, and meta-regression analyses of randomized trials. J Hypertens 2014;32(12):2285–95.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood pressure lowering on outcome incidence in hypertension: 4. Effects of various classes of antihypertensive drugs -overview and meta-analyses. J Hypertens 2015;33(2):195–211.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood pressure-lowering treatment. 6. Prevention of heart failure and new-onset heart failure - meta-analyses of randomized trials. J Hypertens 2016;34(3):373–84.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood pressure lowering on outcome incidence in hypertension: 7. Effects of more vs. less intensive blood pressure lowering and different achieved blood pressure levels - updated overview and meta-analyses of randomized trials. J Hypertens 2016;34(4):613–22. Thomopoulos C, Parati G, Zanchetti A. Effects of blood-pressure-lowering treatment on outcome incidence in hypertension: 10 - Should blood pressure management differ in hypertensive patients with and without diabetes mellitus? Overview and meta-analyses of randomized trials. J Hypertens 2017;35(5):922–44.
- Tsai WC, Wu HY, Peng YS et al. Association of intensive blood pressure control and kidney disease progression in nondiabetic patients with chronic kidney disease: A systematic review and meta-analysis. JAMA Intern Med 2017;177(6): 792–9.
- Tucker KL, Sheppard JP, Stevens R et al. Self-monitoring of blood pressure in hypertension: A systematic review and individual patient data meta-analysis. PLoS Med 2017;14(9):e1002389.
- Williamson JD, Supiano MA, Applegate WB et al. Intensive vs standard blood pressure control and cardiovascular disease outcomes in adults aged ≥75 years: A randomized clinical trial. JAMA 2016;315(24):2673–82.
- Xie X, Atkins E, Lv J et al. Effects of intensive blood pressure lowering on cardiovascular and renal outcomes: updated systematic review and meta-analysis. Lancet 2016;387(10017):435–43.
- Yusuf S, Bosch J, Dagenais G et al. Cholesterol lowering in intermediate-risk persons without cardiovascular disease. N Engl J Med 2016;374(21):2021–31.
- Mancia G, Fagard R, Narkiewicz K et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension The Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). Eur Heart J 2013;34(28):2159–219.
- European Society of Hypertension-European Society of Cardiology Guidelines Committee. 2003 European Society of Hypertension-European Society of Car dio - logy guidelines for the management of arterial hypertension. J Hypertens 2003; 21(6):1011–53.
- Mancia G, De Backer G, Dominiczak A, et al. 2007 Guidelines for the Mana - gement of Arterial Hypertension: The Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2007;25(6):1105–87.
- Lurbe E, Agabiti-Rosei E, Cruickshank J, et al. 2016 European Society of Hypertension guidelines for the management of high blood pressure in children and adolescents. J. Hypertens 2016;34(10):1887–920.
- Böhm M, Schumacher H, Teo KK, et al. Achieved blood pressure and cardiovascular outcomes in high-risk patients: results from ONTARGET and TRANSCEND trials. Lancet 2017;389(10085):2226–37.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood-pressure-lowering treatment on outcome incidence. 12. Effects in individuals with high-normal and normal blood pressure: overview and meta-analyses of randomized trials. J Hypertens 2017;35(11):2150–60.
- Williamson JD, Supiano MA, Applegate WB, et al. Intensive vs standard blood pressure control and cardiovascular disease outcomes in adults aged ≥75 years: A randomized clinical trial. JAMA 2016;315(24):2673–82.
- Beckett N, Peters R, Leonetti G, et al. Subgroup and per-protocol analyses from the Hypertension in the Very Elderly Trial. J Hypertens 2014;32(7):1478–87.
- Lonn EM, Bosch J, López-Jaramillo P, et al. Blood-pressure lowering in intermediate-risk persons without cardiovascular disease. N Engl J Med 2016;374(21): 2009–20.
- Banegas JR, López-García E, Dallongeville J, et al. Achievement of treatment goals for primary prevention of cardiovascular disease in clinical practice across Europe: the EURIKA study. Eur Heart J 2011;32(17):2143–52.
- Chow CK, Teo KK, Rangarajan S, et al. Prevalence, awareness, treatment, and control of hypertension in rural and urban communities in high-, middle-, and low-income countries. JAMA 2013;310:959–68.
- Williams B, Mancia G, Spiering W, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J 2018;39(33):3021–104.
- Wald DS, Law M, Morris JK, et al. Combination therapy versus monotherapy in reducing blood pressure: meta-analysis on 11,000 participants from 42 trials. Am J Med 2009;122(3):290–300.
- Thomopoulos C, Parati G, Zanchetti A. Effects of blood-pressure-lowering treatment in hypertension: 9. Discontinuations for adverse events attributed to different classes of antihypertensive drugs: meta-analyses of randomized trials. J Hyper tens 2016;34(10):1921–32.
- Rimoldi SF, Scherrer U, Messerli FH. Secondary arterial hypertension: when, who, and how to screen? Eur Heart J 2014;35(19):1245–54.
- van den Born B-JH, Lip GYH, Brguljan-Hitij J, et al. ESC Council on hypertension position document on the management of hypertensive emergencies. Eur Heart J Cardiovasc Pharmacother 2019;5(1):37–46.
- ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial. Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA 2002;288(23):2981–97.
- Wright JT, Dunn JK, Cutler JA, et al. Outcomes in hypertensive black and nonblack patients treated with chlorthalidone, amlodipine, and lisinopril. JAMA 2005;293(13):1595–608.
- Farsang C, Kiss I, Tykarski A, Narkiewicz K. Treatment of hypertension in patients with chronic obstructive pulmonary disease. European Society of Hyper ten - sion Scientific Newsletter;2016(17):62.
- Baker JG, Wilcox RG. β-Blockers, heart disease and COPD: current controversies and uncertainties. Thorax 2017;72(3):271–6.
- Cazzola M, Noschese P, D’Amato G, Matera MG. The pharmacologic treatment of uncomplicated arterial hypertension in patients with airway dysfunction. Chest 2002;121(1):230–41.
- Lip GYH. Atrial fibrillation in patients with hypertension: trajectories of risk factors in yet another manifestation of hypertensive target organ damage. Hyper - tension 2016;68(3):544–5.
- Lip GYH, Coca A, Kahan T, et al. Hypertension and cardiac arrhythmias: a consensus document from the European Heart Rhythm Association (EHRA) and ESC Council on Hypertension, endorsed by the Heart Rhythm Society (HRS), Asia-Pacific Heart Rhythm Society (APHRS) and Sociedad Latinoamericana de Estimulación Cardíaca y Electrofisiología (SOLEACE). Europace 2017;19(6): 891–911.
- 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS | European Heart Journal | Oxford Academic. [https://academic.oup.com/eurheartj/article/37/38/2893/2334964].
- Viigimaa M, Doumas M, Vlachopoulos C, et al. Hypertension and sexual dysfunction: time to act. J Hypertens 2011;29(2):403–7.
- Foy CG, Newman JC, Berlowitz DR, et al. Blood pressure, and sexual activity and dysfunction in women with hypertension: baseline findings from the Systolic Blood Pressure Intervention Trial (SPRINT). J Sex Med 2016;13(9):1333–46.
- Shamloul R, Ghanem H. Erectile dysfunction. Lancet 2013;381(9861):153–65.
- Jain M, Townsend RR. Chemotherapy agents and hypertension: a focus on angiogenesis blockade. Curr Hypertens Rep 2007;9(4):3208.
- Abi Aad S, Pierce M, Barmaimon G et al. Hypertension induced by chemotherapeutic and immunosuppresive agents: a new challenge. Crit Rev Oncol Hematol 2015;93(1):28–35.
- Maitland ML, Bakris GL, Black HR, et al. Initial assessment, surveillance, and management of blood pressure in patients receiving vascular endothelial growth factor signaling pathway inhibitors. J Natl Cancer Inst 2010;102(9):596–604.
- Zinman B, Wanner C, Lachin JM, et al. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015; 373(22):2117–28.
- Neal B, Perkovic V, Mahaffey KW, et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. N Engl J Med 2017;377(7):644–57.
- Marso SP, Bain SC, Consoli A, et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2016;375(19):1834–44.
- Marso SP, Daniels GH, Brown-Frandsen K, et al. Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2016;375(4):311–22.
- 2016 ESC/EAS Guidelines for the Management of Dyslipidaemias: The Task Force for the Management of Dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS) Developed with the special contribution of the European Assocciation for Cardiovascular Prevention & Rehabilitation (EACPR). Atherosclerosis 2016;253:281–344.
- Ridker PM, Danielson E, Fonseca FAH, et al. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Engl J Med 2008; 359(21):2195–207.
- Yusuf S, Bosch J, Dagenais G, et al. Cholesterol lowering in intermediate-risk persons without cardiovascular disease. N Engl J Med 2016;374(21):2021–31.
