Неврологические осложнения инфекционного эндокардит
Неврологические осложнения развиваются у15-40% пациентов с инфекционным эндокардитом и в большинстве случаев обусловлены тромбоэмболией церебральных сосудов. Риск эмболий зависит от размеров и подвижности вегетаций. Среди возбудителей эндокардита сразвитием данных осложнений чаще других ассоциирован Staphylococcus aureus. При возникновении неврологических осложнений инфекционного эндокардита принципиально важным является привлечение специалистов различного профиля с целью более точной диагностики, определения тактики лечения и улучшения прогноза пациентов.
Неврологические осложнения развиваются у 15-40% пациентов с инфекционным эндокардитом (ИЭ). Чаще всего они возникают до начала антимикробной терапии (АМТ) и в первые дни после ее назначения, когда отмечается гемодинамическая нестабильность вегетаций [1,2]. Спектр неврологических осложнений ИЭ включает в себя ишемический и геморрагический инсульт, транзиторные ишемические атаки, бессимптомную церебральную эмболию, микотические аневризмы, абсцесс мозга, менингит, токсическую энцефалопатию и эпилепсию [3,4]. Среди возбудителей ИЭ с развитием неврологических осложнений чаще других ассоциирован Staphylococcus aureus. Это связано с тем, что при стафилококковой этиологии заболевания наблюдаются острое течение инфекционного процесса и изменения в свертывающей системе крови, способствующие возникновению тромбоэмболий [5,6]. Ишемическое или геморрагическое повреждение центральной нервной системы приводит к более чем двукратному повышению внутрибольничной летальности пациентов с ИЭ [7,8].
| Локализация | Частота, % |
|---|---|
| Селезенка | 40,8 |
| Головной мозг | 35,2 |
| Конечности | 25,3 |
| Почки | 22,5 |
| Коронарные артерии | 15,5 |
| Легкие | 8,5 |
| Центральная артерия сетчатки | 2,8 |
Структура и характеристика неврологических осложнений ИЭ
Тромбоэмболические проявления – одни из самых частых системных осложнений ИЭ. Например, в многоцентровом исследовании МАЭСТРО частота их составила 38,2% и превышала таковую иммунопатологических проявлений заболевания (11,1%) (рис. 1) [2]. При стафилококковой этиологии ИЭ тромбоэмболические осложнения возникают чаще, чем при стрептококковой или энтерококковой (рис. 2) [9]. Результаты ряда современных исследований свидетельствуют о том, что при ИЭ чаще всего развиваются тромбоэмболии сосудов селезенки и головного мозга (табл. 1) [3,9].
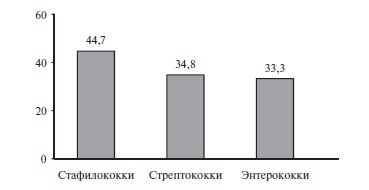
Ряд экспертов констатировали достоверно более высокую летальность в группе пациентов с тромбоэмболиями (39%, p<0,001) по сравнению с таковой у пациентов, у которых данные осложнения не отмечались (9%) [9].
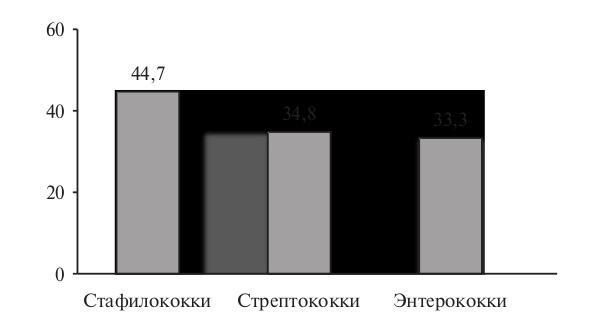
ИЭ может осложниться внутримозговым или субарахноидальным кровоизлияниями, сопровождающимися высокой летальностью [3,11]. Первичное внутримозговое кровоизлияние у больных с ИЭ наблюдается в 2,4% случаев [9]. Основной причиной вторичных геморрагических осложнений ИЭ является геморрагическая трансформация ишемического инсульта как следствие септической эмболии церебральных сосудов. К более редким причинам внутримозговых кровоизлияний относятся гнойный артериит, некроз сосудистой стенки, не приводящий к образованию аневризмы, а также сопутствующее назначение антиагрегантов и антикоагулянтов [8].
Микотические аневризмы встречаются у 2-5% пациентов с ИЭ (рис. 3) и могут быть обусловлены как прямым воздействием инфекционного агента на стенку сосуда, так и септической эмболией vasa vasorum [8]. Mикотические аневризмы чаще развиваются в бифуркациях дистальных отделов средней мозговой артерии. Окклюзия сосудов септическими эмболами, сопровождающаяся вторичным артериитом и деструкцией стенки сосуда, как правило, наблюдается при ИЭ, вызванным S. aureus, в то время как поражение сосудистой стенки vasa vasorum ассоциировано с выделением Streptococcus viridans [12]. Микотические аневризмы могут быть бессимптомными, а клинические проявления их варьируются от легкой головной боли до менингеального синдрома, расстройств чувствительности, поражения черепно-мозговых нервов, эпилептических приступов, внезапно развившегося гемипареза и гемианопсии [13].
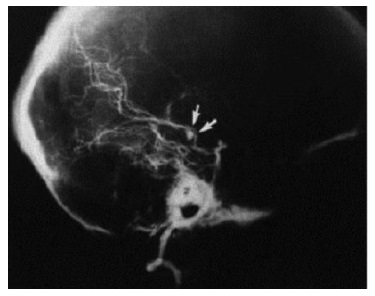
Менингит и менингоэнцефалит в последние десятилетия осложняют течение ИЭ примерно в 3% случаев. Они вызывают существенное ухудшение состояния больных и прогноза. Развитие воспаления мозговых оболочек связывают с воздействием высоко вирулентных возбудителей, присутствующих в составе тромботических масс, прежде всего S. aureus [9].
Абсцессы головного мозга при ИЭ встречаются редко. Они формируются в результате септических эмболий на фоне ограниченного инфекционного воспаления нервных волокон, которое может трансформиро ваться в микро- и/или макроабсцессы. Чаще развиваются микроабсцессы, которые могут проявляться головной болью, эпилептическими приступами и энцефалопатией [8].
Энцефалопатия является неспецифическим проявлением ИЭ и может быть объяснена наличием лихорадки, развитием острого нарушения мозгового кровообращения в лобных долях головного мозга, а также усугублением дисциркуляторной энцефалопатии у пожилых пациентов на фоне интоксикации. Развитие данного осложнения характеризуется изменением личности, возникновением галлюцинаций и параноидальных идей [9,10].
Ведение пациентов с неврологическими осложнениями инфекционного эндокардита
В рекомендациях Европейского общества кардиологов 2015 года подчеркивается важность лечения пациентов с ИЭ в специализированных центрах и привлечения мультидисциплинарной команды специалистов, которая способна определить тактику ведения пациентов (выбор комбинаций антимикробных препаратов и длительности АМТ, установление показаний для оперативного лечения), своевременно выявить осложнения заболевания и провести их коррекцию (табл. 2) [3,14].
| Показания | Время | Класс рекомендаций | Уровень доказательств |
|---|---|---|---|
| Примечание: *эхстренное хирургическое вмешательство – в течение 24 часов; **неотложное хирургическое вмешательство – в течение нескольких дней; ***отложить – через 1-2 недели АМТ | |||
| Сердечная недостаточность | |||
| Поражение аортального или митрального клапана с тяжелой острой регургитацией, обструкцией или фистулой, ведущее к рефрактерному отеку легких или кардиогенному шоку | Экстренно | I | B |
| Поражение аортального или митрального клапана с тяжелой острой регургитацией, обструкцией, вызывающее симптомы сердечной недостаточности или эхокардиографические признаки нарушенной гемодинамики | Неотложно | I | B |
| Неконтролируемая инфекция | |||
| Локально неконтролируемая инфекция (абсцесс, псевдоаневризма, фистула, растущая вегетация) | Неотложно | I | B |
| Инфекция, вызванная грибами или множественно-резистентными микроорганизмами | Неотложно/ отложить |
I | C |
| Персистирующие положительные результаты бактериологического исследования крови несмотря на назначение адекватной АМТ | Неотложно | IIа | B |
| Поражение протезированных клапанов, вызванное стафилококками и не-HACEK грамотрицательными микроорганизмами | Неотложно/ отложить |
IIа | C |
| Предотвращение тромбоэмболических осложнений | |||
| Поражение аортального или митрального клапана с персистирующими вегетациями размером более 10 мм после хотя бы одного эпизода эмболии несмотря на назначение адекватной АМТ | Неотложно | I | B |
| Поражение аортального или митрального клапана с вегетациями более 10 мм, ассоциированное с тяжелым стенозом или регургитацией и низким операционным риском | Неотложно | IIа | B |
| Поражение аортального или митрального клапана с изолированными очень большими вегетациями (более 30 мм) | Неотложно | IIа | B |
| Поражение аортального или митрального клапана с изолированными большими вегетациями (более 15 мм) и отсутствием других показаний для хирургического вмешательства | Неотложно | IIb | C |
Ключевую роль в прогнозировании тромбоэмболических осложнений играет эхокардиография, которая позволяет точно установить локализацию поражения, размеры микробных вегетаций, степень и динамику компенсации поврежденного клапана, что, в свою очередь, определяет дальнейшую тактику ведения пациентов с ИЭ. Факторы риска эмболий включают в себя размер и подвижность вегетаций, их локализацию на митральном клапане [15]. По данным современных исследований, высокий риск тромбоэмболических осложнений отмечается при наличии вегетаций диаметром более 10 мм, а самый высокий – при размере вегетаций 30 мм и более [16,17].
В многоцентровом исследовании МАЭСТРО чреспищеводная эхокардиография, позволяющей диагностировать ИЭ на начальных стадиях заболевания, использовалась в 15,8% случаев. Инфекционное поражение чаще всего локализовалось на митральном (43,6%) и аортальном (37,9%) клапанов. У 15,9% больных отмечалось сочетанное поражение клапанов, которое обусловливало повышенный риск развития тромбоэмболических осложнений [18].
В последние годы увеличилось количество публикаций, свидетельствующих о потенциальной роли в диагностике инфекционного поражения эндокарда компьютерной и магнитно-резонансной томографии. Однако на сегодняшний день эти методы исследования не вошли в рутинную практику, а их применение при ИЭ в основном ограничено диагностикой поражения головного мозга (табл. 3). Кроме того, использование контрастных веществ в ходе проведения данных визуализирующих методов исследования должно быть ограничено у пациентов с нефропатией и нестабильной гемодинамикой [3].
| Рекомендации | Класс рекомендаций | Уровень доказательств |
|---|---|---|
| Если после бессимптомной эмболии или транзиторной ишемической атаки кардиохирургическое вмешательство показано, оно должно быть выполнено без задержки | I | B |
| Нейрохирургическое вмешательство рекомендуется при очень больших, увеличивающихся или разрывающихся микотических аневризмах | I | C |
| После внутричерепного кровоизлияния хирургическое лечение должно быть отложено по крайней мере на 1 месяц | IIа | B |
| После развития ишемического инсульта вопрос о хирургическом лечении с целью коррекции сердечной недостаточности, устранения абсцесса или неконтролируемой инфекции должен быть немедленно рассмотрен при сохраняющихся показаниях к его проведению при отсутствии комы и исключении внутричерепного кровоизлияния с помощью КТ или МРТ | IIа | B |
| При сохранении подозрения на развитие микотических аневризм и отрицательных результатах неинвазивных визуализирующих методов рекомендуется проведение ангиографии | IIа | B |
В соответствии с рекомендациями Европейского общества кардиологов наибольшее значение для снижения риска тромбоэмболических осложнений имеет раннее назначение адекватной АМТ [3]. Вместе с тем, согласно результатам исследования МАЭСТРО, стартовая АМТ при ИЭ была эффективной лишь в 51,3% случаев [1]. Следует отметить, что с учетом низкой частоты выделения этиологически значимых возбудителей при ИЭ в Российской Федерации (по данным исследования МАЭСТРО – 35,5%) важное значение для обеспечения эффективности АМТ имеет выявление потенциальных факторов риска, таких как инъекционная наркомания, кардиохирургические вмешательства и инвазивные медицинские манипуляции, которые обусловливают ведущую роль S. aureus в этиологической структуре за бо левания [1,2].
Важно подчеркнуть, что применение антитромботических лекарственных средств в активную фазу инфекционного процесса в настоящее время не подкреплено данными крупных клинических исследований и оправдано лишь при поражении протезированных клапанов, частота вовлечения которых на сегодняшний день не превышает 15%. Кроме того, в случае поражения протезированных клапанов увеличивается вероятность выделения коагулазонегативных стафилококков, что также может способствовать нарушению реологических свойств крови [3].
Целесообразность выполнения раннего хирургического вмешательства для предотвращения тромбоэмболических осложнений у пациентов с ИЭ широко обсуждается в экспертном сообществе. В настоящее время рекомендуется индивидуально подходить к решению этого вопроса, принимая во внимание степень поражения клапанного аппарата сердца и динамику ответа на АМТ (табл. 2) [3,19].
Хирургическое лечение микотических аневризм, включающее клипирование или эндоваскулярную эмболизацию, представляет собой одну из наиболее сложных процедур даже в современных условиях. При отсутствии возможности хирургического вмешательства терапия должна включать в себя длительный курс назначения антимикробных препаратов, что в подавляющем большинстве случаев позволяет уменьшить размер микотических аневризм [18].
Заключение
Проблема неврологических осложнений ИЭ остается одной из наиболее серьезных в кардионеврологии. Для ее успешного решения необходимы усилия широкого круга специалистов – кардиологов, кардиохирургов, неврологов, нейрохирургов, врачей функциональной диагностики и других. Современная диагностика ИЭ основывается на предложенных в 1994 г. и впоследствии дополненных Duke критериев, согласно которым ключевая роль отводится бактериологическому исследованию крови и визуализирующим методам диагностики. Вместе с тем, в Российской Федерации отмечается чрезвычайно низкая частота выделения этиологически значимых возбудителей из крови, а также недостаточно широкое использование чреспищеводной эхокардиографии, позволяющей диагностировать поражение клапанов сердца на начальных стадиях заболевания. Ранняя диагностика ИЭ и назначение адекватной АМТ способствуют максимальному сокращению риска неврологических осложнений. В случае развития таких осложнений показания к хирургическому лечению сохраняются, но потенциальная польза его должна быть сопоставлена с операционным риском и послеоперационным прогнозом.
Среди неврологических осложнений ИЭ чаще всего встречается ишемическое поражение головного мозга вследствие тромбоэмболии церебральных сосудов. Наиболее высокий риск тромбоэмболических осложнений наблюдается в первые 2 недели заболевания и ассоциирован с размерами и подвижностью вегетаций, наличием в анамнезе эпизода тромбоэмболии, а также видом этиологически значимого микроорганизма. Знание вариантов поражения нервной системы при ИЭ, которое может маскировать основное заболевание, позволит в более ранние сроки поставить правильный диагноз и своевременно назначить лечение, способствующее снижению смертности и улучшению прогноза у данной категории пациентов.
Повышение эффективности ведения пациентов с ИЭ невозможно без знания особенностей диагностики и подходов к терапии, четких представлений об этиологической структуре, учета глобальных и локальных данных об антимикробной резистентности наиболее часто встречающихся возбудителей. В этой связи чрезвычайно важной представляется совместная работа клиникомикробиологических лабораторий, направленная на получение достоверных данных о возбудителях и их чувствительности к антимикробным препаратам, и врачей, осуществляющих лечение пациентов с ИЭ. Одним из методов получения подобной информации является участие научных работников и практикующих врачей в многоцентровых клинических исследованиях, проводимых по единому протоколу.
Используемые источники
- Данилов А.И., Козлов Р.С., Козлов С.Н. и др. Особенности антимикробнойтерапии инфекционного эндокардита в Российской Федерации.Антибиотики и химиотерапия 2018;63(9-10):48-52 [Danilov AI, Kozlov RS,Kozlov SN, et al. Features of antimicrobial therapy of infective endocarditis in theRussian Federation. Аntibiotiki i khimioterapiya 2018;63(9-10):48-52 (In Russ.)].
- Данилов А.И., Осипенкова Т.А., Нанкевич И.Н. Современные особенностиклинической картины инфекционного эндокардита в РоссийскойФедерации. Трудный пациент 2019;17(6-7):6-8 [Danilov AI, Osipenkova TA,Ninkevich IN. Modern features of infectious endocarditis in the RussianFederation. Trudnyj patsient 2019;17(6-7):6-8 (In Russ.)].
- Habib G, Lancellotti P, Antunes MJ, et al. 2015 ESC Guidelines for the manage-ment of infective endocarditis: The Task Force for the Management of InfectiveEndocarditis of the European Society of Cardiology (ESC). Endorsed by:European Association for Cardio-Thoracic Surgery (EACTS), the EuropeanAssociation of Nuclear Medicine (EANM). Europ Heart J 2015;36(44):3075-128.
- Baddour LM, Wilson WR, Bayer AS, et al. Infective endocarditis: diagnosis,antimicrobial therapy, and management of complications: a statement for health-care professionals from the Committee on Rheumatic Fever, Endocarditis, andKawasaki Disease, Council on Cardiovascular Disease in the Young, and theCouncils on Clinical Cardiology, Stroke, and Cardiovascular Surgery andAnesthesia, American Heart Association: endorsed by the Infectious DiseasesSociety of America. Circulation 2005;111(23):394-434.
- Abdallah L, Habib G, Remadi JP, et al. Comparison of prognosis of Staphy-lococcusaureusleft-sided prosthetic endocarditis and prosthetic endocarditiscaused by other pathogens. Arch Cardiovasc Dis 2016;109(10):542-9.
- Yombi JC, Yuma SN, Pasguet A, et al. Staphylococcal versus streptococcal infec-tive endocarditis in a tertiary hospital in Belgium: epidemiology, clinical charac-teristics and outcome. Acta Clinica Belgica 2017;4:1-7.
- Пономарева Е.Ю., Ландфанг С.В. Анализ госпитальной летальности приинфекционном эндокардите. Фундаментальные исследования 2015;1-6:1222-5 [Ponomareva EYu, Landfang SV. Analysis of the in-hospital mortality ininfective endocarditis. Fundamental'nye issledovaniya 2015;1-6:1222-5 (InRuss.)].
- Саковец Т.В., Хузина Г.Р. Неврологические осложнения при инфекцион-ном эндокардите: клиника, диагностика, лечение. Практическая медицина2018;16(10):25-9 [Sakovets TV, Khuzina GR. Neurological complications ofinfective endocarditis. Prakticheskaya meditsina 2018;16(10):25-9 (In Russ.)].
- Тюрин В.П. Инфекционные эндокардиты. Москва, 2001 [Tuyrin VP. Infective endocarditis. Moscow, 2001 (In Russ.)].
- Carneiro TS, Awtry E, Dobrilovic N, et al. Neurological complications of endo-carditis: a multidisciplinary review with focus on surgical decision making.Seminars Neurol 2019; 39(04): 495-506..
- Morotti A, Gamba M, Costa P, et al. Infective endocarditis presenting withintracranial bleeding. J Emerg Med 2016;51(1):50-4.
- Соболева В.Н., Гордеев И.Г., Волов Н.А., Отарова С.М. Инфекционныйэндокардит и микотические аневризмы (клинические наблюдения).Терапевт 2013;7:65-70 [Soboleva VN, Gordeev IG, Volov NA, Otarova SM.Infective endocarditis and mycotic aneurisms (clinical cases). Terapevt 2013;7:65-70 (In Russ.)].
- Glucksman A., Naut E. Cerebral aneurysm from cardiobacterium hominis endo-carditis. Connecticut Med 2016;80(5):297-300.
- Chambers J, Sandoe J, Ray S, et al. The infective endocarditis team: recommen-dations from an international working group. Heart 2014;100(7):524-27.
- Toyoda N, Chikwe J, Itagaki S, et al. Trends in infective endocarditis inCalifornia and New York State, 1998-2013. J Amer Med Ass 2017;317(16):1652-60.
- Berdejo J, Shibayama K, Harada K, et al. Evaluation of vegetation size and itsrelationship with embolism in infective endocarditis: a real-time 3-dimensionaltransesophageal echocardiography study. Circulation Cardiovasc Imag2013;7(1):149-54.
- Fukuda W., K. Daitoku, M. Minakawa et al. Management of infective endocardi-tis with cerebral complications. Annals of Thoracic and Cardiovascular Surgery2014; 20(3):229-236.
- Данилов А.И., Абраменкова Н.Ю., Милягин В.А., Осипенкова Т.А.Эхокардиографическое исследование пациентов с инфекционным эндокар-дитом в Российской Федерации. Вестник Смоленской государственноймедицинской академии 2019; 18(1):95-98 [Danilov AI, Abramenkova Nyu,Milyagin VA, Osipenkova TA. Echocardiography in patients with infective endo-carditis in the Russian Federation. Vestnik Smolenskoj gosudarstvennoj meditsin-skoj akademii 2019; 18(1):95-98 (In Russ.)].
- Hodges KE, Hussain ST, Stewart WJ, Pettersson GB. Surgical management ofinfective endocarditis complicated by ischemic stroke. J Cardiol Surg 2017;32(1):9-1
