Преимущество комбинированной терапии нестероидным противовоспалительным препаратом и миорелаксантом при боли в спине
Боль – важнейший физиологический механизм защиты организма от различных неблагоприятных воздействий. Дифференциальная диагностика типов боли имеет очень важное значение для выбора тактики терапии. Основная цель терапии боли в нижней части спины (БНЧС) – быстрое купирование болевого синдрома и возвращение пациента к обычному образу жизни. Комбинированная терапия нестероидным противовоспалительным препаратом и миорелаксантом дает более быстрый терапевтический эффект у пациентов с БНЧС, обусловленной мышечно-тоническим синдромом, и позволяет быстрее восстановить нормальную активность.
Боль является одной из самых распространенных жалоб на приеме у врача или у фармацевта при покупке лекарственного препарата [1]. Согласно многолетнему исследованию "Глобальное бремя болезни" (1990-2013) среди основных 10 причин, снижающих качество жизни населения, боль в нижней части спины (БНЧС) занимает первое место и опережает по распространенности другие болевые синдромы, в том числе боль в шейном отделе позвоночника (4-е место), мигрень (6-е место), другие скелетно-мышечные боли (10-е место). БНЧС является одной из основных причин ограничения или утраты трудоспособности [2,3]. До 25-30% людей, испытывающих БНЧС, обращаются к врачу, в то время как остальные занимаются самолечением [4] Согласно международным исследованиям каждый день до 5,6% взрослого населения в США испытывают БНЧС [5], а не менее 80% – хотя бы раз в жизни [6,7]. Болевой синдром одинаково часто встречается во всех возрастных и этнических группах независимо от культурных особенностей отдельно взятой страны.
Условный термин "боль в нижней части спины" подразумевает под собой боль, мышечное напряжение и/или скованность, локализующиеся между XII парой ребер и нижними ягодичными складками [8] Необходимо понимать, что БНЧС – это только симптом, а не клинический диагноз. Из-за высокой распространенности в популяции, влияния на трудоспособность и колоссальных расходов для общества БНЧС является актуальной медицинской проблемой и требует междисциплинарного подхода.
В 2010 г. в НИИ ревматологии им В.А. Насоновой было проведено эпидемиологическое исследование "Изучение БНЧС в клинической практике на амбулаторном приеме" [9], в котором проводилась оценка БНЧС в зависимости от ее длительности. В исследовании приняли участие 1300 пациентов трудоспособного возраста (средний возраст 39,3±10,3 лет), обратившихся амбулаторно на прием к терапевтам, неврологам и ревматологам. 324 пациента испытывали боль в спине. Чаще всего встречалась острая боль (49,4%), реже – подострая (17,9%) и хроническая (5,5%), а у 27,2% пациентов в день обращения БНЧС отсутствовала. Таким образом, именно острая боль была основной причиной обращения за медицинской помощью, причем если боль возникла повторно через 6 и более месяцев, она расценивалась как рецидив острой боли, если возникла в течение менее 6 месяцев – обострение хронической боли.
С практической точки зрения выделяют три основные причины БНЧС: 1) неспецифическая (скелетно-мышечная) боль; 2) специфическая боль, связанная с "серьезной патологией" (опухоли, травмы, инфекции и др.); 3) боль, вызванная компрессионной радикулопатией или стенозом спинномозгового канала. Чаще всего (в 85% случаев) в клинической практике встречается неспецифическая (скелетно-мышечная) боль. Компрессионная радикулопатия и поясничный стеноз отмечаются в 4–7% случаев, в то время как доля других причин, включая опухоль, травму, инфекции, ревматическое поражение, в целом составляет менее 7% от всех случаев БНЧС [10-12].
Дифференциальная диагностика типов боли является необходимым и важным этапом в обследовании больного и выборе дальнейшей тактики терапии. В этом врачу помогает система "красных флажков" или "симптомов опасности". Это комплекс симптомов, которые позволяют усомниться в доброкачественном (неспецифическом, первичном) характере боли и предположить наличие серьезного заболевания – онкологического или инфекционного и др., а также требуют дальнейшего обследования пациента. Для выявления подобных симптомов необходимо уточнить анамнестические данные, характер болевого синдрома, наличие или отсутствие выраженных ограничений движения, оценить данные объективного осмотра, а также эффективность и адекватность ранее проводимой терапии.
К "красным флажкам" при болях в спине относят следующие:- возникновение боли в возрасте менее 20 или старше 55 лет,
- перенесенная в недавнем прошлом травма спины,
- нарастание боли с течением времени,
- отсутствие облегчения боли или ее усиление после пребывания в положении лежа,
- перенесенные онкологические заболевания,
- длительный прием глюкокортикостероидов, в том числе в виде ингаляций,
- злоупотребление наркотическими препаратами,
- длительное недомогание,
- лихорадка,
- необъяснимое снижение массы тела,
- наличие очагового неврологического дефицита.
Наиболее частым источником неспецифической боли в спине являются мышцы спины, межпозвоночный диск (нервные окончания обнаружены в наружной трети фиброзного кольца), фасеточные суставы, крестцово-подвздошные суставы [11]. У одного и того же пациента источником боли может быть поражение нескольких структур, а выделить ведущую причину зачастую сложно. Некоторые авторы считают, что поражение мышц (спазм, небольшие травмы, растяжение) является наиболее частой причиной боли в спине [13]. Спазмированная мышца не утрачивает свою функцию, однако при участии в определенных движениях, за которые отвечает мышца, она провоцирует болевой синдром.
Причинами неспецифической мышечно-скелетной боли могут быть чрезмерные физические нагрузки или сидячий образ жизни, переохлаждение, ожирение, стресс и др. Рецидивом боли в спине считается ее возобновление после 6 месяцев ремиссии. Выделяют ряд факторов, способных привести к рецидиву болевого синдрома: (1) неизбежное развитие дегенеративного процесса, приводящего к структурным изменениям хрящевой ткани; (2) ортопедические проблемы/анатомические аномалии скелета; (3) чрезмерные нагрузки и микротравматизация; (4) неадекватное лечение острой боли в дебюте заболевания; (5) "неадекватное" отношение пациента к болевому синдрому.
Основная цель терапии острой БНЧС – своевременное купирование болевого синдрома и возвращение пациента к обычному активному образу жизни. Важное значение имеет коррекция поведения и отношения человека к боли. С этой целью используется когнитивно-поведенческая психотерапия, направленная на осознание пациентом особенностей текущего состояния, определение наиболее значимых целей по изменению самочувствия [14]. Когнитивно-поведенческая психотерапия является ведущим методом терапии хронической боли, однако и при острых болевых состояниях важное значение имеют образование пациента (представление о природе болевого ощущения и возможности его модуляции, которая включает в себя примеры биологических, психологических и социальных факторов, оказывающих действие на восприятие боли); постановка целей; когнитивный компонент (выявление и преобразование связанных с болью знаний, представлений, страхов и ожиданий, а также развитие стратегий преодоления боли) [15]. Если пациент нуждается в покое для уменьшения болевого синдрома, то его необходимо мотивировать к более быстрому возвращению к активному образу жизни.
Препаратами выбора для лечения острой БНЧС, обусловленной мышечно-тоническим синдромом, являются нестероидные противовоспалительные препараты (НПВП) и миорелаксанты. Немедикаментозные методы при острой боли, в отличии от подострой и особенно хронической, оказались неэффективными. Мануальная терапия дает кратковременный и умеренный эффект. Лечебную физкультуру предлагают начинать после 2-6 недель. Монотерапия перестала быть стандартом лечения БНЧС, так как применение препаратов нескольких классов, действующих на разные патогенетические звенья болевого синдрома, обеспечивает наиболее эффективное и быстрое купирование боли.
В клинической практике при острой БНЧС чаще всего применяют НПВП, оказывающие противовоспалительное и выраженное обезболивающее действие. Эффективность препаратов этой группы при острой неспецифической боли в спине была неоднократно подтверждена в различных плацебо-контролируемых исследованиях [16-18]. Однако, применение НПВП ассоциируется с широким спектром нежелательных явлений как со стороны желудочно-кишечного тракта (ЖКТ), так и сердечно-сосудистой системы [19]. Поэтому вопросы оптимизации применения НПВП и снижения риска развития нежелательных явлений стали целью разработки новых подходов к лечению болевых синдромов, в частности комбинированной терапии.
В конце XX века препаратом с наилучшим соотношением эффективности и безопасности считали диклофенак – "золотой стандарт" обезболивающей терапии. Однако последующие клинические исследования свидетельствовали о том, что диклофенак все же достаточно часто вызывает осложнения со стороны ЖКТ и оказывает негативное действие на сердечно-сосудистую систему [20,21]. Мета-анализ 28 рандомизированных клинических исследований, в которых оценивали безопасность НПВП в отношении ЖКТ, показал, что наиболее эффективным и безопасным препаратом этой группы является ацеклофенак (Аэртал) [22]. Ацеклофенак хорошо известен практикующим врачам, проверен множеством клинических исследований и длительной реальной практикой и с успехом используется во многих странах мира уже более четверти века [23-28]. Рекомендованная доза препарата составляет 100 мг 2 раза в сутки строго после еды (утром и вечером). Максимальная рекомендованная доза – 200 мг в сутки.
Для усиления обезболивающего действия НПВП при мышечно-тонических расстройствах используют адьювантную терапию – миорелаксанты, которые снижают тонус скелетной мускулатуры [29]. Наиболее популярным и широко используемым препаратом из этой группы является толперизон (Мидокалм) – препарат центрального действия для нормализации тонуса в спазмированной мышце. Он обладает высокой безопасностью и может широко использоваться в различных возрастных группах, оказывает минимальное влияние на АД и не противопоказан при вождении автомобиля. Терапевтическая доза препарата для взрослых составляет 450 мг в сутки (по 150 мг 3 раза в сутки после еды). Длительность курса лечения варьируется от 2 до 3 недель, однако в отдельных случаях возможно более длительное применение препарата. Чтобы достичь более быстрого эффекта, препарат можно вводить по 1 мл (100 мг) внутримышечно два раза в сутки.
Эффективность комбинации НПВП и миорелаксанта при лечении болевого синдрома в спине была не раз доказана в различных исследованиях. М.Л. Кукушкин и соавт. (2017 г.) [30] оценили эффективность и безопасность совместного применения толперизона (Мидо кал ма) с НПВП и монотерапии НПВП в лечении острой неспецифической БНЧС. В рандомизированное двойное слепое исследование были включены 239 пациентов. Первые 5 дней пациенты получали толперизон или плацебо в виде инъекций с последующим их применением в таблетированной форме. Общая длительность терапии составила 14 дней. НПВП (диклофенак) применяли в обеих группах на протяжении всего исследования. По эффективности комбинированная терапия достоверно превосходила монотерапию НПВП. Через 14 дней в основной группе было отмечено уменьшение интенсивности болевого синдрома в покое на 76% и при движении на 73% (рис. 1). По безопасности две схемы терапии существенно не отличались. Основы ваясь на полученных результатах, толперизон в лекарственных формах для парентерального введения и приема внутрь можно считать эффективным и безопасным препаратом для комбинированной терапии у пациентов с острой БНЧС.
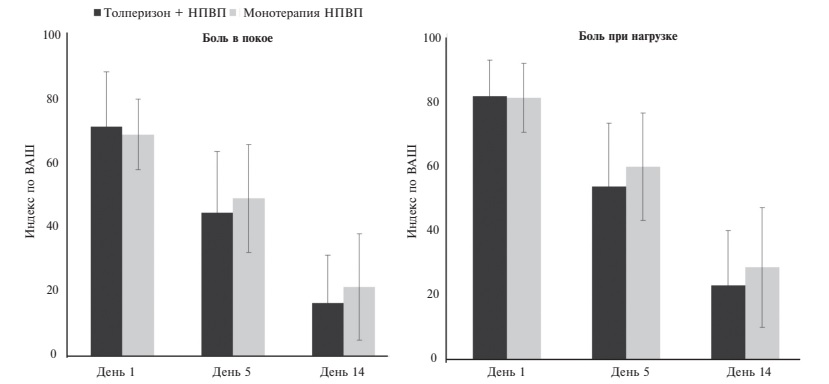
В.А. Парфенов и соавт. (2006 г.) [31] изучали эф фективность толперизона (Мидокалма) в комплексной терапии у амбулаторных пациентов с рефлекторным мышечно-тоническим и миофасциальным болевым синдромом в спине. В исследовании приняли участие 60 пациентов в возрасте 18-60 лет, которые были разделены на две группы. Пациенты контрольной группы (n=30) получали НПВП в сочетании с лечебной гимнастикой, а больные основной группы (n=30) дополни тельно принимали толперизон (Мидокалм) в дозе 150 мг 3 раза в сутки после еды. Положительный результат лечения был отмечен в обеих группах. Интенсивность болевого синдрома, которую оценивали с помощью визуальной аналоговой шкалы (ВАШ), в контрольной группе снизилась с 7,2±1,2 до 4,3±1,0 (p<0,01), в основной группе – с 7,3±1,8 до 3,4±1,2 (p<0,01). Однако средняя длительность временной нетрудоспособности в контрольной группе (17,7±3,3 дня) достоверно превышала таковую в основной (10,3±1,0 дня; p<0,05) (рис. 2). Авторы сделали вывод о том, что комбинировання терапия НПВП и толперизоном дает более быстрый терапевтический эффект у пациентов с БНЧС, обусловленной мышечно-тоническим синдромом, и позволяет им быстрее вернуться к повседневной активности.
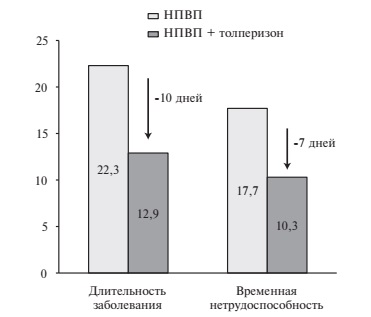
В отличие от других миорелаксантов, толперизон (Мидокалм) не обладает седативным эффектом, не вызывает мышечную слабость и не оказывает гипотензивное действие. Переносимость препарата в низкой (150 мг/сут) и высокой (450 мг/сут в три приема) дозах в течение 8 дней у добровольцев не отличалась [32], что позволяет рекомендовать наиболее эффективную дозировку 450 мг/сут для амбулаторной клинической практики.
Комбинированная терапия НПВП и миорелаксантом широко используется неврологами, ревматологами, терапевтами и врачами общей практики у пациентов с острой БНЧС и миофасциальным болевым синдромом различной локализации. Применение ацеклофенака (Аэртала), эффективного НПВП с незначительным воздействием на ЖКТ, в сочетании с толперизоном (Мидокалмом) представляется оптимальным для более быстрого, безопасного и эффективного купирования болевого синдрома.
Используемые источники
- Давыдов О.С. Распространенность болевых синдромов и их влияние на качество жизни в мире и России по данным исследования глобального бремени болезней за период с 1990 по 2013 гг. Российский журнал боли 2015;40(3-4):11-9 [Davydov OS. The prevalence of pain syndromes and their impact on quality of life in the world and Russia according to the data of the Global Burden of Disease Study in the period 1990 to 2013. Rossiyskiy Zhurnal Boli 2015;40(3–4):11–8 (In Russ.)].
- Vos T, Flaxman A, Naghavi M, et al. Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;380(9859):2163-96.
- Buchbinder R, Blyth FM, March LM, et al. Placing the global burden of low back pain in context. Best Pract Res Clin Rheumatol 2013;27(5):575-89
- Wolsko PM, Eisenberg DM, Davis RB, et al. Patterns and perceptions of care for treatment of back and neck pain: results of a national survey. Spine (Phila Pa 1976) 2003;28(3):292-8.
- Loney PL, Stratford PW. The prevalence of low back pain in adults: a methodo- logical review of the literature. Phys Ther 1999;79(4):384-96.
- van Tulder M, Koes B, Bombardier C. Low back pain. Best Pract Res Clin Rheumatol 2002;16(5):761-75.
- Hart LG, Deyo RA, Cherkin DC. Physician office visits for low back pain. Frequency, clinical evaluation, and treatment patterns from a U.S. national sur- vey. Spine (Phila Pa 1976) 1995;20(1):11-9.
- Поясничная боль. Предложения по ведению больных. ВОЗ 1999;115. Дубинина Т.В., Эрдес Ш.Ф. Причины поздней диагностики анкилозирую- щего спондилита в клинической практике. Научно-практическая ревмато- логия 2010;48(2):43-8 [Dubinina TV, Erdes SF. Reasons for late diagnosis of ankylosing spondylitis in clinical practice. Rheumatology Science and Practice 2010;48(2):43-8 (In Russ.)].
- Van Tulder MW, Becker A, Bekkering T, et al. European guidelines for the mana- gement of acute nonspecific low back pain in primary care. Eur Spine J 2006;15(Suppl. 2):S169-91.
- Chou R, Qaseem A, Snow V, et al. Diagnosis and treatment of low back pain: a joint clinical practice guideline from the American College of Physicians and the American Pain Society. Ann Intern Med 2007;147:478-91.
- Chou R, Atlas SJ, Stanos SP, et al. Nonsurgical interventional therapies for low back pain: a review of the evidence for an American Pain Society clinical practice guideline. Spine (Phila Pa 1976) 2009;34:1078-93.
- Deyo RA, Mirza SK, Turner JA, Martin BI. Overtreating chronic back pain: Time to back off? J Am Board Fam Med 2009;22:62-8
- Livneh H. Psychosocial adaptation to heart diseases: the role of coping strategies. J Rehabil 1999;65(3):24-33.
- Field BJ, Swarm RA. Chronic pain (Advances in psychotherapy - evidence-based practice). Hogrefe, 2008,
- Bogduk N, McGuirk B. Medical management of acute at chronic low back pain. Amsterdam: Elsevier; 2002, 94.
- Bogduk N. Why I pursue discogenic pain? In: Bogduk N (editor). Practice Guidelines for Spinal Diagnostic and Treatment Procedures. Intervetional Spine 2005,15-27.
- Burton AK, Balague F, Cardon G, et al, for the COST B13 Working Group on European Guidelines for Prevention in Low Back Pain. How to prevent low back pain? Best Pract Res Clin Rheumatol 2005;19:541-55.
- Gislason GH, Jacobsen S, Rasmussen JN, et al. Risk of death or reinfarction associated with the use of selective cyclooxygenase-2 inhibitors and nonselective nonsteroidal antiinflammatory drugs after acute myocardial infarction. Circulation 2006;113(25):2906-13.
- Каратеев А.Е. Оценка популяционной безопасности нестероидных проти- вовоспалительных препаратов в рамках общеевропейской программы SOS: фокус на ацеклофенак. Неврология, нейропсихиатрия, психосоматика 2020;12(2):109–13 [Karateev AE. Evaluation of the population safety of nonste- roidal anti-inflammatory drugs in the framework of the Pan-European SOS pro- gram: focus on aceclofenac. Neurology, Neuropsychiatry, Psychosomatics 2020;12(2):109-13 (In Russ.)].
- Cooper C, Chapurlat R, Al-Daghri N, et al. Safety of oral non-selective non-ste- roidal anti-inflammatory drugs in osteoarthritis: what does the literature say? Drugs Aging 2019;36(Suppl 1):15-24.
- Castellsague J, Riera-Guardia N, Calingaert B, et al. Individual NSAIDs and upper gastrointestinal complications: A systematic review and meta-analysis of observational studies (the SOS Project). Drug Saf 2012;35(12):1127-46.
- Dooley M, Spencer C, Dunn C. Aceclofenac: a reappraisal of its use in the mana- gement of pain and rheumatic disease. Drugs 2001;61(9):1351-78.
- Patel PB, Patel TK. Efficacy and safety of aceclofenac in osteoarthritis: A meta- analysis of randomized controlled trials. Eur J Rheumatol 2017;4(1):11-8.
- Лила А.М. Применение Аэртала (ацеклофенака) в клинической практике. РМЖ 2009;17(4):291-4 [Lila AM. The use of Aertal (aceclofenac) in clinical practice. RMZh 2009;17(4):291-4 (In Russ.)].
- Иголкина Е.В., Чичасова Н.В., Имаметдинова Г.Р. Ацеклофенак в лечении патологии опорнодвигательного аппарата. Современная ревматология 2017;11(3):99-105 [Igolkina EV, Chichasova NV, Imametdinova GR. Aceclofenac in the treatment of diseases of the locomotor apparatus. Modern Rheumatology Journal 2017;11(3):99-105 (In Russ.)].
- Yscla A. Aceclofenac and paracetamol in episiotomal pain. Drugs Exp Clin Res 1988;14(7):491-4.
- Насонова В.А. Ацеклофенак (Аэртал) в ревматологической практике. Тер архив 2005;77(5):87-90 [Nasonova VA. Aceclophenac (Aertal) in rheumatology practice. Terapevticheskij arkhiv 2005;77(5):87-90 (In Russ.)].
- Гилман А.Г. Миорелаксанты. В кн. Клиническая фармакология по Гудману и Гилману. Книга 1. Практика, 2006.
- Кукушкин М.Л., Брылев Л.В., Ласков В.Б. и др. Результаты рандомизиро- ванного двойного слепого параллельного исследования эффективности и безопасности применения толперизона у пациентов с острой неспецифиче- ской болью в нижней части спины. Журнал неврологии и психиатрии им. С.С. Корсакова. 2017;117(11):69-78 [Kukushkin ML, Brylev LV, Laskov VB, et al. Results of a randomized, double-blind, parallel study of the efficacy and safety of tolperisone in patients with acute nonspecific lower back pain. Zhurnal nevro- logii i psikhiatrii im. S.S. Korsakova 2017;117(11):69-78 (In Russ.)].
- Гурак С.В., Парфенов В.А., Борисов К.Н. Мидокалм в комплексной тера- пии острой поясничной боли. Боль 2006;3:27–30 [Gurak SV, Parfenov VA, Borisov KN. Midocalm for the treatment of acute low back pain. Pain 2006;3:27- 30 (In Russ.)].
- Dulin J, Kovacs L, Ramm S, et al. Evaluation of sedative effects of single and repeated doses of 50 mg and 150 mg tolperisone hydrochloride. Results of a pro- spective, randomized, double-blind, placebo-controlled trial. Pharmacopsychiat 1998;31:137-42.
