Влияние антигипертензивной терапии на поражение органов-мишеней у амбулаторных пациентов с артериальной гипертонией в условиях низкой приверженности к лечению
Изучение влияния применяемых в амбулаторной практике схем антигипертензивной терапии на показатели гемодинамики и органопротекции в условиях низкой приверженности к лечению.
В проспективное исследование были включены 280 пациентов трудоспособного возраста с впервые установленной артериальной гипертонией (АГ), у которых отсутствовали сердечно-сосудистые осложнения в анамнезе, но имелись дополнительные сердечно-сосудистые факторы риска. Пациенты получали назначенную лечащим врачом поликлиники антигипертензивную терапию (монотерапию или свободные или фиксированные двухкомпонентные и трехкомпонентные комбинации). Исходно и через год оценивали изменения АД, частоты сердечных сокращений, эхокардиографических показателей (массы миокарда и фракции выброса левого желудочка) и расчетной скорости клубочковой фильтрации (СКФ). Приверженность к лечению определяли в конце исследования на основании опроса пациентов.
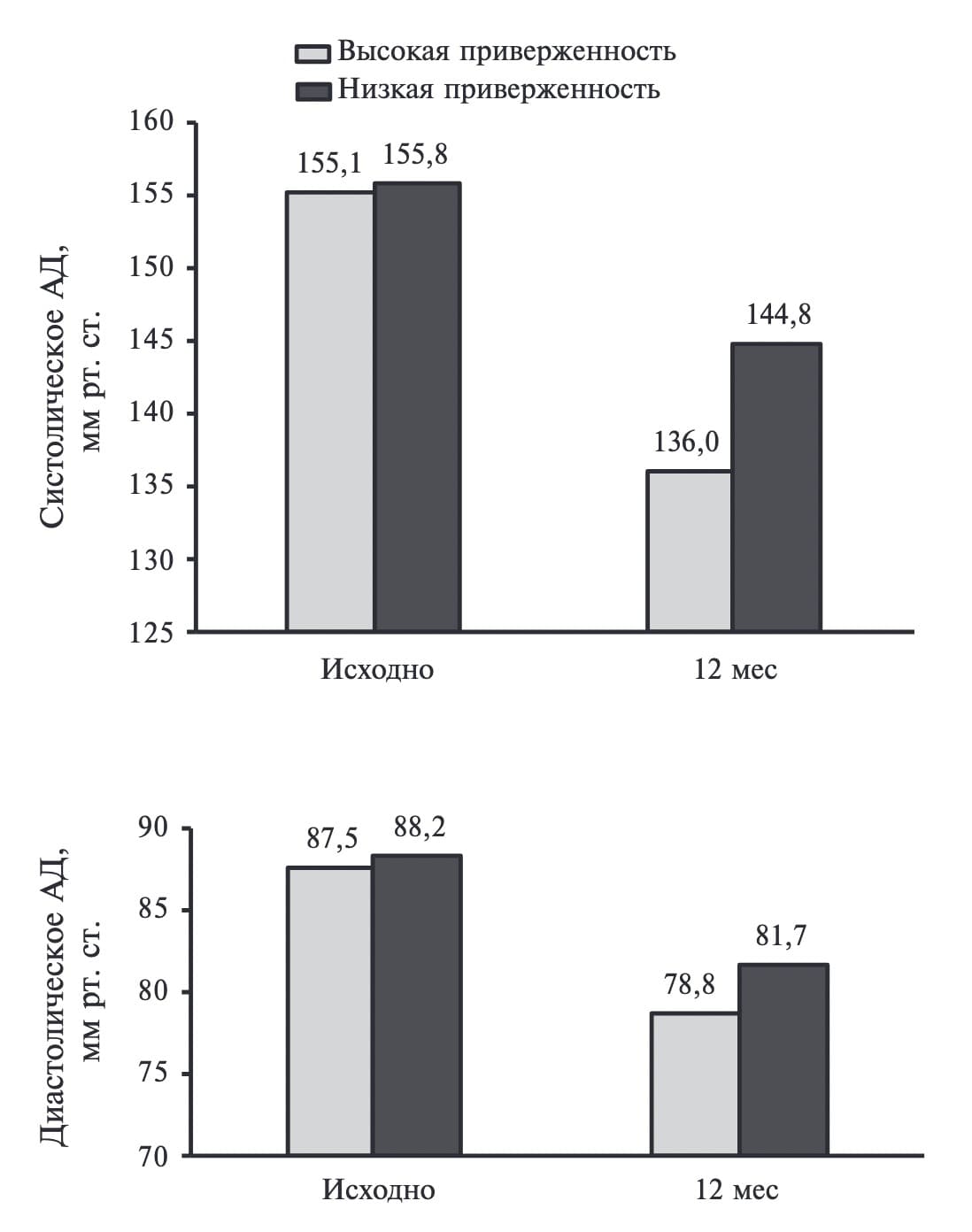
В течение года частично или полностью от антигипертензивной терапии отказались 71 (26,3%) из 280 пациентов. У больных, регулярно принимавших назначенные антигипертензивные препараты среднее офисное АД в течение года снизилось в большей степени (со 155,1/87,5 до 136,0/78,8 мм рт. ст.), чем у пациентов, не выполнявших рекомендации врача (со 155,8/88,2 до 144,8/81,7 мм рт. ст.). Масса миокарда левого желудочка в первой группе снизилась в среднем на 2,4%, а во второй увеличилась на 4,5%. Кроме того, высокая приверженность к лечению сопровождалась более значительным увеличением фракции выброса левого желудочка (на 3,2% и 0,5%, соответственно) и СКФ (на 11,0% и 7,7%).
Вне зависимости от выбранной схемы антигипертензивной терапии около четверти пациентов в течение года частично или полностью отказались от лечения, что ограничивало его гипотензивное, кардио- и нефропротективное действие.
На протяжении последних десятилетий сердечно-сосудиcтые заболевания остаются ведущей проблемой общественного здравоохранения. По данным ВОЗ, в 2019 г. сердечно-сосудистые заболевания были причиной 32% случаев смерти в мире [1]. Во время пандемии COVID-19 в Российской Федерации сердечно-сосудистая смертность увеличилась на 6,6%, а ее доля в структуре общей смертности достигла 47%. При этом сердечно-сосудистые заболевания в анамнезе повышают риск тяжелого течения новой коронавирусной инфекции и госпитализации в отделения реанимации и интенсивной терапии [2,3].
Основной модифицируемый фактор риска сердечно-сосудистых заболеваний – неконтролируемая артериальная гипертония (АГ), которая приводит к развитию хронической сердечной недостаточности (ХСН), ишемической болезни сердца (ИБС), хронической болезни почек (ХБП), снижению когнитивных функций [4-6], а также является причиной более половины случаев сердечно-сосудистой смерти [7]. В настоящее время в мире насчитывается 1,28 млрд пациентов с АГ [8]. Ожидается, что к 2025 г. каждый пятый житель планеты будет страдать АГ, а каждый десятый – умрет от сердечнососудистых заболеваний вследствие неадекватного контроля АД [9]. Основными причинами считают распространение сердечно-сосудистых факторов риска, в том числе гиподинамии, ожирения, никотиновой зависимости (включая курение электронных сигарет), и постарение населения [9-11].
Современные рекомендации по лечению АГ прежде всего основываются на оценке уровня АД [12], хотя критерии ее диагностики отличаются в разных странах. Например, в соответствии с рекомендациями Европейского общества кардиологов АГ была диагностирована у 50,2% из 20652 жителей Российской Федерации, а в соответствии с рекомендациями Американской коллегии кардиологов/Американской ассоциации сердца – у 72,1% [13]. По данным скринингового исследования, проводившегося в 80 странах, АГ была выявлена у 34,9% из 1,2 млн обследованных, причем АД было повышено у 17,3% участников, не получавших антигипертензивную терапию, и не контролировалось у 46,3% пациентов, которые принимали антигипертензивные препараты [14]. D. Prakash и соавт. при обследовании пациентов с впервые выявленной АГ выявили поражение одного органа-мишени в 27,3% случаев, двух – в 21,3%, трех – в 12,0% [15]. Сегодня остается неясным, при каких именно значениях АД происходит поражение органов-мишеней [16], однако увеличение систолического АД (САД) на 20 мм рт. ст. и диастолического АД (ДАД) на 10 мм рт. ст. сопровождалось двукратным ростом смертности от инфакта миокарда и инсульта [5,12].
При выборе стратегии антигипертензивной терапии помимо антигипертензивных свойств лекарственных средств (ЛС) следует учитывать их органопротективные свойства, т.е. способность предотвращать или минимизировать выраженность поражения органов-мишеней [17]. Основные классы антигипертензивных препаратов включают в себя ингибиторы ангиотензинпревращающего фермента (АПФ), блокаторы рецепторов ангиотензина II (БРА), β-адреноблокаторы, блокаторы кальциевых каналов и тиазидные и тиазидоподобные диуретики. Кроме того, для лечения АГ применяют α-адреноблокаторы и агонисты имидазолиновых рецепторов. Стартовую терапию часто начинают с комбинаций антигипертензивных средств, прежде всего фиксированных, что позволяет обеспечить синергизм их действия, подавить контррегуляторные механизмы повышения АД и, соответственно, достичь более выраженной стабилизации АД и улучшить переносимость лечения. При этом применение фиксированных комбинаций антигипертензивных препаратов (стратегия "одной таблетки") способствовало повышению приверженности к лечению на 20% по сравнению с таковой у пациентов, получавших те же препараты по отдельности [18,19]. P. Gupta и соавт. выявили связь между количеством принимаемых таблеток и частичным или полным отказом от лечения. Так, при приеме одной таблетки пациенты не выполняли рекомендации менее чем в 10% случаев, двух таблеток – в 20%, трех таблеток – в 40% [20].
Поскольку выбор класса антигипертензивных препаратов не влияет на приверженность к лечению пациентов с АГ, можно предположить, что возможные побочные эффекты медикаментозного лечения не являются основной причиной несоблюдения врачебных рекомендаций [21]. По данным мета-анализов, наиболее частая причина прекращения антигипертензивной терапии заключается в бессимптомном или легком течении АГ, которая не воспринимается пациентами как состояние, требующее регулярного лечения [22]. Низкая приверженность к лечению была отмечена у пациентов, которым антигипертензивную терапию рекомендовала до развития сердечно-сосудистых осложнений [23]. По данным мета-анализа, низкая приверженность к антигипертензивной терапии наблюдалась у 45,0% больных АГ и была основной причиной неадекватного контроля АД [24], который необходим для снижения глобального бремени сердечно-сосудистых заболеваний за счет предотвращения развития или прогрессирования поражения органов-мишеней [25,26].
Целью исследования было изучение влияния применяемых в амбулаторной практике стратегий антигипертензивной терапии на показатели гемодинамики и органопротекции в условиях низкой приверженности к лечению.
Материал и методы
В проспективное неинтервенционное исследование включали амбулаторных пациентов с впервые выявленной АГ 1-2 степени, у которых отсутствовали сердечно-сосудистые осложнения в анамнезе, но имелись дополнительные факторы риска (избыточная масса тела, гиподинамия, никотиновая зависимость, стрессовый образ жизни, нарушения углеводного и липидного обмена) и сопутствующие заболевания. Тяжесть коморбидности определяли по шкале Cumulative lllness Rating Scale (CIRS), которая предполагает оценку состояния каждой из 14 систем органов в баллах: 0 – отсутствие заболеваний соответствующей системы, 1 – легкое отклонение от нормы или перенесенное в прошлом заболевание, 2 – болезни, требующие назначения медикаментозной терапии, 3 – заболевание, ставшее причиной инвалидности, 4 – тяжелая органная недостаточность, требующая проведения неотложной терапии. Сумма баллов по шкале CIRS варьируется от 0 до 56.
Все пациенты дали письменное информированное согласие на участие в исследовании. Не позднее трех месяцев до начала наблюдения пациентам лечащим врачом на свое усмотрение был рекомендован прием антигипертензивных препаратов. Исходно и через 1 год анализировали АД и частоту сердечных сокращений, проводили суточное мониторирование АД (СМАД), эхокардиографию и рассчитывали скорость клубочковой фильтрации (СКФ) по формуле CKD-EPI. При эхокардиографии определяли динамику фракции выброса (ФВ) и массы миокарда (ММ) левого желудочка (ЛЖ). Анализ изучаемых показателей осуществлялся ретроспективно на основании медицинской документации. Кроме того, через 1 год лечащие врачи оценивали приверженность к лечению при опросе пациентов. Критериями низкой приверженности к лечению считали самостоятельную отмену или коррекцию схемы антигипертензивной терапии пациентом (частичный отказ) и полное несоблюдение врачебных рекомендаций (полный отказ).
Статистическая обработка данных проводилась с помощью программы IBM SPSS 27.0. Характер распределения количественных данных оценивался с помощью критерия Колмогорова-Смирнова. Количественные данные представлены в виде средних арифметических значений (M) и стандартных отклонений (SD). Для сравнения связанных групп пациентов по одному или нескольким признакам, распределение которых подчинялось закону нормального распределения, применяли однофакторный дисперсионный анализ с повторными измерениями (repeated measures ANOVA/ANOVARM). Три и более связанных групп сравнивали по качественному биноминальному признаку с помощью критерия Q Кохрена (Cochran's Q test).
Результаты
В проспективное исследование были включены 280 амбулаторных пациентов с впервые выявленной АД, в том числе 145 мужчин и 135 женщин в возрасте 50,5±4,2 лет. В зависимости от назначенной антигипертензивной терапии пациенты были распределены на 4 группы: 1-я (n=70) – монотерапия, 2-я (n=70) – свободная комбинация двух антигипертензивных препаратов, 3-я (n=70) – фиксированная комбинация двух антигипертензивных препаратов, 4-я (n=70) – фиксированная комбинация трех антигипертензивных средств (табл. 1). Средний балл по шкале CIRS в четырех группах составил 10,2, 9,9, 9,6 и 10,8, соответственно, что соответствовало легкой степени коморбидности. Среднее число препаратов, которые пациенты получали по поводу сопутствующих заболеваний в четырех группах, равнялось 1,7, 2,2, 2,7 и 2,4, соответственно. Десять пациентов (3,6%) не завершили наблюдение в течение года по несвязанным с АГ обстоятельствам.
| Классы препаратов | n (%) | ||
|---|---|---|---|
| Примечание: СК - свободная комбинация, ФК - фиксированная комбинация | |||
| 1-я группа (монотерапия; n=70) | |||
| Ингибитор АПФ | 27 (38,6) | ||
| БРА | 22 (31,4) | ||
| Тиазидоподобный диуретик | 8 (11,4) | ||
| Блокатор кальциевых каналов | 5 (7,1) | ||
| Бета-адреноблокатор | 4 (5,7) | ||
| Агонист имидазолиновых рецепторов | 2 (2,9) | ||
| Альфа-адреноблокатор | 2 (2,9) | ||
| 2-я группа (двухкомпонентные СК; n=70) | |||
| Ингибитор АПФ + тиазидоподобный диуретик | 13 (18,6) | ||
| БРА + тиазидоподобный диуретик | 11 (15,7) | ||
| Ингибитор АПФ + тиазидный диуретик | 10 (14,3) | ||
| Ингибитор АПФ + блокатор кальциевых каналов | 10 (14,3) | ||
| БРА + тиазидный диуретик | 9 (12,7) | ||
| БРА + блокатор кальциевых каналов | 8 (11,4) | ||
| Ингибитор АПФ + β-адреноблокатор | 5 (7,1) | ||
| БРА + β-адреноблокатор | 2 (2,9) | ||
| Агонист имидазолиновых рецепторов + тиазидоподобный диуретик | 2 (2,9) | ||
| 3-я группа (двухкомпонентные ФК; n=70) | |||
| Ингибитор АПФ + блокатор кальциевых каналов | 18 (25,7) | ||
| Ингибитор АПФ + тиазидный диуретик | 14 (20,0) | ||
| БРА + блокатор кальциевых каналов | 13 (18,6) | ||
| Ингибитор АПФ + тиазидоподобный диуретик | 11 (15,7) | ||
| БРА + тиазидный диуретик | 9 (12,9) | ||
| БРА + тиазидоподобный диуретик | 5 (7,1) | ||
| 4-я группа (трехкомпонентная ФК; n=70) | |||
| Ингибитор АПФ + тиазидоподобный диуретик + β-адреноблокатор | 70 (100,0) | ||
По данным опроса, через 1 год низкая приверженность к лечению была зафиксирована у 16 (22,5%) пациентов 1-й группы, 22 (31,0%) – 2-й группы, 18 (25,5%) – 3-й группы и 15 (21,1%) – 4-й группы.
Случаев смерти или цереброваскулярных и сердечнососудистых событий во всех группах не зарегистрировано. В течение года развитие неосложненного гипертонического криза наблюдали у 41 (15,2%) пациента, в том числе у 14 (20,9%) – в 1-й группе, у 11 (16,7%) – во 2-й, у 9 (13,0%) – в 3-й и у 7 (10,3%) – в 4-й. В трети случаев пациентам потребовалась госпитализация для коррекции АД, в том числе 5 (35,7%) из 14 в 1-й группе, 4 (36,4%) из 11 во 2-й, 3 (33,3%) из 9 в 3-й и 2 (28,6%) из 7 в 4-й. Частота неосложненного гипертонического криза и связанной с ним экстренной госпитализации достоверно не отличалась между группами. У 6 и 3 больных 2-й и 3-й групп, соответственно, во время наблюдения зафиксированы зафиксированы эпизоды артериальной гипотонии (3,2%).
Все схемы терапии обеспечивали антигипертензивный эффект. Целевые значения АД были достигнуты у 54 (80,6%) больных 1-й группы, 59 (89,4%) – 2-й группы, 64 (92,8%) – 3-й группы и 59 (86,8%) – 4-й группы. Офисное систолическое АД через 1 год в четырех группах снизилось на 9,8%, 11,4%, 10,8% и 12,1%, соответственно (p<0,05 по сравнению с исходным во всех группах), а диастолическое – на 7,2%, 10,7%, 10,7% и 11,7% (p<0,05) (табл. 2). Частота сердечных сокращений также снизилась на 4,2, 0,3%, 3,2% и 12,4%, соответственно. Наиболее выраженное снижение этого показателя в 4-й группе объяснялось тем, что одним из компонентов антигипертензивной терапии у всех больных был β-адреноблокатор.
| Показатели/группы | Исходно | 12 мес | Δ% |
|---|---|---|---|
| Примечание: изменения всех показателей были статистически значимыми (p<0,05). | |||
| САД, мм рт. ст. | |||
| 1-я группа | 153,7±3,2 | 138,6±3,2 | -9,8 |
| 2-я группа | 156,2±2,7 | 138,4±2,4 | -11,4 |
| 3-я группа | 156,3±3,4 | 139,3±3,8 | -10,8 |
| 4-я группа | 154,8±3,6 | 136,1±3,4 | -12,1 |
| ДАД, мм рт. ст. | |||
| 1-я группа | 86,8±3,5 | 80,6±3,4 | -7,2 |
| 2-я группа | 87,9±3,2 | 78,4±3,1 | -10,7 |
| 3-я группа | 88,5±2,9 | 79,0±2,4 | -10,7 |
| 4-я группа | 87,5±2,9 | 77,2±2,5 | -11,7 |
| Фракция выброса ЛЖ, % | |||
| 1-я группа | 61,9±1,1 | 63,4±1,3 | 2,4 |
| 2-я группа | 62,1±1,3 | 65,5±1,2 | 5,5 |
| 3-я группа | 61,1±0,9 | 63,2±1,0 | 3,4 |
| 4-я группа | 60,7±1,1 | 63,4±1,0 | 4,5 |
| Масса миокарда ЛЖ, г | |||
| 1-я группа | 203,9±1,4 | 201,3±1,3 | -1,3 |
| 2-я группа | 205,6±1,6 | 204,7±1,4 | -1,3 |
| 3-я группа | 206,2±1,4 | 204,8±1,5 | -0,7 |
| 4-я группа | 204,3±1,3 | 201,3±1,2 | -0,5 |
| СКФ, мл/мин/1,73 м2 | |||
| 1-я группа | 97,1±2,0 | 104,9±1,9 | 8,0 |
| 2-я группа | 97,1±1,7 | 106,6±2,1 | 9,8 |
| 3-я группа | 95,7±2,0 | 107,5±2,0 | 12,3 |
| 4-я группа | 94,5±1,8 | 104±1,9 | 10,5 |
В результате лечения ФВ ЛЖ увеличилась в среднем на 2,4-5,5% в четырех группах, а ММ ЛЖ снизилась на 0,7-1,5% (табл. 2). Кроме того, антигипертензивная терапия привела к увеличению СКФ на 8,0-12,3% (табл. 2).
Результаты лечения были также сопоставлены у пациентов с низкой приверженностью к антигипертензивной терапии (n=71) и больных, принимавших антигипертензивные препараты в соответствии с рекомендациями врача (n=199). Следует отметить, что среди больных с низкой приверженностью, получавших монотерапию или фиксированные комбинации, отказ от антигипертензивной терапии отмечался на 23,1% реже. Регулярный прием антигипертензивных средств сопровождался более значительным (p<0,05) снижением как систолического, так и диастолического офисного АД (рис. 1). Кроме того, при высокой приверженности к лечению было отмечено более значительное (p<0,05) увеличение ФВ ЛЖ (табл. 3). При невыполнении рекомендаций врача ММ ЛЖ увеличилась в среднем на 4,5%, в то время как при высокой приверженности к антигипертензивной терапии она снизилась на 2,4% (табл. 3). Расчетная СКФ при низкой и высокой приверженности к лечению увеличилась на 7,7% и 11,0%, соответственно.
| Показатели | Высокая приверженность | Низкая приверженность | ||||
|---|---|---|---|---|---|---|
| Исходно | 12 мес | Δ% | Исходно | 12 мес | Δ% | |
| Примечание: изменения всех показателей были статистически значимыми (p<0,05) | ||||||
| Эхокардиография | ||||||
| Фракция выброса ЛЖ, % | 61,3±1,5 | 63,3±1,3 | 3,2 | 61,8±1,2 | 62,1±1,4 | 0,5 |
| Масса миокарда ЛЖ, г | 206,7±1,3 | 201,3±1,5 | -2,4 | 200,1±1,6 | 209,2±1,4 | 4,5 |
| СКФ, мл/мин/1,73 м2 | 95,5±1,9 | 106,0±2,1 | 11,0 | 96,5±2,2 | 103,9±2,0 | 7,7 |
Обсуждение
Результаты исследования свидетельствуют о том, что все применяемые в амбулаторной практике схемы антигипертензивной терапии (монотерапия, двухкомпонентная и трехкомпонентная комбинации) обеспечивают контроль АД у пациентов с впервые выявленной АГ 1-2 степени и обладают органопротективными свойствами, в частности замедляют ремоделирования ЛЖ и вызывают увеличение СКФ. В 91,1% случаев пациентам назначали ингибиторы АПФ или БРА. В крупных проспективных исследованиях доказано, что блокаторы ренин-ангиотензин-альдостероновой системы вызывают снижению ММ ЛЖ, что, в свою очередь, обеспечивает снижение риска развития сердечно-сосудистых осложнений вдвое [28,29]. Кроме того, препараты этих групп оказывают нефропротективное действие [30-32]. Во всех группах через год после начала наблюдение среднее АД было ниже 140/90 мм рт. ст., что, по данным многочисленных исследований, способствует снижению риска сердечно-сосудистой заболеваемости и смертности [33,34].
Несмотря на применение в амбулаторной практике современных схем антигипертензивной терапии, которые не только оказывают гипотензивное действие, но и обладают органопротективными свойствами [36], на практике пациенты достигают целевых показателей АД менее чем в 50% случаев [25,37,38], в первую очередь, вследствие низкой приверженности к лечению. В течение первых 6 мес от медикаментозного лечения АГ отказываются до трети пациентов, а в течение года – до половины [39]. По данным нашего исследования, в течение года от антигипертензивной терапии частично или полностью отказались 26,3% пациентов.
Один из подходов к повышению приверженности к лечению – стратегия "одной таблетки". В рамках настоящего исследования, пациенты, получавшие монотерапию или фиксированные комбинации антигипертензивных средств в виде одной таблетки, на 23,1% реже частично или полностью отказывались от терапии, что согласуется с опубликованными ранее данными [18,19]. Высокая приверженность к антигипертензивной терапии у пациентов с впервые выявленной АГ сопровождалась более выраженным снижением офисного АД, а отсутствие приверженности к лечению нивелировало его кардиопротективный эффект. Так, у пациентов, регулярного принимавших антигипертензивные препараты, ММ ЛЖ снизилась в среднем на 5,4 г, в то время как при низкой приверженности к терапии она увеличилась на 9,1 г. Кроме того, в первой группе отмечено более значительное увеличение ФВ ЛЖ и СКФ.
Заключение
Амбулаторным пациентам с впервые установленной АГ 1-2 степени и без сердечно-сосудистых осложнений в анамнезе лечащие врачи первичного звена рекомендовали различные схемы антигипертензивной терапии (монотерапия, двух- и трехкомпонентные комбинации), которые в течение одного года способствовали стабилизации АД, нормализации его вариабельности и оказывали благоприятное влияние на систолическую функцию и ММ ЛЖ и СКФ. Эффективность антигипертензивной терапии и ее кардио- и нефропротективное действие значительно снижались в случае частичного или полного отказа пациента от приема антигипертензивных препаратов. Результаты исследования свидетельствуют о том, что в реальной амбулаторной практике по-прежнему остается актуальным вопрос повышения приверженности пациентов с АГ к лечению с целью адекватной профилактики сердечно-сосудистых осложнений, в первую очередь, хронической сердечной недостаточности.
Используемые источники
- World Health Organization. (WHO). Available from: https://www.who.int/newsroom/fact-sheets/detail/cardiovascular-diseases-(cvds).
- O'Gallagher K, Shek A, Bean DM, et al. Pre-existing cardiovascular disease rather than cardiovascular risk factors drives mortality in COVID-19. BMC Cardiovasc Disord 2021;21(1):327.
- Bae S, Kim SR, Kim MN, et al. Impact of cardiovascular disease and risk factors on fatal outcomes in patients with COVID-19 according to age: a systematic review and meta-analysis. Heart 202;107(5):373-80.
- Iqbal AM, Jamal SF. Essential hypertension. Updated 2021 Jul 26. StatPearls [Internet]. Treasure Island (FL): StatPearls 2022 Jan. https://www.ncbi.nlm.nih.gov/books/NBK539859/
- Lewington S, Clarke R, Qizilbash N, et al. Prospective Studies Collaboration. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360(9349):1903-13.
- Rapsomaniki E, Timmis A, George J, et al. Blood pressure and incidence of twelve cardiovascular diseases: lifetime risks, healthy life-years lost, and age-specific associations in 1·25 million people. Lancet 2014;383:1899-911.
- He J, Whelton PK. Elevated systolic blood pressure and risk of cardiovascular and renal disease: overview of evidence from observational epidemiologic studies and randomized controlled trials. Am Heart J 1999;138(3):211–9.
- Zhou B, Carrillo-Larco MR, Danaei G, et al. Worldwide trends in hypertension prevalence and progress in treatment and control from 1990 to 2019: a pooled analysis of 1201 population-representative studies with 104 million participants. Lancet 2021;398:957–80.
- Virani SS, Alonso A, Aparicio HJ, et al. Heart Disease and Stroke Statistics—2021 Update. Circulation 2021;143:e254–743.
- Lim SS, Vos T, Flaxman AD, Danaei G, et al. A comparative risk assessment of burden of disease and injury attributable to 67 risk factors and risk factor clusters in 21 regions, 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;380:2224–60.
- Piera-Jimenez J, Winters M, Broers E, et al. Changing the health behavior of patients with cardiovascular disease through an electronic health intervention in three different countries: cost-effectiveness study in the Do Cardiac Health: Advanced New Generation Ecosystem (Do CHANGE) 2 Randomized Controlled Trial. J Med Internet Res 2020;22(7):e17351.
- Herrett E, Gadd S, Jackson R, et a. Eligibility and subsequent burden of cardiovascular disease of four strategies for blood pressure-lowering treatment: a retrospective cohort study. Lancet 2019;10199:663-71.
- Ерина А.М., Ротарь О.П., Солнцев В.Н. и др. Эпидемиология артериальной гипертензии в Российской Федерации – важность выбора критериев диагностики. Кардиология 2019;59(6):5-11 [Erina AM, Rotar OP, Solntsev VN, et al. Epidemiology of arterial hypertension in Russian Federation – importance of choice of criteria of diagnosis. Kardiologiia 2019;59(6):5-11 (In Russ.)].
- Beaney T, Schutte AE, Tomaszewski M, et al; MMM Investigators. May Measurement Month 2017: an analysis of blood pressure screening results worldwide. Lancet Glob Health 2018;6(7):e736-43.
- Prakash D. Target organ damage in newly detected hypertensive patients. J Family Med Prim Care 2019;8(6):2042-6.
- Williamsom JD, Supiano MA, Applegate WB, et al. Intensive vs standard blood pressure control and cardiovascular disease outcomes in adults aged ≥75 years: a randomized clinical trial. JAMA 2016;315(24):2673–82.
- Parati G, Lombardi C, Pengo M, et a. Current challenges for hypertension management: From better hypertension diagnosis to improved patients' adherence and blood pressure control, Intern J Cardiol 2021;0167-5273:262-9.
- Dezii CM. A retrospective study of persistence with single-pill combination therapy vs. concurrent two-pill therapy in patients with hypertension. Manag Care 2000;9:2–6.
- Gupta AK, Arshad S, Poulter NR. Compliance, safety, and effectiveness of fixeddose combinations of antihypertensive agents: a meta-analysis. Hypertension 2010;55:399–407.
- Gupta P, Patel P, Strauch B, et al. Biochemical screening for nonadherence is associated with blood pressure reduction and improvement in adherence. Hypertension 2017,70(5):1042-8.
- Ashoorkhani M, Majdzadeh R, Gholami J, et al. Understanding non-adherence to treatment in hypertension: A qualitative study. Int J Community Based Nurs Midwifery 2018;6(4):314–23.
- Naderi SH, Bestwick JP, Wald DS. Adherence to drugs that prevent cardiovascular disease: meta-analysis on 376,162 patients. Amer J Med 2012;9:882-7.
- Alhaddad IA, Hamoui O, Hammoudeh A, Mallat S. Treatment adherence and quality of life in patients on antihypertensive medications in a Middle Eastern population: adherence. Vasc Health Risk Manag 2016;12:407–13.
- Abegaz TM, Shehab A, Gebreyohannes EA, et al. Nonadherence to antihypertensive drugs: A systematic review and meta-analysis. Medicine (Baltimore) 2017;96(4):e5641.
- Cameron AC, Lang NN, Touyz RM. Drug treatment of hypertension: focus on vascular health. Drugs 2016;76(16):1529–50.
- Xie X, Atkins E, Lv J, et al. Effects of intensive blood pressure lowering on cardiovascular and renal outcomes: updated systematic review and meta-analysis. Lancet 2016;387(10017):435–43.
- Fan Z, Wu G, Yue M, et al. Hypertension and hypertensive left ventricular hypertrophy are associated with ACE2 genetic polymorphism. Life Sciences 2019; 225:39-45.
- Klingbeil AU, Schneider M, Martus P, et al. A meta-analysis of the effects of treatment on left ventricular mass in essential hypertension. Amer J Med 2003;115:41–46.
- Verdecchia P, Angeli F, Borgioni C, et al. Changes in cardiovascular risk by reduction of left ventricular mass in hypertension: a meta-analysis. Am J Hypertens 2003;16:895–9.
- Mancia G, Laurent S, Agabiti-Rosei E, et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document. Hypertens 2009;27:2121–58.
- Deutsche Hochdruckliga. Leitlinien zur Behandlung der arteriellen Hypertonie. Nieren- und Hochdruckkrankheiten 2009;38:137–88.
- Parving HH, Persson F, Lewis JB, et al. Aliskiren combined with losartan in type 2 diabetes and nephropathy. N Engl J Med. 2008;358:2433–46.
- Kjeldsen SE. Hypertension and cardiovascular risk: General aspects. Pharmacol Res 2018;1043-6618:95-99.
- Mancia G, Fagard R, Narkiewicz K, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens 2013;31(7):1281-357.
- Dorobanţu M, Darabont R, Ghiorghe S, et al. Hypertension prevalence and control in Romania at a seven-year interval. Comparison of SEPHAR I and II surveys. J Hypertens 2014;32:39–47.
- Williams B, Mancia G, Spiering W, et al. ESC Scientific Document Group, 2018 ESC/ESH Guidelines for the management of arterial hypertension: The Task Force for the management of arterial hypertension of the European Society of Cardiology (ESC) and the European Society of Hypertension (ESH). Europ Heart J 2018;33(01):3021-104.
- Ротарь О.П., Толкунова К.М., Мевша О.В. и др. Скрининговое измерение артериального давления в российской популяции (результаты акции МММ17). Артериальная гипертензия 2018;24(4):448-58. [Rotar OP, Tolkunova KM, Mevsha OV, et al. Screening blood pressure measurement in the Russian population (the results of the МММ17 activity). Arterial’naya Gipertenziya = Arterial Hypertension 2018;24(4):448-58 (In Russ.)].
- Kearney PM, Whelton M, Reynolds K, et al. Worldwide prevalence of hypertension: a systematic review. J Hypertens 2004;22(1):11–9.
- Naderi SH, Bestwick JP, Wald DS. Adherence to drugs that prevent cardiovascular disease: meta-analysis on 376,162 patients. Amer J Med 125(9):882–887.
