Комплексная оценка статуса гидратации у пациентов с острой декомпенсацией хронической сердечной недостаточности: клинические ассоциации и прогностическое значение
Изучить клиническое и прогностическое значение комплексной оценки статуса гидратации у пациентов с острой декомпенсацией хронической сердечной недостаточности (ОДХСН).
В одноцентровое проспективное исследование были включены 171 пациент, госпитализированный с ОДХСН. Всем пациентам проводили стандартное физическое обследование, определение NT-proBNP, ультразвуковое исследование (УЗИ) легких, непрямую фиброэластометрию печени и биоимпедансный векторный анализ при поступлении и при выписке. Для оценки клинического застоя использовали шкалу документа HFA. Оценка долгосрочных клинических исходов проведена методом структурированного телефонного опроса через 1, 3, 6, 12 мес после выписки. Оценивали суммарную частоту смерти от всех причин и повторных госпитализаций.
По данным комплексной оценки состояния гидратации с помощью четырех методов, состояние компенсации при выписке было достигнуто у 12% пациентов с ОДХСН, в то время как субклинический и остаточный застой сохранялись у 31% и 57% пациентов соответственно. Пороговое значение количества В линий, позволявшее прогнозировать неблагоприятный исход в течение года после выписки, составило >5, содержания NT-proBNP – >2336 пг/мл, плотности печени – >9,7 кПа и импеданса Z – ≤479 Ом/м. Результаты лабораторно-инструментальных методов ухудшались, а риск неблагоприятных исходов возрастал при увеличении количества методов, подтверждавших наличие застоя, с 1 до 4. Комбинации УЗИ легких + непрямой эластометрии (два метода), УЗИ легких + непрямой эластометрии + NT-proBNP (три метода) и особенно всех четырех методов имели наилучшую прогностическую ценность в отношении риска неблагоприятных исходов.
Пациентам, госпитализированным с ОДХСН, для оценки остаточного и субклинического застоя при выписке целесообразно использовать различные методы. Внедрение интегральной оценки застоя в рутинную практику позволит выявить группу пациентов с повышенным риском смерти и повторных госпитализаций и интенсифицировать медикаментозную терапию и наблюдение пациентов на амбулаторном этапе.
Ведущим патофизиологическим механизмом декомпенсации сердечной недостаточности и причиной госпитализации является системный застой [1], наличие которого ассоциировано с неблагоприятным прогнозом [2]. По данным ряда исследований, в том числе DOSE-AHF и CARESS-HF, признаки периферического застоя крови при выписке наблюдаются примерно у половины пациентов [3-5]. Остаточный застой – одна из причин повторных госпитализаций пациентов с острой декомпенсацией хронической сердечной недостаточности (ОДХСН), частота которых достигает 18% в первые 30 дней после выписки. Наличие остаточного застоя крови ассоциировалось с повышением смертности и частоты повторных госпитализаций в течение 60 дней [3], а застоя на 7-й день госпитализации – с повышением риска повторных госпитализаций по поводу сердечной недостаточности в течение 180 дней после выписки [6].
Достаточно часто застойные явления остаются незамеченными, так как в ряде случаев не проявляются клинически, а могут быть выявлены только лабораторными и/или инструментальными методами. Данные наблюдательных исследований свидетельствуют о том, что у существенной части пациентов перед выпиской из стационара сохраняются клинические или инструментальные признаки застоя, которые приводят к увеличению риска повторной госпитализации по поводу сердечной недостаточности и смерти от всех причин [6-8]. В связи с этим в современных рекомендациях указывается на необходимость тщательного обследования пациентов с ОДХСН перед выпиской из стационара для выявления клинических и параклинических признаков застоя с целью оптимизации терапии [9].
Методы оценки застоя, которые по данным литературы имеют прогностическую ценность, включают измерение концентрации мозгового натрийуретического пептида (NT-proBNP), определение количества В-линий при УЗИ легких и плотности печени методом непрямой эластометрии, а также оценку гидратации методом биоимпедансного векторного анализа (БИВА). В ряде исследований показана высокая частота остаточного застоя при использовании отдельных инструментальных методов [8,10,11]. Однако изучению комплексной оценки остаточного и субклинического застоя лабораторно-инструментальными методами и ее влияния на прогноз посвящены единичные работы [2, 12].
Целью исследования было изучить клиническое и прогностическое значение комплексной оценки статуса гидратации у пациентов с ОДХСН.
Материал и методы
В исследование включали пациентов, госпитализированных с ОДХСН в Центр сердечной недостаточности на базе ГКБ им. В.В. Виноградова (Москва). ОДХСН диагностировали на основании общепринятых критериев [13]. В исследование не включали больных с острым коронарным синдромом, тяжелыми соматическими и злокачественными заболеваниями, отечным синдромом иной этиологии, острым гепатитом c повышением активности аминотрансфераз более чем в 5 раз по сравнению с верхней границей нормы, иммобилизацией, а также пациентов, которым нельзя было выполнить БИВА. Все пациенты перед проведением процедур исследования подписали информированное согласие. Исследование было выполнено в соответствии со стандартами надлежащей клинической практики (Good Clinical Practice) и принципами Хельсинской декларации. Протокол исследования был одобрен локальным этическим комитетом.
Всем пациентам, включенным в исследование, в первые 24 часа от момента госпитализации и при выписке, проводили стандартное физическое, лабораторное и инструментальное обследование, включая УЗИ легких, NT-proBNP, фиброэластометрию печени и БИВА.
В отдаленном периоде клинические события оценивали методом структурированного телефонного опроса через 1, 3, 6 и 12 мес после выписки. В качестве конечной точки определяли суммарную частоту смерти от всех причин и повторных госпитализаций.
Застой крови оценивали с помощью клинической шкалы Heart Failure Association (HFA) [14]. Каждый клинический симптом и признак оценивали в день поступления и выписки. Критерием наличия клинического застоя при поступлении и остаточного застоя с клиническими проявлениями при выписке служило значение суммарного балла ≥1.
NT-proBNP в сыворотке крови определяли методом иммуноферментного анализа ELISA с использованием тест систем NT-proBNP-ИФА-БЕСТ (Россия, ЗАО "ВекторБест").
УЗИ легких (VIVID iq, GE) с подсчетом суммы В-линийвыполняли в 8 областях (II и IV межреберья между парастернальной и среднеключичной линиями и между передней и средней подмышечными линиями с обеих сторон).
Непрямую эластометрию печени проводили с помощью аппарата FibroScan 502 touch (Echosens, Франция) в проекции правой доли печени на уровне VIII или IX межреберьев по передней или средней подмышечной линии. Определяли показатель плотности (эластичности) печени в килопаскалях (кПа) и интерквартильный размах в процентах (%).
Для оценки статуса гидратации выполняли БИВА (АВС01 "Медасс"). Электрический импеданс биологических тканей имеет два компонента – активное (R) и реактивное (Xc) сопротивление. Более низкие значения активного и реактивного сопротивления соответствовали большей степени гидратации. Импеданс рассчитывается по формуле Z = √(R2 + Xc2).
УЗИ легких расценивали как метод оценки застоя по малому кругу кровообращения, непрямую эластометрию печени – по большому кругу кровообращения, БИВА и NT-proBNP – как методы оценки системного застоя. При наличии клинических и отсутствии инструментальных данных фиксировали остаточный застой с клиническими проявлениями, обусловленный застоем по-другому кругу кровообращения. О субклиническом застое свидетельствовали отсутствие клинических и наличие инструментальных его признаков, об эуволемии – отсутствие признаков застоя как при клиническом, так и дополнительном исследовании.
Для статистической обработки данных использовали программное обеспечение MedCalc Software’s VAT Version 19.0 и SPSS (версия 22.0). Количественные переменные описывали как среднее арифметическое значение (М) и стандартное отклонение среднего значения (SD) (при нормальном распределении) или как медиану (Me) и интерквартильный размах (IQR) (при асимметричном распределении). Определение пороговых значений выживаемости для каждого из методов производили с помощью построения ROC кривых. Значимым считали р<0,05. Для оценки влияния результатов разных методов на риск наступления переменных интереса использовали одно- и многофакторные модели регрессионного анализа Кокса. Переменные, включенные в модуль, выбирали с учетом их значимости. Вероятность выживания оценивали методом построения кривых выживаемости Каплана-Мейера, сравнение производили с помощью лог-рангового критерия.
Результаты
В исследование были включены 171 пациент с ОДХСН, в том числе 105 мужчин (табл. 1). На амбулаторном этапе пациенты получали петлевые диуретики (72,5%), антагонисты минералокортикоидных рецепторов (53,2%), ингибиторы АПФ/блокаторы ангиотензиновых рецепторов (БРА)/ингибитор ангиотензиновых рецепторов и неприлизина (АРНИ) (77,2%), β-адреноблокаторы (70,1%), сердечные гликозиды (17,0%) и оральные антикоагулянты (55,0%), а в стационаре – петлевые диуретики (100%), антагонисты минералокортикоидных рецепторов (72,5%), ингибиторы АПФ/БРА/АРНИ (92,3%), β-адреноблокаторы (96,4%), сердечные гликозиды (17,0%) и оральные антикоагулянты (62,0%). Динамика застоя, который оценивали клинически и с помощью лабораторных и инструментальных параметров, приведена в табл. 2.
| Показатель | Значение |
|---|---|
| Примечание: ЧКВ - чрескожное вмешательство на коронарных артериях. Приведены М±SD, если не указано иное | |
| Мужчины, n (%) | 105 (61) |
| Возраст, годы | 69,4±12,3 |
| Индекс массы тела, кг/м2 | 32,2±7,0 |
| Ожирение, n (%) | 77 (58) |
| Курение, n (%) | 58 (34) |
| Фракция выброса левого желудочка, % | 41,6±13,3 |
| Артериальная гипертония, n (%) | 158 (92) |
| Инсульт в анамнезе, n (%) | 21 (12) |
| Ишемическая болезнь сердца, n (%) | 92 (54) |
| Инфаркт миокарда в анамнезе, n (%) | 66 (39) |
| Аортокоронарное шунтирование, n (%) | 8 (5) |
| ЧКВ, n (%) | 19 (11) |
| Фибрилляция/трепетание предсердий, n (%) | 107 (62) |
| Сахарный диабет 2 типа, n (%) | 40 (23) |
| Хроническая болезнь почек, n (%) | 25 (15) |
| Анемия, n (%) | 39 (23) |
| ХОБЛ/бронхиальная астма, n (%) | 31 (18) |
Плотность печени при поступлении и при выписке коррелировала с суммой В-линий (r=0,16; p=0,034 и r=0,24; p=0,002, соответственно) и показателем импеданса Z (r=-0,46; p<0,001 и r=-0,28; p<0,001), сумма Влиний – с показателем импеданса Z (r=-0,34; p=0,001 и r=-0,16; р=0,038), шкала клинической оценки – с плотностью печени (r=0,35; p<0,001 и r=0,46; p<0,001) и показателем импеданса Z (r=-0,46; p<0,001 и r=-0,50; p<0,001). Концентрация NT-proBNP при поступлении коррелировала с плотностью печени (r=0,30; p<0,001), количеством В-линий (r=0,27; p<0,001) и показателем импеданса Z (r=-0,18; р=0,016), а при выписке – только с плотностью печени (r=0,30; p<0,001).
| Показатели | Поступление | Выписка | р |
|---|---|---|---|
| Примечание: Данные представлены как Me (IQR) | |||
| Клинические, n (%) | |||
| Ортопное | 131,0 (77,0) | 44 (25,7) | <0,001 |
| Гепатомегалия | 86 (50,3) | 46 (27,0) | <0,001 |
| Набухание шейных вен | 68,0 (39,7) | 27,0 (15,7) | <0,001 |
| Отеки | 155 (90,6) | 53 (31,0) | <0,001 |
| Дополнительные методы | |||
| Плотность печени, кПа | 12,3 (7,0; 23,6) | 7,4 (5,0; 14,0) | <0,001 |
| Сумма В-линий | 35 (23; 51) | 9 (3; 24) | <0,001 |
| Импеданс Z, Ом/м | 416 (351; 481) | 484 (418; 536) | <0,001 |
| NT-proBNP, пг/мл | 2332 (1130; 4528) | 1901 (765; 3437) | <0,001 |
Частота остаточного застоя, выявленного с помощью различных методов (фиброэластометрии печени, УЗИ легких, БИВА и NT-proBNP), составляла от 33 до 39%, субклинического – от 12 до 24%, а доля пациентов, достигших эуволемии, – от 19 до 32% (рис. 1).
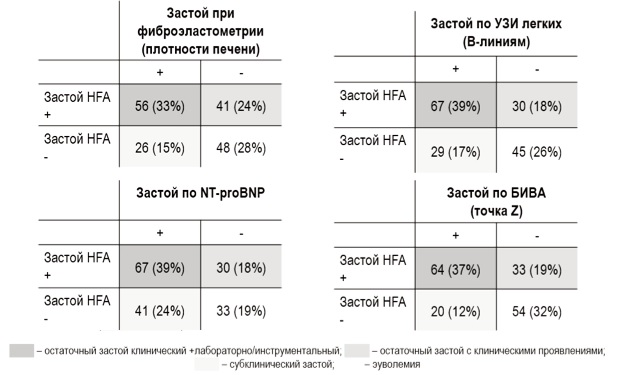
У пациентов с остаточным застоем с клиническими проявлениями, у которых признаки его не были выявлены при фиброэластометрии печени, отсутствовала гепатомегалия и определялись признаки застоя по малому кругу кровообращения, в то время как у пациентов с клиническими проявлениями остаточного застоя, у которых не было увеличено число В-линий, отсутствовало ортопное, но имелись признаки застоя по большому кругу кровообращения (гепатомегалия, набухание шейных вен, отеки) (табл. 3).
| Показатели | Без застоя при УЗИ легких (n=30) | Без застоя при фиброэластометрии печени (n=41) | p |
|---|---|---|---|
| Примечание: Данные представлены как Me (IQR) | |||
| Клинические, n (%) | |||
| Ортопное | 0 (0) | 24 (59) | <0,001 |
| Гепатомегалия | 13 (43) | 0 (0) | <0,001 |
| Набухание шейных вен | 11 (37) | 7 (17) | 0,03 |
| Отеки | 18 (60) | 23 (56) | нд |
| Дополнительные методы | |||
| Плотность печени, кПа | 8,0 (6,0; 14,0) | 5,5 (4,6; 6,9) | <0,001 |
| Сумма В-линий | 3 (2; 5) | 16 (3; 33) | <0,001 |
| Импеданс Z, Ом/м | 443 (408; 498) | 473 (419; 502) | 0,06 |
| NT-proBNP, пг/мл | 1888 (562; 2834) | 1363 (539; 2518) | 0,03 |
У пациентов без клинических проявлений застоя при выписке были нормальными плотность печени и количество В-линий и определялись максимальные значения импеданса Z (медиана 521 Ом/м) и более низкие уровни NT-proBNP (медиана 1634 пг/мл). У пациентов с клиническими проявлениями застоя по малому кругу кровообращения медиана количества В-линий составила 25,5, в то время как остальные лабораторно-инструментальные показатели были сопоставимы с таковыми в группе пациентов без застоя. Пациенты с клиническим застоем по большому кругу кровообращения характеризовались отсутствием ортопноэ и нормальным количеством В-линий (<5), более высокими показателями плотности печени (медиана 11,1 кПа) и NT-proBNP (2154 пг/мл) и более низкими значениями импеданса Z (медиана 439 Ом/м). У пациентов с клиническим застоем по обоим кругам кровообращения наблюдались высокая плотность печени (медиана 13,2 кПа), максимальные количество В-линий (медиана 26) и NT-proBNP (медиана 2398 пг/мл) и минимальное значение импеданса Z (медиана 395 Ом/м).
При использовании комплексной оценки статуса гидратации с помощью дополнительных методов частота остаточного застоя, определявшегося и клинически, составила 57%, субклинического – 31%, компенсации – 12%. Таким образом, комплексная оценка застоя обладает преимуществом перед отдельными методами и позволяет выявить большее количество пациентов с остаточным и субклиническим застоем.
У пациентов с остаточным застоем по данным комплексной оценки имелись более выраженные изменения изученных показателей по сравнению с таковыми у пациентов с субклиническим застоем и компенсацией, в том числе более высокие значения медианы плотности печени (10,0, 7,3 и 5,1 кПа, соответственно), количества В-линий (20, 6 и 3) и NT-pro-BNP (2348, 2143 и 450 пг/мл) и более низкие значения медианы показателя Z (447, 511 и 531 Ом/м).
| Показатели | Все пациенты (n=171) | Нет событий (n=112) | Событие (n=59) | p |
|---|---|---|---|---|
| Примечание: данные представлены как Me (IQR) | ||||
| Плотность | 7,4 | 6,3 | 11,4 | <0,001 |
| печени, кПа | (5,0; 14,0) | (4,7; 10,0) | (6,7; 19,1) | |
| Сумма В-линий | 9 (3; 24) | 5 (3; 22) | 16 (5; 25) | 0,045 |
| Импеданс Z, | 484 | 492 | 456 | 0,025 |
| Ом/м | (418; 536) | (430; 544) | (375; 522) | |
| NT-proBNP, | 1901 | 1445 | 2876 | <0,001 |
| пг/мл | (765; 3437) | (536; 2514) | (1519; 5120) | |
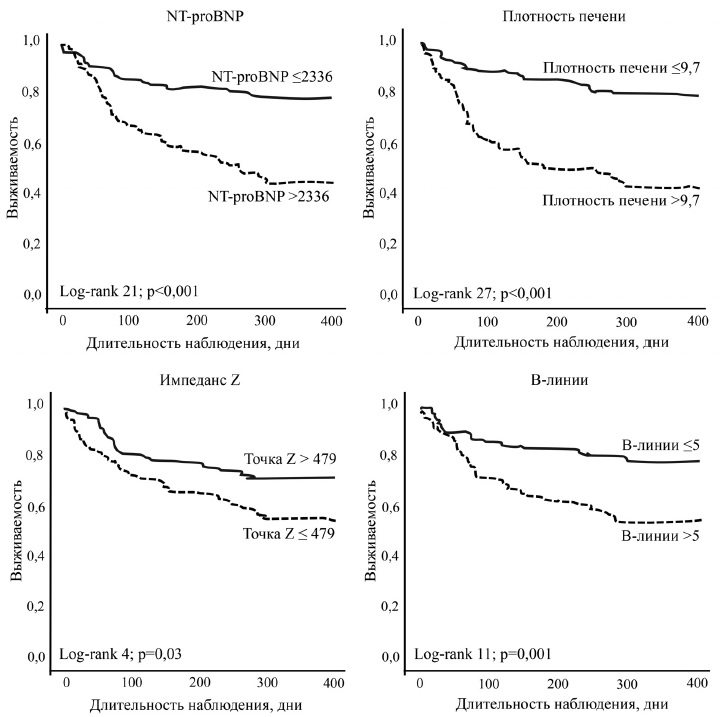
В течение года после выписки у 171 пациентов зарегистрировали 59 событий, в том числе 10 случаев смерти и 49 повторных госпитализаций. Неблагоприятные исходы отсутствовали у пациентов, которые достигли компенсации при выписке, и наблюдались у 42 (43,3%) из 97 пациентов с остаточным застоем и 17 (32,1%) из 53 пациентов с субклиническим застоем. У пациентов с неблагоприятными событиями значения комплексной оценки застоя при выписке были хуже, чем у выживших пациентов, которым не потребовалась повторная госпитализация (табл. 4). По данным ROC-анализа, пороговые значения показателей, позволявшие прогнозировать неблагоприятный исход, были следующими: количество В линий >5, NT-proBNP>2336 пг/мл, плотность печени >9,7 кПа и импеданс Z ≤479 Ом/м (табл. 5, рис. 2).
| Показатели | Значения | Чувств. | Спец. | AUC | p |
|---|---|---|---|---|---|
| Плотность печени, кПа | >9,7 | 64,4 | 75,0 | 0,716 | <0,001 |
| Сумма В-линий | >5 | 74,5 | 53,5 | 0,611 | 0,013 |
| Импеданс Z, Ом/м | ≤479 | 57,6 | 62,5 | 0,616 | 0,013 |
| NT-proBNP, пг/мл | >2336 | 64,4 | 72,3 | 0,716 | <0,001 |
Пациенты, у которых был выявлен застой с помощью всех четырех методов (фиброэластометрия, УЗИ легких, БИВА и NT-proBNP), лабораторно-инструментальные показатели были хуже, чем у пациентов, у которых застой определялся с помощью 1-3 методов (табл. 6). При наличии застоя, выявленного двумя, тремя или четырьмя методами при выписке, наблюдается достоверное повышение риска неблагоприятных исходов у пациентов с ОДХСН. Комбинации УЗИ легких + непрямой эластометрии (два метода), УЗИ легких + непрямой эластометрии + NT-proBNP (три метода) и особенно всех четырех методов имеют наилучшую прогностическую ценность в отношении риска неблагоприятных исходов (табл. 7).
| Показатели | Нет застоя (n=21) | 1 метод (n=29) | 2 метода (n=49) | 3 метода (n=45) | 4 метода (n=27) | p |
|---|---|---|---|---|---|---|
| Плотность печени, кПа | 5,1 (3,7; 6,0) | 5,4 (4,5; 6,4) | 7,0 (4,4; 10,5) | 11,0 (8,0; 16,2) | 17,0 (13,0; 22,0) | <0,001 |
| Сумма В-линий | 3 (2; 3) | 4 (3; 5) | 16 (3; 31) | 16 (6; 24) | 21 (17; 28) | <0,001 |
| Импеданс Z, Ом/м | 531 (500; 578) | 521 (457; 543) | 490 (443; 520) | 479 (396; 545) | 383 (349; 432) | <0,001 |
| NT-proBNP, пг/мл | 450 (127; 949) | 1054 (367; 2496) | 1649 (868; 2766) | 2685 (1621; 5291) | 2795 (2121; 5191) | <0,001 |
Обсуждение
Системный застой при сердечной недостаточности характеризуется более сложной патофизиологией, чем просто накопление избыточной воды в организме [15]. Отсутствие универсальных критериев его оценки и методов, подтверждающих достижение так называемой "эуволемии" [16], подчеркивают актуальность исследований по сопоставлению клинической и прогностической ценности различных методов диагностики и лабораторных показателей застоя.
| Количество методов | ОР (95% ДИ) | р |
|---|---|---|
| Два метода | ||
| УЗИ легких + эластометрия | 21,0 (2,2-205,0) | 0,008 |
| УЗИ легких + БИВА | 2,6 (0,4-14,6) | 0,880 |
| УЗИ легких + NT-proBNP | 15,7 (1,7-140,0) | 0,014 |
| Три метода | ||
| УЗИ легких +эластометрия+NT-proBNP | 28,2 (3,6-219,0) | 0,001 |
| УЗИ легких + эластометрия + БИВА | 23,3 (2,7-200,0) | 0,004 |
| УЗИ легких + БИВА + NT-proBNP | 12,2 (1,3-110,0) | 0,025 |
| Четыре метода | 33,1 (4,2-255,0) | 0,001 |
В данном исследовании продемонстрировано прогностическое значение лабораторных и инструментальных методов, отражающих разные компоненты застойных явлений при ОДХСН, в отношении суммарного риска смерти и повторных госпитализаций. Оценка "гемодинамического" застоя проводилась на основании содержания NT-proBNP, "легочного" – методом УЗИ легких, "печеночного" – путем оценки плотности печени с помощью непрямой фиброэластометрии, периферической гидратация – методом БИВА. Несомненно, на практике главным инструментом оценки застоя остается физический осмотр. Однако точность традиционных клинических симптомов и признаков застоя, отражающих увеличение внутрисердечного давления наполнения и/или, как следствие, избыточное накопление внесосудистой жидкости, относительно невелика по сравнению с внутрисердечной оценкой гемодинамики [16].
У всех обследованных нами пациентов с ОДХСН при поступлении в стационар были выявлены как лабораторно-инструментальные, так и клинические признаки застоя. Определялась достоверная корреляция содержания NT-proBNP с результатами всех инструментальных методов оценки застоя, таких как непрямая фиброэластометрия, УЗИ легких и БИВА. При выписке уровень NT-proBNP прямо коррелировал только с плотностью печени, достоверных взаимосвязей с количеством В-линий и значениями импеданса Z по БИВА выявлено не было.
В результате лечения было отмечено достоверное уменьшение как клинических, так и лабораторноинструментальных признаков застоя. Однако частота остаточного застоя, который определялся клинически и с помощью дополнительных методов, составляла от 33 до 39%, а субклинического застоя – от 12 до 24%. Соответственно, доля пациентов, достигших компенсации, варьировалась от 19 до 32%. Частота выявления остаточного застоя при использовании УЗИ легких составила 39%, определения содержания NT-proBNP – 39%, БИВА – 37%, непрямой фиброэластометрии – 33%, субклинического застоя – 17%, 24%, 15% и 12%, соответственно. При комплексной оценке результатов различных методов частота выявления остаточного и субклинического застоя была выше – 57% и 31%, соответственно. Таким образом, комплексный подход к оценке застоя обладает преимуществом перед отдельными методами и позволяет выявить большее количество пациентов с остаточным и субклиническим застоем в результате анализа различных его компонентов (гемодинамического, сосудистого и т.д.), а также застоя по малому и большому кругам кровообращения. Так, застой по малому кругу кровообращения отражают результаты УЗИ легких и положение ортопное, по большому кругу – данные непрямой фиброэластометрии и БИВА, отеки, гепатомегалия и набухание шейных вен, в то время как содержание NT-proBNP представляет собой "системный" маркер застоя, уровень которого не зависит от вовлеченности того или иного кругов кровообращения. У пациентов, у которых застой определялся с помощью всех четырех методов (фиброэластометрия, УЗИ легких, БИВА, NT-proBNP), лабораторно-инструментальные показатели были хуже, чем у пациентов, у которых он был выявлен с помощью 1-3 методов.
Наличие застоя при выписке у пациентов с ОДХСН сопровождалось увеличением риска неблагоприятных событий в течение года наблюдения. Так, у пациентов с эуволемией случаи смерти или повторной госпитализации зарегистрированы не были, в то время как у пациентов с субклиническим и остаточным застоем их частота составила 32,1% и 43,3%, соответственно. При этом содержание NT-proBNP, количество В-линий, плотность печени и импеданс Z при выписке из стационара имели независимую ценность в оценке риска неблагоприятных исходов в отдаленном периоде. Учитывая необходимость исследования обоих кругов кровообращения, любая комбинация УЗИ легких с методом оценки застоя по большому кругу кровообращения будет максимально эффективной. Более высоким прогностическим значением характеризовались комбинации УЗИ легких с непрямой эластометрией (ОР 21,0, 95% ДИ 2,2– 205,0; р=0,008) и УЗИ легких с непрямой эластометрией и содержанием NT-proBNP (ОР 28,2, 95% ДИ 3,6–219,0; p=0,001), а максимальной ценностью обладала комбинация всех четырех методов (ОР 33,1, 95% ДИ 4,2–255,0; р=0,001). Опубликованы единичные исследования, в которых оценивалось прогностическое значение различных методов выявления застоя у пациентов с сердечной недостаточностью. Так, F. Massari и соавт. показали, что совместное определение уровня мозгового натрийуретического пептида (BNP), расчетного объема плазмы, показателя импеданса и отношения азота мочевины крови к креатинину при поступлении имеют независимое и взаимодополняющее прогностическое значение [12]. В другом исследовании при многофакторном регрессионном анализе установлено, что содержание BNP и индекс гидратации при поступлении были значимыми предикторами продолжительности пребывания пациентов в больнице (р<0,0001) [17].
застоя и концентрация NT-proBNP при выписке пациентов с ОДХСН могут быть недостаточно информативными. Комбинация объективных методов диагностики застоя в дополнение к клинической оценке помогает оценить его наличие и выбрать рациональную тактику дальнейшего наблюдения и лечения. При этом УЗИ легких, оценка плотности печени и БИВА обладают доказанной прогностической ценностью. Результаты нашего исследования открывают новые перспективы не только оценки застоя у пациентов с сердечной недостаточностью, но и разработки стратегии "управления" путем интенсификации медикаментозной терапии и наблюдения на амбулаторном этапе, что может привести к снижению частоты повторных госпитализаций и смерти. Однако необходимо дальнейшее изучение диагностической и прогностической ценности комплексной оценки застоя на большей группе пациентов с сердечной недостаточностью.
Используемые источники
- Dupont M, Mullens W, Tang WH. Impact of systemic venous congestion in heart failure. Curr Heart Fail Rep 2011;8(4):233-41.
- Girerd N, Seronde MF, Coiro S, et al. Integrative assessment of congestion in heart failure throughout the patient journey. JACC Heart Fail 2018;6(4):273-85.
- Lala A, McNulty S, Mentz R, et al. Relief and recurrence of congestion during and after hospitalization for acute heart failure: insights from Diuretic Optimization Strategy Evaluation in Acute Decompensated Heart Failure (DOSE-AHF) and Cardiorenal Rescue Study in Acute Decompensated Heart Failure (CARESS-HF). Circulation Heart Failure 2015;8(4):741-8.
- Fonarow G, ADHERE Scientific Advisory Committee. The Acute Decom pensated Heart Failure National Registry (ADHERE): opportunities to improve care of patients hospitalized with acute decompensated heart failure. Rev Cardiovasc Med 2003;4 Suppl 7:S21-30.
- Kirkwood F, Gregg F, Emerman C, et al. Characteristics and outcomes of patients hospitalized for heart failure in the United States: Rationale, design, and preliminary observations from the first 100,000 cases in the Acute Decompensated Heart Failure National Registry (ADHERE). Amer Heart J 2005;149(2):209-16.
- Rubio-Gracia J, Demissei B, Maaten J, et al. Prevalence, predictors and clinical outcome of residual congestion in acute decompensated heart failure. Intern J Cardiol 2018;258:185-91
- Alvarez-Garcia J, Rivas-Lasarte M, Benedicto A, et al. Subclinical pulmonary congestion: a silent and prevalent killer at heart failure discharge. Amer J Cardiol 2020;75(11):1093.
- Кобалава Ж.Д., Сафарова А.Ф., Соловьева А.Е. и др. Легочный застой по данным ультразвукового исследования у пациентов с декомпенсацией сердечной недостаточности. Кардиология 2019;59(8):5-14 [Kobalava ZD, Safarova AF, Soloveva AE, et al. Pulmonary congestion assessed by lung ultrasound in decompensated heart failure. Kardiologiya 2019;59(8):5-14 (In Russ.)].
- McDonagh T, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) with the special contribution of the Heart Failure Association (HFA) of the ESC. Europ Heart J 2021;42(36):3599-726
- Соловьева А.Е., Кобалава Ж.Д., Виллевальде С.В. и др. Прогностическое значение плотности печени при декомпенсации сердечной недостаточности: результаты проспективного наблюдательного исследования, основанные на данных непрямой эластометрии. Кардиология 2018;58(10S):20-32 [Solovyeva AE, Kobalava ZhD, Villevalde SV, et al. Prognostic value of liver stiffness in decompensated heart failure: results of prospective observational transient elastography-based study. Kardiologiia 2018;58(10S):20-32 (In Russ.)].
- Маматов Б.М., Виллевальде С.В., Клименко А.С., Кобалава Ж.Д. Значение биоимпедансного векторного анализа в диагностике субклинического застоя крови у пациентов с декомпенсацией сердечной недостаточности. Клин фармакол тер 2016;25(5):45-9 [Mamatov BM, Villevalde SV, Klimenko AS, Kobalava ZhD. Bioimpedance vector analysis for detecting subclinical congestion in patients with decompensated heart failure. Clin Pharmacol Ther 2016;25(5):45-9 (In Russ.)].
- Massari F, Scicchitano P, Iacoviello M, et al. Multiparametric approach to congestion for predicting long-term survival in heart failure. J Cardiol 2020;75:47-52.
- Kleiner Shochat M, Fudim M, Shotan A, et al. Prediction of readmissions and mortality in patients with heart failure: lessons from the IMPEDANCE-HF extended trial. ESC Heart Fail 2018;5(5):788-99.
- Gheorghiade M, Follath F, Ponikowski P, et al. European Society of Cardiology; European Society of Intensive Care Medicine. Assessing and grading congestion in acute heart failure: a scientific statement from the acute heart failure committee of the heart failure association of the European Society of Cardiology and endorsed by the European Society of Intensive Care Medicine. Eur J Heart Fail 2010;12(5):423-33.
- Piccoli A, Codognotto M, Cianci V, et al. Differentiation of cardiac and noncardiac dyspnea using bioelectrical impedance vector analysis (BIVA). J Card Failure 2012;18(3):226-32.
- Pivetta E, Goffi A, Lupia E, et al. Lung ultrasound-implemented diagnosis of acute decompensated heart failure in the ED: a SIMEU Multicenter Study. Chest 2015;148(1): 202– 10
- Massari F, Scicchitano P, Ciccone M, et al. Bioimpedance vector analysis predicts hospital length of stay in acute heart failure. Nutrition 2019;61:56-60.
